












实验动物与比较医学 ›› 2026, Vol. 46 ›› Issue (2): 261-270.DOI: 10.12300/j.issn.1674-5817.2025.083
唐小杭1( ), 谷颖敏1, 吕阳阳1, 黄明姝1(
), 谷颖敏1, 吕阳阳1, 黄明姝1( )(
)( ), 田雪松2(
), 田雪松2( )(
)( )
)
收稿日期:2025-02-27
修回日期:2025-10-18
出版日期:2026-04-25
发布日期:2026-04-18
通讯作者:
田雪松(1973—),男,博士,研究员,硕士生导师,主要从事中医药防治脑、视网膜疾病研究。E-mail:xuesong.tian@shutcm.edu.cn。ORCID:0000-0001-6162-2856作者简介:唐小杭(1982—),男,硕士,助理实验师,主要从事中药毒理学研究。E-mail:js19820209@163.com。ORCID:0009-0000-6648-1036
基金资助:
TANG Xiaohang1( ), GU Yingmin1, LÜ Yangyang1, HUANG Mingshu1(
), GU Yingmin1, LÜ Yangyang1, HUANG Mingshu1( )(
)( ), TIAN Xuesong2(
), TIAN Xuesong2( )(
)( )
)
Received:2025-02-27
Revised:2025-10-18
Published:2026-04-25
Online:2026-04-18
Contact:
TIAN Xuesong (ORCID: 0000-0001-6162-2856), E-mail: xuesong.tian@shutcm.edu.cn
HUANG Mingshu (ORCID: 0009-0004-7583-8366), E-mail: kou24@hotmail.com
摘要:
目的 比较包含本团队自研固定液在内的4种组织固定液用于制备大鼠眼球组织石蜡切片的组织学染色效果。 方法 将20只5周龄的SPF级雄性SD大鼠,随机分为4组,每组5只。腹腔注射舒泰?50(45 mg/kg体重)麻醉大鼠后,采用腹主动脉放血法安乐死大鼠,沿眼眶完整摘取双侧眼球,分别于体积分数为10%的甲醛固定液、戊二醛-甲醛混合固定液、改良Davidson固定液和自研固定液中固定72 h。固定结束后,沿视神经纵向切开眼球,保留带有视神经的部分组织,脱水、包埋,并制备切片。切片经HE染色后,比较角膜、晶状体、视网膜等眼球结构的组织学染色效果。 结果 10%甲醛组和戊二醛-甲醛组大鼠眼球整体外观出现明显收缩,而改良Davidson固定液组和自研固定液组大鼠眼球形态保持圆润。改良Davidson固定液组、10%甲醛组和自研固定液组的角膜基质层明显断裂,细胞排列不整齐;而戊二醛-甲醛组的角膜细胞排列整齐、未见断裂或褶皱、染色清晰,提示戊二醛-甲醛组的角膜制片效果最佳。10%甲醛组的晶状体赤道和皮质部位出现裂痕,但晶状体纤维结构完整;改良Davidson固定液组的晶状体出现大面积明显破裂和脱片现象;戊二醛-甲醛组仅赤道部位有轻微裂痕,自研固定液组仅晶状体外围部位有轻微红色褶皱,其余结构完整、无破碎,提示戊二醛-甲醛组与自研固定液组的晶状体制片效果最佳。10%甲醛组的视网膜与脉络膜/巩膜层严重分离,各细胞层出现大面积断裂;而戊二醛-甲醛组的视网膜与脉络膜/巩膜层部分分离,外网层和神经纤维层可见分离肿胀,各层细胞排列整齐;改良Davidson固定液和自研固定液的视网膜均完整无断裂,各层结构无分离,在保持视网膜各层细胞完整性、排列整齐度等方面均有优势,但自研固定液组视网膜切片的对比度更高。 结论 固定液的选择对大鼠眼球各结构的形态保存效果具有显著影响。自研固定液在维持眼球整体形态、晶状体结构完整性及视网膜贴合度等方面的综合效果最佳。如果仅针对眼球的角膜结构展开研究,推荐使用戊二醛-甲醛混合固定液。体积分数为10%的甲醛固定液在上述所有眼球结构的固定效果均不理想,不建议用于眼球组织的精细形态学研究。
中图分类号:
唐小杭,谷颖敏,吕阳阳,等. 一种自研固定液用于制备大鼠眼球切片的组织学染色效果评价[J]. 实验动物与比较医学, 2026, 46(2): 261-270. DOI: 10.12300/j.issn.1674-5817.2025.083.
TANG Xiaohang,GU Yingmin,Lü Yangyang,et al. Evaluation of the Histological Staining Performance of Rat Eyeball Sections Prepared Using a Self-Developed Fixative[J]. Laboratory Animal and Comparative Medicine, 2026, 46(2): 261-270. DOI: 10.12300/j.issn.1674-5817.2025.083.
分值(程度) Score(grade) | 评分标准 Scoring criteria |
|---|---|
| 0(正常) | 各层组织结构完整,无裂痕、皱褶或脱片现象;各层细胞染色清晰、排列整齐、形态完整 |
| 1(轻微) | 裂痕、褶皱范围在10%以下,各层结构无分离,断裂;细胞染色清楚、形态完整、无变形 |
| 2(轻度) | 裂痕、褶皱范围在10%~30%,各层结构排列整齐,无分离;细胞染色清楚、组织完整、无变形 |
| 3(中度) | 裂痕、褶皱范围在30%~50%,各层结构分离、断裂;细胞界限不明显,颜色对比度降低,组织明显变形、破碎 |
| 4(重度) | 裂痕、褶皱在50%以上,大范围脱片、破碎明显;细胞界限不明显,颜色对比度降低,组织变形严重、收缩明显、结构不完整 |
表1 眼球HE染色质量的定量评分标准
Table 1 Quantitative scoring criteria for eyeball HE staining quality
分值(程度) Score(grade) | 评分标准 Scoring criteria |
|---|---|
| 0(正常) | 各层组织结构完整,无裂痕、皱褶或脱片现象;各层细胞染色清晰、排列整齐、形态完整 |
| 1(轻微) | 裂痕、褶皱范围在10%以下,各层结构无分离,断裂;细胞染色清楚、形态完整、无变形 |
| 2(轻度) | 裂痕、褶皱范围在10%~30%,各层结构排列整齐,无分离;细胞染色清楚、组织完整、无变形 |
| 3(中度) | 裂痕、褶皱范围在30%~50%,各层结构分离、断裂;细胞界限不明显,颜色对比度降低,组织明显变形、破碎 |
| 4(重度) | 裂痕、褶皱在50%以上,大范围脱片、破碎明显;细胞界限不明显,颜色对比度降低,组织变形严重、收缩明显、结构不完整 |
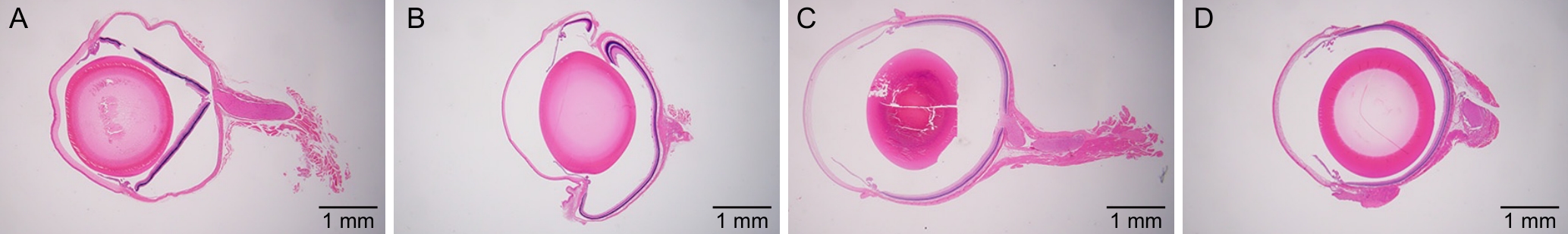
图1 不同固定液组大鼠眼球的整体形态和组织结构(×12.5)
Figure 1 Overall morphology and tissue structure of rat eyeballs in different fixative groups (×12.5)
固定液种类 Fixative types | 眼球圆润度 Sphericality of eyeball | 角膜完整度 Corneal integrity | 晶状体完整度 Lens integrity | 视网膜完整度 Retinal integrity |
|---|---|---|---|---|
| 10%甲醛组(10% Formaldehyde group) | 皱缩、凹陷 | 可见裂隙 | 基本完整 | 完全分离、断裂 |
| 戊二醛-甲醛组(Glutaraldehyde-formaldehyde group) | 皱缩、凹陷 | 完整 | 完整 | 部分分离、断裂 |
| 改良Davidson固定液组(Modified Davidson’s fixative group) | 圆润、无变形 | 明显裂隙 | 破碎 | 完整 |
| 自研固定液组(Self-developed fixative group) | 圆润、无变形 | 有裂隙 | 完整 | 完整 |
表2 不同固定液组大鼠眼球的整体形态和组织结构比较 (n=10)
Table 2 Comparison of overall morphology and tissue structure of rat eyeballs in different fixative groups
固定液种类 Fixative types | 眼球圆润度 Sphericality of eyeball | 角膜完整度 Corneal integrity | 晶状体完整度 Lens integrity | 视网膜完整度 Retinal integrity |
|---|---|---|---|---|
| 10%甲醛组(10% Formaldehyde group) | 皱缩、凹陷 | 可见裂隙 | 基本完整 | 完全分离、断裂 |
| 戊二醛-甲醛组(Glutaraldehyde-formaldehyde group) | 皱缩、凹陷 | 完整 | 完整 | 部分分离、断裂 |
| 改良Davidson固定液组(Modified Davidson’s fixative group) | 圆润、无变形 | 明显裂隙 | 破碎 | 完整 |
| 自研固定液组(Self-developed fixative group) | 圆润、无变形 | 有裂隙 | 完整 | 完整 |
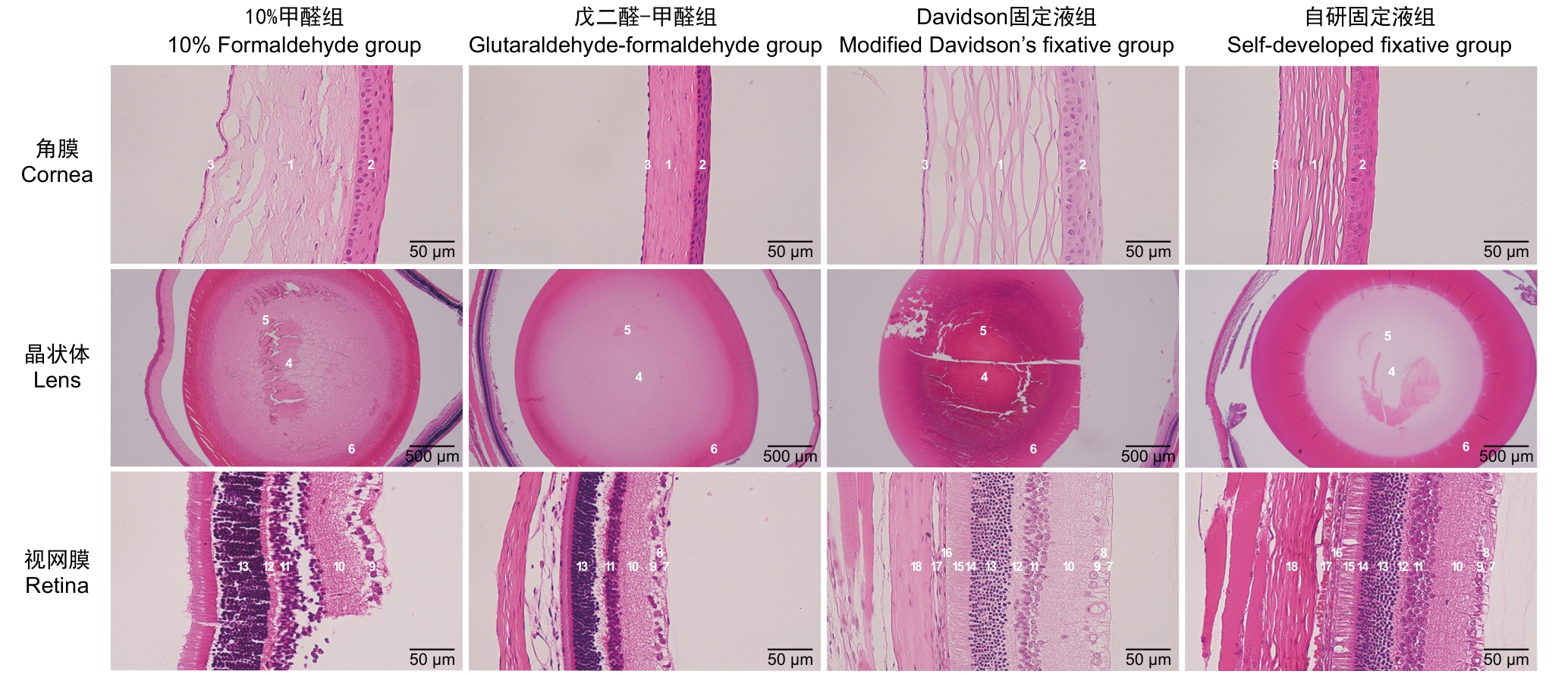
图2 显微镜下不同固定液组大鼠的眼球结构
Figure 2 Microscopic observation of rat eyeballs structures in different fixative groups
观察指标 Observation indicators | 10%甲醛组 10% Formaldehyde group | 戊二醛-甲醛组 Glutaraldehyde-formaldehyde group | 改良Davidson固定液组 Modified Davidson’s fixative group | 自研固定液组 Self-developed fixative group | |
|---|---|---|---|---|---|
角膜 Cornea | 结构完整度 | 基质层明显裂痕 | 紧密 | 基质层明显裂痕 | 基质层轻微裂痕 |
| 各层结构 | 褶皱不规则、完整性差,上皮层与基质层分离 | 整齐、紧密无断裂 | 褶皱不规则、完整性差,上皮层与基质层分离明显 | 完整性尚可,基质层结构不紧密 | |
| 细胞紧密程度 | 裂隙较多 | 整齐无裂隙 | 裂隙较多 | 裂隙轻微 | |
| 染色情况 | 淡染 | 鲜艳 | 淡染 | 鲜艳 | |
晶状体 Lens | 结构完整度 | 赤道和皮质有裂痕 | 完整 | 大面积破碎、脱片 | 外围轻微褶皱 |
| 细胞紧密程度 | 有裂隙 | 整齐无裂隙 | 有裂隙 | 整齐无裂隙 | |
| 染色情况 | 鲜艳 | 鲜艳 | 深染 | 鲜艳 | |
视网膜 Retina | 完整度 | 断裂,部分结构脱落 | 较少断裂 | 完整无断裂 | 完整无断裂 |
| 各层结构 | 与脉络膜/巩膜严重分离 | 外网层分离肿胀,神经纤维层分离肿胀 | 各层完整无分离 | 各层完整无分离 | |
| 细胞紧密程度 | 大面积裂隙 | 部分有裂隙 | 整齐无裂隙 | 整齐无裂隙 | |
| 染色情况 | 鲜艳 | 鲜艳 | 淡染 | 鲜艳 | |
表3 不同固定液组大鼠眼球组织结构比较
Table 3 Comparison of the histological structure of rat eyeballs in different fixative groups
观察指标 Observation indicators | 10%甲醛组 10% Formaldehyde group | 戊二醛-甲醛组 Glutaraldehyde-formaldehyde group | 改良Davidson固定液组 Modified Davidson’s fixative group | 自研固定液组 Self-developed fixative group | |
|---|---|---|---|---|---|
角膜 Cornea | 结构完整度 | 基质层明显裂痕 | 紧密 | 基质层明显裂痕 | 基质层轻微裂痕 |
| 各层结构 | 褶皱不规则、完整性差,上皮层与基质层分离 | 整齐、紧密无断裂 | 褶皱不规则、完整性差,上皮层与基质层分离明显 | 完整性尚可,基质层结构不紧密 | |
| 细胞紧密程度 | 裂隙较多 | 整齐无裂隙 | 裂隙较多 | 裂隙轻微 | |
| 染色情况 | 淡染 | 鲜艳 | 淡染 | 鲜艳 | |
晶状体 Lens | 结构完整度 | 赤道和皮质有裂痕 | 完整 | 大面积破碎、脱片 | 外围轻微褶皱 |
| 细胞紧密程度 | 有裂隙 | 整齐无裂隙 | 有裂隙 | 整齐无裂隙 | |
| 染色情况 | 鲜艳 | 鲜艳 | 深染 | 鲜艳 | |
视网膜 Retina | 完整度 | 断裂,部分结构脱落 | 较少断裂 | 完整无断裂 | 完整无断裂 |
| 各层结构 | 与脉络膜/巩膜严重分离 | 外网层分离肿胀,神经纤维层分离肿胀 | 各层完整无分离 | 各层完整无分离 | |
| 细胞紧密程度 | 大面积裂隙 | 部分有裂隙 | 整齐无裂隙 | 整齐无裂隙 | |
| 染色情况 | 鲜艳 | 鲜艳 | 淡染 | 鲜艳 | |
观察指标 Observation indicators | 分值/程度 Score/grade | 角膜 Cornea | 晶状体 Lens | 视网膜 Retina |
|---|---|---|---|---|
10%甲醛组 10% Formaldehyde group | 0(正常) | 0 | 0 | 0 |
| 1(轻微) | 0 | 1 | 0 | |
| 2(轻度) | 4 | 5 | 0 | |
| 3(中度) | 4 | 4 | 1 | |
| 4(重度) | 2 | 0 | 9 | |
戊二醛-甲醛组 Glutaraldehyde-formaldehyde group | 0(正常) | 6 | 2 | 0 |
| 1(轻微) | 4 | 5 | 0 | |
| 2(轻度) | 0 | 3 | 4 | |
| 3(中度) | 0 | 0 | 5 | |
| 4(重度) | 0 | 0 | 1 | |
改良Davidson固定液组 Modified Davidson’s fixative group | 0(正常) | 0 | 0 | 8 |
| 1(轻微) | 0 | 0 | 2 | |
| 2(轻度) | 0 | 0 | 0 | |
| 3(中度) | 2 | 0 | 0 | |
| 4(重度) | 8 | 10 | 0 | |
自研固定液组 Self-developed fixative group | 0(正常) | 0 | 2 | 9 |
| 1(轻微) | 0 | 6 | 1 | |
| 2(轻度) | 0 | 2 | 0 | |
| 3(中度) | 3 | 0 | 0 | |
| 4(重度) | 7 | 0 | 0 |
表4 不同固定液组大鼠眼球的组织学评分 (n)
Table 4 Histological scoring results of rat eyeballs in different fixative groups
观察指标 Observation indicators | 分值/程度 Score/grade | 角膜 Cornea | 晶状体 Lens | 视网膜 Retina |
|---|---|---|---|---|
10%甲醛组 10% Formaldehyde group | 0(正常) | 0 | 0 | 0 |
| 1(轻微) | 0 | 1 | 0 | |
| 2(轻度) | 4 | 5 | 0 | |
| 3(中度) | 4 | 4 | 1 | |
| 4(重度) | 2 | 0 | 9 | |
戊二醛-甲醛组 Glutaraldehyde-formaldehyde group | 0(正常) | 6 | 2 | 0 |
| 1(轻微) | 4 | 5 | 0 | |
| 2(轻度) | 0 | 3 | 4 | |
| 3(中度) | 0 | 0 | 5 | |
| 4(重度) | 0 | 0 | 1 | |
改良Davidson固定液组 Modified Davidson’s fixative group | 0(正常) | 0 | 0 | 8 |
| 1(轻微) | 0 | 0 | 2 | |
| 2(轻度) | 0 | 0 | 0 | |
| 3(中度) | 2 | 0 | 0 | |
| 4(重度) | 8 | 10 | 0 | |
自研固定液组 Self-developed fixative group | 0(正常) | 0 | 2 | 9 |
| 1(轻微) | 0 | 6 | 1 | |
| 2(轻度) | 0 | 2 | 0 | |
| 3(中度) | 3 | 0 | 0 | |
| 4(重度) | 7 | 0 | 0 |
组别 Group | 角膜 Cornea | 晶状体 Lens | 视网膜 Retina |
|---|---|---|---|
| 改良Davidson固定液组(Modified Davidson’s fixative group) | 3.80±0.42 | 4.00±0.00 | 0.20±0.42 |
| 10%甲醛组(10% Formaldehyde group) | 2.80±0.79** | 2.30±0.67** | 3.90±0.32** |
| 戊二醛-甲醛组(Glutaraldehyde-formaldehyde group) | 0.40±0.52** | 1.10±0.74** | 2.70±0.67** |
| 自研固定液组(Self-developed fixative group) | 3.70±0.48 | 1.00±0.67** | 0.10±0.32 |
表5 不同固定液对大鼠眼球各部位切片的制备的效果评价 (
Table 5 Evaluation of sectioning quality of different parts of rat eyeballs in different fixative groups
组别 Group | 角膜 Cornea | 晶状体 Lens | 视网膜 Retina |
|---|---|---|---|
| 改良Davidson固定液组(Modified Davidson’s fixative group) | 3.80±0.42 | 4.00±0.00 | 0.20±0.42 |
| 10%甲醛组(10% Formaldehyde group) | 2.80±0.79** | 2.30±0.67** | 3.90±0.32** |
| 戊二醛-甲醛组(Glutaraldehyde-formaldehyde group) | 0.40±0.52** | 1.10±0.74** | 2.70±0.67** |
| 自研固定液组(Self-developed fixative group) | 3.70±0.48 | 1.00±0.67** | 0.10±0.32 |
| [1] | 成前, 李月, 王伟进, 等. 中国老年人口健康状况及其家庭照料需求预测[J]. 人口学刊, 2024, 46(5):73-89. DOI: 10.16405/j.cnki.1004-129X.2024.05.005 . |
| CHENG Q, LI Y, WANG W J, et al. The prediction of health status and family care needs of the elderly people in China[J]. Popul J, 2024, 46(5):73-89. DOI: 10.16405/j.cnki.1004-129X.2024.05.005 . | |
| [2] | 王余萍, 袁源智. 青光眼视神经损害机制[J]. 中国临床医学, 2016, 23(5):667-671. DOI: 10.12025/j.issn.1008-6358.2016.2016 0290 . |
| WANG Y P, YUAN Y Z. Mechanisms of glaucomatous optic neuropathy[J]. Chin J Clin Med, 2016, 23(5):667-671. DOI: 10.12025/j.issn.1008-6358.2016.20160290 . | |
| [3] | 蔡永民. 白内障发病机制及治疗进展研究[J]. 医学理论与实践, 2020, 33(15):2450-2452. DOI: 10.19381/j.issn.1001-7585.2020.15.012 . |
| CAI Y M. Research on pathogenesis and therapeutic advances of cataract[J]. J Med Theory Pract, 2020, 33(15):2450-2452. DOI: 10.19381/j.issn.1001-7585.2020.15.012 . | |
| [4] | 葛军, 朱思泉. 中医药治疗老年性黄斑变性的研究进展[J]. 中医临床研究, 2023, 15(21):74-78. DOI: 10.3969/j.issn.1674-7860.2023.21.014 . |
| GE J, ZHU S Q. A review on the TCM treatment of age-related macular degeneration[J]. Clin J Chin Med, 2023, 15(21):74-78. DOI: 10.3969/j.issn.1674-7860.2023.21.014 . | |
| [5] | 裴希. 螺内酯与缬沙坦对氧诱导小鼠视网膜病变新生血管抑制作用及机制的初步探讨[D]. 广州: 南方医科大学, 2014. |
| PEI X. A Preliminary Study on the Inhibitory effects and mechanisms of spironolactone and valsartan on oxygen-induced retinopathy neovascularization in mice[D]. Guangzhou: Southern Medical University, 2014. | |
| [6] | 孙河龙, 李耀洋, 李丹, 等. 组织固定液与固定方法选择的探讨[J]. 甘肃医药, 2019, 38(12):1061-1064, 1069. DOI: 10.15975/j.cnki.gsyy.2019.12.002 . |
| SUN H L, LI Y Y, LI D, et al. Selection of tissue fixation fluid and fixation method[J]. Gansu Med J, 2019, 38(12):1061-1064, 1069. DOI: 10.15975/j.cnki.gsyy.2019.12.002 . | |
| [7] | SCHAFER K A, EIGHMY J, FIKES J D, et al. Use of severity grades to characterize histopathologic changes[J]. Toxicol Pathol, 2018, 46(3): 256-265. DOI: 10.1177/0192623318761348 . |
| [8] | 李晶晶, 朱鸿, 施彩虹. 三种方法对大鼠视网膜固定效果的比较研究[J]. 上海交通大学学报(医学版), 2011, 31(8):1105-1107. DOI: 10.3969/j.issn.1674-8115.2011.08.013 . |
| LI J J, ZHU H, SHI C H. Outcomes of rat retina fixation with three different methods[J]. J Shanghai Jiaotong Univ Med Sci, 2011, 31(8):1105-1107. DOI: 10.3969/j.issn.1674-8115.2011.08.013 . | |
| [9] | 王松涛, 肖虹蕾, 王敏, 等. 四种不同固定液固定小鼠视网膜效果的比较研究[J]. 眼科新进展, 2016, 36(8):709-712. DOI: 10.13389/j.cnki.rao.2016.0188 . |
| WANG S T, XIAO H L, WANG M, et al. Comparative study of mouse retinal fixation outcomes with four different fixation solutions[J]. Recent Adv Ophthalmol, 2016, 36(8):709-712. DOI: 10.13389/j.cnki.rao.2016.0188 . | |
| [10] | 张遐, 鞠躬, 董光皎. 甲醛和戊二醛应用于神经系统免疫组织化学组织固定的特性分析[J]. 神经解剖学杂志, 1990, 6(2):249-256. |
| ZHANG X, JU G, DONG G J. Analysis of the properties of formaldehyde and glutaraldehyde for tissue fixation in neural system immunohistochemistry[J]. Chin J Neuroanat, 1990, 6(2):249-256. | |
| [11] | 宋惠欣, 蒋文君, 毕宏生. 三种不同固定液对豚鼠眼球的固定效果比较[J]. 国际眼科杂志, 2018, 18(6):1010-1013. DOI: 10.3980/j.issn.1672-5123.2018.6.07 . |
| SONG H X, JIANG W J, BI H S. A comparative study on the effect of fixation for guinea pigs eyeballs among three different fixation solution[J]. Int Eye Sci, 2018, 18(6):1010-1013. DOI: 10.3980/j.issn.1672-5123.2018.6.07 . | |
| [12] | 张文忻, 李永平, 林健贤, 等. 冰醋酸固定液对视网膜组织固定效果的探讨[J]. 眼科学报, 2006, 22(2):112-114. DOI: 10.3969/j.issn.1000-4432.2006.02.012 . |
| ZHANG W X, LI Y P, LIN J X, et al. The investigation of FFA fixative solution for retina[J]. Eye Sci, 2006, 22(2):112-114. DOI: 10.3969/j.issn.1000-4432.2006.02.012 . | |
| [13] | 赵宝忠, 刘俊华, 高俊琴, 等. 乙醇类固定剂对组织细胞处理性能的实验评价[J]. 临床与实验病理学杂志, 2012, 28(2):223-225. DOI: 10.3969/j.issn.1001-7399.2012.02.033 . |
| ZHAO B Z, LIU J H, GAO J Q, et al. Experimental evaluation of ethanol-based fixatives for the processing of tissues and cells[J]. Chin J Clin Exp Pathol, 2012, 28(2):223-225. DOI: 10.3969/j.issn.1001-7399.2012.02.033 . | |
| [14] | TOKUDA K, BARON B, KURAMITSU Y, et al. Optimization of fixative solution for retinal morphology: a comparison with Davidson's fixative and other fixation solutions[J]. Jpn J Ophthalmol, 2018, 62(4):481-490. DOI: 10.1007/s10384-018-0592-7 . |
| [15] | WANG H, YANG L L, JI Y L,et al. Different fixative methods influence histological morphology and TUNEL staining in mouse testes[J].Reprod Toxicol, 2016, 60:53-61.DOI: 10.1016/j.reprotox.2016.01.006 . |
| [16] | BAK S Y, LEE S W, CHOI C H, et al. Assessment of the influence of acetic acid residue on typeⅠcollagen during isolation and characterization[J]. Materials, 2018, 11(12):2518. DOI: 10.3390/ma11122518 . |
| [17] | 郭志鲲. 蛋白质变性作用研究动向[J]. 生物化学与生物物理进展, 1974, 1(4):16-22, 49. DOI: CNKI:SUN:SHSW.0.1974-04-006 . |
| GUO Z K. Advances in the study of protein denaturation[J]. Prog Biochem Biophys, 1974, 1(4):16-22, 49. DOI: CNKI:SUN:SHSW.0.1974-04-006 . | |
| [18] | POSOKHOV Y O, KYRYCHENKO A. Effect of acetone accumulation on structure and dynamics of lipid membranes studied by molecular dynamics simulations[J]. Comput Biol Chem, 2013, 46:23-31. DOI: 10.1016/j.compbiolchem.2013. 04.005 . |
| [19] | AL-GHOUL K J, COSTELLO M J. Fiber cell morphology and cytoplasmic texture in cataractous and normal human lens nuclei[J]. Curr Eye Res, 1996, 15(5):533-542. DOI: 10.3109/0271 3689609000764 . |
| [20] | 常晓杰, 徐颖超, 刘畅. 不同实验方法检测常用有机溶剂对细菌活性的影响及其安全使用限量[J]. 微生物学通报, 2016, 43(7):1635-1645. DOI: 10.13344/j.microbiol.china.150595 . |
| CHANG X J, XU Y C, LIU C. Effects of common solvent concentrations on bacterial activities[J]. Microbiol China, 2016, 43(7):1635-1645. DOI: 10.13344/j.microbiol.china.150595 . | |
| [21] | 黄熙泰, 于自然, 李翠凤. 现代生物化学[M]. 3版. 北京: 化学工业出版社, 2012. |
| HUANG X T, YU Z R, LI C F. Modern Biochemistry[M]. 3rd. Beijing: Chemical Industry Press, 2012. | |
| [22] | ZAZERI G, POVINELLI A P R, PAVAN N M, et al. Solvent-induced lag phase during the formation of lysozyme amyloid fibrils triggered by sodium dodecyl sulfate: biophysical experimental and in silico study of solvent effects[J]. Molecules, 2023, 28(19):6891. DOI: 10.3390/molecules 2819 6891 . |
| [23] | SUN N, SHIBATA B, HESS J F, et al. An alternative means of retaining ocular structure and improving immunoreactivity for light microscopy studies[J]. Mol Vis, 2015, 21:428-442. |
| [24] | 秦川. 实验动物比较组织学彩色图谱[M]. 北京: 科学出版社, 2017: 234-241, 247. |
| Qin C. Color atlas of comparative histology of laboratory animals[M]. Beijing: Science Press, 2017: 234-241, 247. |
| [1] | 宋静, 杨宗统, 李晓晶, 李自发, 苏凤云, 徐东川, 隋在云. 泻白散对过敏性哮喘大鼠肺、肠组织形态结构及PI3K和Akt表达水平的影响[J]. 实验动物与比较医学, 2026, 46(2): 191-204. |
| [2] | 姜海涛, 袁韩涛, 黄雯婷, 杨蓉蓉, 陈晓春, 禹宝庆, 李四波. 腰舒逐瘀方通过miR-17-5P/MDM2/p53通路调控大鼠椎间盘纤维环细胞增殖与凋亡[J]. 实验动物与比较医学, 2026, 46(1): 55-65. |
| [3] | 高超奇, 祝志波, 孙显东. 大鼠血管重构模型的应用进展与分类分析[J]. 实验动物与比较医学, 2025, 45(5): 542-550. |
| [4] | 罗一凡, 张臻玮, 梅璐, 史叶萍, 邢艺彤, 张泽奇, 李楚欣, 韩春霞, 杨平顺, 陈秋生. 特络细胞介导肥胖症大鼠膏摩寡肽中草药复合制剂的减肥作用及其机制[J]. 实验动物与比较医学, 2025, 45(5): 551-560. |
| [5] | 曹星新, 李艾亦, 侯婧涵, 李明学, 李艳艳, 靳玮华, 杨凤梅, 段素琴, 和占龙. 黄芪或其成分治疗急性胰腺炎的动物实验Meta分析[J]. 实验动物与比较医学, 2025, 45(5): 561-573. |
| [6] | 秦超, 李双星, 赵婷婷, 蒋晨晨, 赵晶, 杨艳伟, 林志, 王三龙, 文海若. 药物安全评价用SD大鼠90 d喂养试验的背景数据研究[J]. 实验动物与比较医学, 2025, 45(4): 439-448. |
| [7] | 刘力瑜, 嵇波, 刘小玄, 方洋, 张玲, 郭亭廷, 全烨, 李鹤文, 刘翼天. 大鼠胎儿期肺组织固定方法的探索[J]. 实验动物与比较医学, 2025, 45(4): 432-438. |
| [8] | 肖林林, 杨逸萱, 黎珊杉, 罗兰诗雨, 尹思威, 孙俊铭, 施维, 欧阳轶强, 李习艺. 利用脑立体定位技术将人源三突变APP基因导入海马区构建阿尔茨海默病大鼠模型[J]. 实验动物与比较医学, 2025, 45(3): 269-278. |
| [9] | 刘智伟, 杨然, 连浩, 张玉, 金立伦. 秦皮素对碘乙酸钠诱导骨关节炎模型大鼠的软骨保护与抗炎作用[J]. 实验动物与比较医学, 2025, 45(3): 259-268. |
| [10] | 姜萌, 郝淑兰, 仝立国, 仲启明, 高振飞, 王永辉, 王晞星, 吉海杰. 长春瑞滨诱导大鼠足背静脉炎模型的动态评价[J]. 实验动物与比较医学, 2025, 45(3): 251-258. |
| [11] | 潘颐聪, 蒋汶洪, 胡明, 覃晓. 慢性肾脏病大鼠主动脉钙化模型的术式优化及效果评价[J]. 实验动物与比较医学, 2025, 45(3): 279-289. |
| [12] | 连辉, 姜艳玲, 刘佳, 张玉立, 谢伟, 薛晓鸥, 李健. 异常子宫出血大鼠模型的构建与评价[J]. 实验动物与比较医学, 2025, 45(2): 130-146. |
| [13] | 吴海凤, 周小江, 李晨江, 李怀银, 高明. 6种复合固定液对金黄仓鼠视网膜组织固定效果的比较[J]. 实验动物与比较医学, 2024, 44(6): 675-681. |
| [14] | 孙效容, 苏丹, 贵文娟, 陈玥. 手术诱导大鼠中重度膝骨关节炎模型的建立与评价[J]. 实验动物与比较医学, 2024, 44(6): 597-604. |
| [15] | 殷玉莲, 马丽娜, 屠思远, 陈玲, 叶媚娜, 陈红风. 非哺乳期乳腺炎大鼠模型的建立及评价[J]. 实验动物与比较医学, 2024, 44(6): 587-596. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||