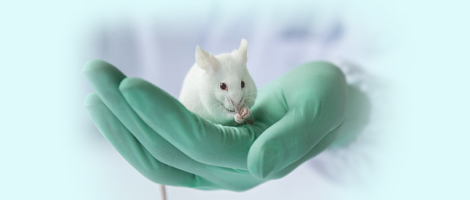
线粒体是真核细胞中高度动态的双膜结构细胞器,作为 “能量工厂”,为细胞内各类生命活动提供能量——ATP。除产生能量外,线粒体还参与钙信号调节、活性氧生成和程序性死亡触发,其功能完整性对维持细胞稳态至关重要[1]。当线粒体功能失调时,会导致ATP合成减少、氧化应激加剧和凋亡通路激活异常,进而引发多种病理状态[1-2]。近年的研究表明,线粒体与衰老及多种年龄相关疾病密切相关[3]。线粒体并非静态细胞器,而是高度动态的管网系统,受线粒体融合(fusion)和分裂(fission)过程持续不断的调控[2]。这种动态平衡对维持细胞内线粒体群体质量至关重要——融合促进代谢协同和嵴网络重组,分裂则有利于受损线粒体的自噬清除[1]。正常线粒体的融合和分裂在线粒体DNA(mitochondrial DNA,mtDNA) 维持[4]、细胞周期进程和代谢调节中发挥着重要作用[5]。
秀丽隐杆线虫(Caenorhabditis elegans,C. elegans,以下简称线虫)是重要的模式生物,在线粒体研究中具有独特的优势:第一,生命周期短(约2~3周),非常适合用于快速评估基因或药物对衰老过程中线粒体变化的影响;第二,遗传背景清晰,已有成熟的基因操作技术,可对基因功能进行高效筛选和验证;第三,线虫全身透明,允许利用荧光探针或荧光蛋白,在活体动物中对特定组织(如肌肉或神经元)的线粒体形态、动态及功能进行无创、实时和高分辨率成像,甚至可以对同一个体从发育到衰老的全过程进行纵向追踪;第四,线粒体的核心功能通路,尤其是调控能量代谢和寿命的通路,在从线虫到人类的进化过程中高度保守,使得线虫成为比较医学研究的有力工具[6]。目前,线虫模型已被成功应用于模拟人类多种与线粒体功能障碍相关的疾病,如帕金森病、亨廷顿病和线粒体心肌病[7]。利用线虫进行大规模药物筛选或遗传抑制因子筛选,能够快速鉴定出潜在的治疗靶点,为后续在哺乳动物的模型研究中提供有力的线索和理论基础[8-10]。因此,基于线虫模型的系统、可靠的线粒体分析方法探索,对于推动衰老生物学和转化医学发展具有至关重要的意义。
本文以野生型线虫年轻(young adult)和衰老(aged adult)群体为模型,系统总结了本实验室对线粒体进行多尺度分析的研究方法与相关经验,并为不同类型线粒体的形态分析提供了详细的插件介绍和批量处理宏,以帮助读者掌握分析技巧;此外,采用Seahorse XF细胞能量代谢分析系统,定量展示了线粒体氧化磷酸化功能随衰老的动态变化规律[11],并讨论了实验中常遇到的问题和部分解决方案,以供同行借鉴。
1 线虫线粒体荧光图像获取
1.1 线虫培养及同步化方法
本文涉及的野生型秀丽隐杆线虫N2,突变品系SJ4103 zcIs14[myo-3::GFP(mit)]购自美国明尼苏达大学线虫遗传中心(Caenorhabditis Genetics Center,CGC),突变品系CZ22488 col-19p-mito::dendra2(juSi271)I由徐素宏实验室赠予。
线虫固体生长培养基(C. elegans growth medium,NGM)和M9溶液按照标准制备[12]。OP50细菌培养使用蛋白胨(购自英国Oxoid公司,货号LP0042B)、酵母粉(购自英国Oxoid公司,货号LP0021B)和琼脂粉(购自中国ABCONE公司,货号A42307)制备。NGM培养基使用蛋白胨(购自美国Gibco公司,货号211677)和琼脂粉(购自美国BD公司,货号214040)制备。线虫在20 ℃恒温培养箱内(购自德国Binder公司,货号KB400)培养,同时保证实验室温度维持在(20 ± 1)℃。
将20条产卵期成虫挑至10 cm NGM培养基上,放置4 h后将成虫移出,其后代即为同步化线虫。同步化3 d后获得成虫期第1天的线虫。将成虫期第1天的线虫按照20条/盘挑至6 cm NGM培养基上,此后每2天将线虫转移至新的6 cm NGM培养基上以除去后代,至成虫期第8天或第10天。
1.2 荧光图像拍摄方法
在体视显微镜(购自日本Olympus公司,型号SZ61)上挑取线虫,使用5 mmol/L左旋咪唑(购自美国Sigma-Aldrich公司,货号31742)对线虫进行麻醉,并将其固定在滴有5%琼脂垫的玻璃载玻片上,盖上盖玻片。使用Olympus BX53生物显微镜对线虫外阴至尾部中段区域进行拍摄。
2 线粒体形态分析
2.1 图像的批量操作
图像前处理和使用Mitochondria Analyzer插件定量分析线粒体形态涉及大量图像数据的处理。这些图像需施加相同的处理流程,批量操作技术可实现自动化处理,该技术可显著提升处理效率,大幅降低时间成本,为后续分析奠定了高效基础。
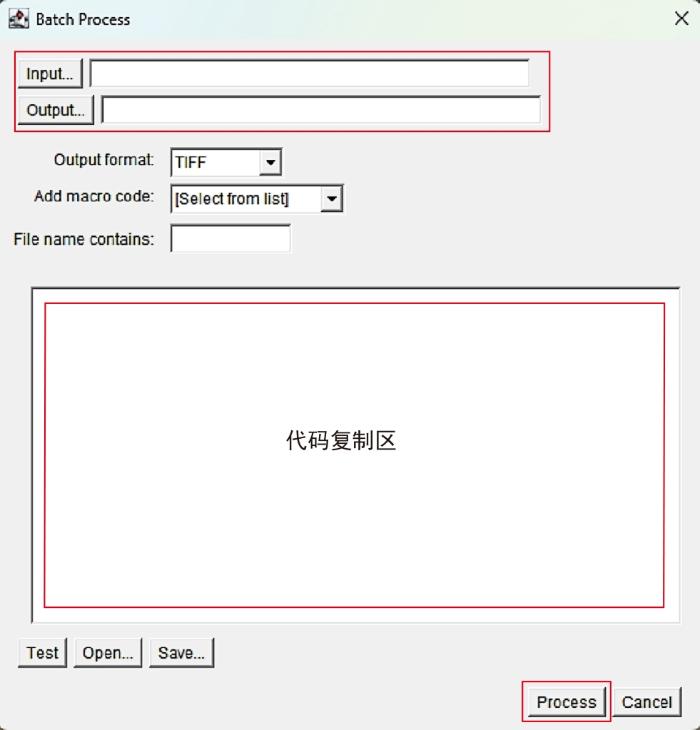
打开Fiji软件基于宏的批量处理(Process-Batch-Macro),Input选择输入文件夹,Output选择输出文件夹。注意输入和输出文件夹不能为同一个,否则会覆盖原始图片。将图像前处理和使用Mitochondria Analyzer插件定量分析线粒体形态所述代码复制在代码复制区内,之后点击Process运行即可完成批量操作(图1)。
图1
图1
Batch Process操作界面介绍
Figure 1
Introduction to Batch Process operation interface
2.2 图像前处理
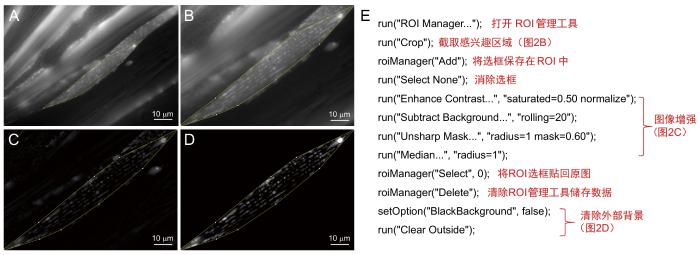
使用Fiji软件的多边形选择工具(polygon selection tool)精确框定感兴趣区域(region of interest, ROI)(图2A),将ROI图像单独保存至新建目录,建立标准化批量处理工作流。对ROI图像进行二次截取(图2B),以避免后续ROI重定位时的配准误差。使用Olympus BX53生物显微镜拍摄的图像存在显著背景荧光干扰,使用共聚焦显微镜拍摄的图像存在随机噪声污染,以上因素均会影响软件在形态测量时的准确度。采用反卷积算法(deconvolution)进行基础图像增强。在Fiji中可应用复合滤波策略:Fiji的[process-filters]模块集成多种数字滤波算法,在批量处理前根据图片实际情况获得设置参数,以获取更贴合原始数据的前处理图像。此处使用了Enhance Contrast + Subtract Background + Unsharp Mask + Median联合处理,即经过“增强反差”“去除背景”“锐化”“中值滤波”这一系列处理来增强图像(图2C)。预处理后执行背景清零(Background Clear,图2D)命令。图像的批量操作可使用如下宏(图2E)。该宏的核心功能通过ROI Manager实现选区存储与动态调用,目的是在图像增强前自动移除ROI边界,此时处理对象为全图,否则将只对选框内部分进行局部处理。全图处理模式可避免局部增强导致的边界伪影,防止处理后的边界信号被误识别为有效信号。
图2
图2
前处理步骤及注释
Figure 2
Preprocessing procedures and annotations
2.3 线粒体形态分类
图3
图3
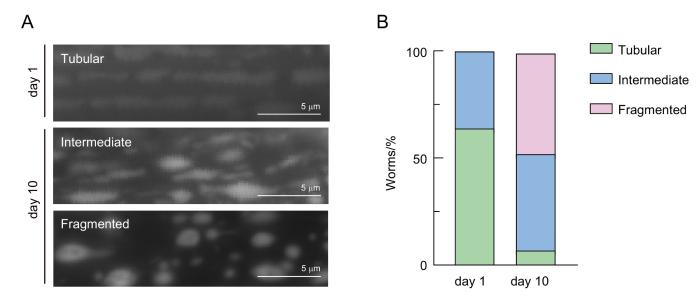
线虫肌肉细胞线粒体形态分类
Figure 3
Classification of mitochondrial morphology in C. elegans muscle cells
2.4 使用Mitochondria Analyzer插件定量分析线粒体形态
Mitochondria Analyzer插件融合了早期用于统计线粒体圆度的插件MorphoLibJ,可以对点状、管状和分支线粒体的形态、动力学和功能进行定量分析[16]。二维(2D)图像运行结果包括线粒体的面积(area)、周长(perimeter)、外形因数(form factor)、长宽比(aspect ratio),以及网络分支数(branches)、分支长度(branch lengths)和分支连接(branch junctions)。
安装方法[17]:导航至[Image-Help-Update...]打开更新界面,选择[Manage Update Sites],勾选3D ImageJ Suite、ImageScience和IJPB-Plugins,点击底部[Add Update Site]创建新条目,在Name列下键入“Mitochondria Analyzer”,在URL列下键入
使用该插件需要先在[Image-Properties]中将像素单位设置为micron(图4A),并只支持8-bit格式。点击运行[Plugins-Mitochondria Analyzer-2D-2D Threshold Optimize]确定Block size和C-value参数(图4B),该结果会返回一个包含所选范围内所有参数组合的参数矩阵图,选择最优参数组合。该插件的2D Threshold已包含去除背景和增强信号的预处理步骤,本文中的数据选择用经本文图像前处理章节方法处理后的图像,导入并使用该插件的前处理步骤进行二次处理(图4C)。然后运行[Plugins-Mitochondria Analyzer-2D-2D Threshold],将上述Block size和C-value参数输入,返还二值化图像(图4D)。最后运行[Plugins-Mitochondria Analyzer-2D-2D Analysis],获得包括数量、面积和骨架信息等最终结果。该插件的骨架分析采用Skeletonize(2D/3D)算法实现(图4E)。图像批量操作可用以下宏(图4F),结果将累计输出在结果列表中,数据单位为μm 或 μm²。需要注意的是,若没有先完成图4A中的步骤,则会在运行宏的第二步时报错。
图4
图4
Mitochondria Analyzer插件步骤及注释
Figure 4
Procedures and annotations of Mitochondria Analyzer plugin
2.5 使用MiNA–Mitochondrial Network Analysis插件定量分析线粒体形态
MiNA插件适用于分支状和网络状线粒体的长度测量及线粒体分支程度评估[18]。该工具从图像的二值化副本中获取线粒体面积(或体积),并用拓扑骨架估计线粒体结构的长度,生成骨架和面积的叠加图(或3D渲染)以评估分析的准确性。MiNA运行结果包括单独个体结构(individuals)、网络结构(networks)、平均分支长度(mean branch length)、分支长度中位数(median branch length)、长度标准偏差(length standard deviation)、平均网络结构大小(mean network size)、网络结构大小中位数(median network size)、网络结构大小标准偏差(network size standard deviation)以及线粒体足迹(mitochondrial footprint)。
安装方法[19]:在[Image-Help-Update…]中打开更新界面,选择[Manage Update Sites],勾选StuartLab,Biomedgroup,点击[Close-Apply Changes]。
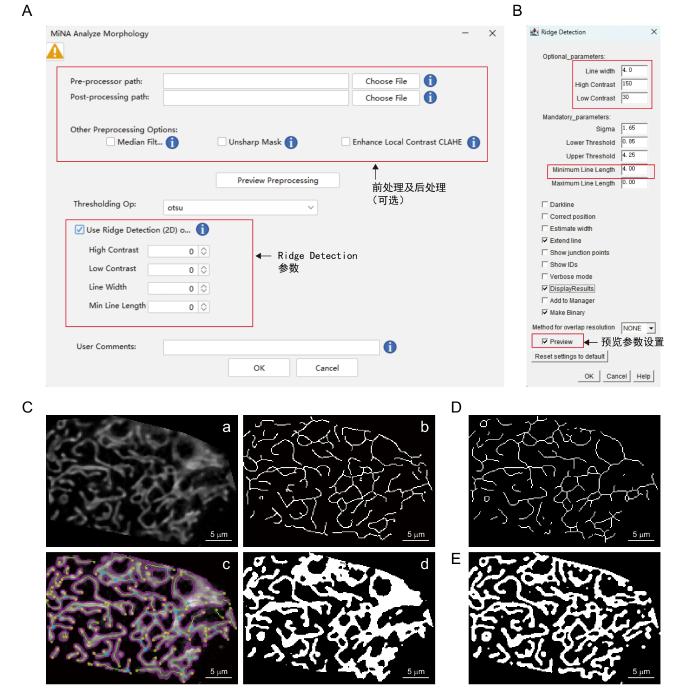
运行[Plugins-StuartLab-MiNA Analyze Morphology],MiNA包含可选的将原始图像转换为二值化图像的前处理(Pre-processor path)和后处理步骤(Post-processing path)(图5A),也可直接使用本文图像前处理章节进行操作。勾选Use Ridge Detection(2D only),参数的优化可预先在[Plugins-Ridge Detection-Preview]中进行(图5B),以接近视觉拓扑结构,从而减少引入偏差。若不勾选则会使用Skeletonize(2D/3D)获取骨架信息(与Mitochondria Analyzer相同)。
图5
图5
MiNA - Mitochondrial Network Analysis插件步骤及注释
Figure 5
Procedures and annotations of MiNA - Mitochondrial Network Analysis plugin
MiNA插件的分析包括两部分:(1)二值化图像获取面积或体积。阈值处理默认为Otsu,在[Auto Threshold]中可预览其他算法。输出为洋红色边框记线粒体区域(图5C-b、d)。(2)二次简化图像获取长度和分支。勾选Using Ridge Detection(2D only)选择框后设置High contrast、Low contrast、Line width、Min Line length四个参数并运行(图5A)。返还结果为绿色骨架标记分支结构(图5C-b、d)。在图5实例中,可以明显看到当图像局部背景较高时,使用两种不同算法生成的面积(图5C-b、D)和骨架(图5C-c、E)。因此,需要根据实际图像情况选择合适的处理方法。由于该插件套用了其他插件,暂无法进行批量处理。
2.6 线粒体形态分析实例
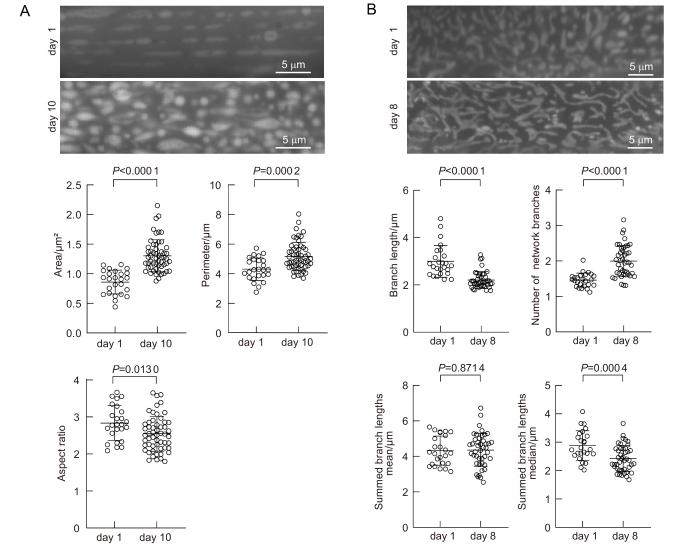
以年轻和年老线虫为例。使用Mitochondria Analyzer插件对年轻和年老线虫肌肉线粒体进行定量统计,使用MiNA-Mitochondrial Network Analysis插件对年轻和年老线虫表皮线粒体进行定量统计。使用GraphPad Prism(version 8.0)进行数据分析并统计作图。使用非配对t检验对不少于20条线虫进行统计分析,图中显示平均数和标准差。
结果显示,与年轻线虫相比,年老线虫肌肉的线粒体面积增大(P<0.000 1)、周长增加(P=0.000 2);纵横比的减少(P=0.013 0)间接反映了线粒体圆度的增加(图6A)。与年轻线虫相比,年老线虫表皮线粒体分支长度显著减小(P<0.000 1),网络数量显著增加(P<0.000 1)(图6B);年老线虫表皮线粒体独立骨架长度平均值没有显著性变化(P=0.871 4),独立骨架长度中位数显著减小(P=0.000 4)(图6B)。说明随着年龄衰老,表皮细胞线粒体同时发生融合和分裂,融合的线粒体形成网络结构,使其分支长度减少,网络数量增加。线粒体独立骨架长度平均值无变化但中位数减小,说明除网络结构外的线粒体碎片程度增高。
图6
图6
老年线虫线粒体形态发生改变
Figure 6
Age-dependent mitochondrial morphology changes in C. elegans
3 线粒体活性生化测试
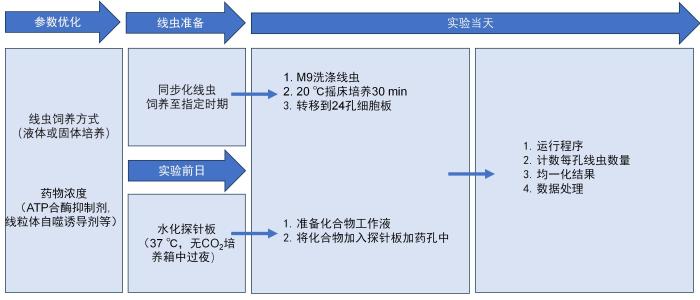
用Seahorse XFe24分析仪(购自美国Agilent Technologies公司)对线虫氧化呼吸能力进行测量。Seahorse可深入分析线粒体功能和代谢中的糖酵解,已被广泛运用于各种模型,从癌细胞、类器官到模式生物(如秀丽隐杆线虫)。其大致分析流程可归纳为:系统优化,实验前准备(水化探针板及样品制备),加药测试及数据处理(图7)。
图7
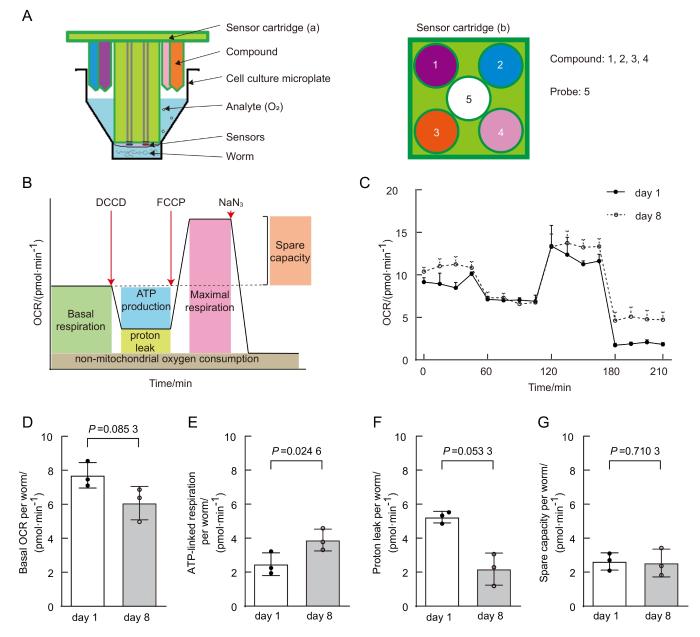
使用线虫作为样本时方法如下:用M9将培养皿上的线虫洗下,自然沉淀后弃上清并加入1 mL M9,重复清洗3次,于20 ℃摇床培养30 min。待线虫消耗完肠道细菌后,将线虫转移至专用24孔板,成年期第1天线虫每孔置20~40条,成年期第8天线虫每孔置50~80条,用M9溶液补足每孔液体总体积至525 μL。在加药孔中依次加入75 μL 的160 μmol/L N,N′-二环己基碳二亚胺(dicyclohexylcarbodiimide,DCCD) (购自美国Sigma-Aldrich公司,货号379115,终浓度20 μmol/L)、225 μmol/L羰基氰化物4-(三氟甲氧基)苯腙(carbonyl cyanide 4-(trifluoromethoxy) phenyl-hydrazone,FCCP)(购自美国Sigma-Aldrich公司,货号C2920,终浓度25 μmol/L)、100 mmol/L 叠氮钠(sodium azide,NaN₃,终浓度10 mmol/L)。设置仪器参数:混匀循环1 min → 平衡循环3 min→检测循环3 min。空白对照孔及每组样品至少设置4次技术重复。测量8次基础呼吸(basal respiration),然后依次添加DCCD、FCCP和NaN3。在每添加一种药物后,ATP相关呼吸(ATP-linked respiration)、最大呼吸和叠氮反应分别测量8次、8次和4次。将氧气消耗速率根据每个孔中的线虫数量进行归一化(图8A~B)。
图8
图8
年老线虫线粒体代谢发生改变(数据来自本实验室已发表文献[20])
Figure 8
Age-dependent mitochondrial function changes in C.elegans (data from published paper of our lab [20])
实验结果可以得到基础呼吸、ATP相关呼吸、呼吸潜力(spare respiratory capacity)和质子泄露(proton leak)。基础呼吸为基础耗氧率(oxygen consumption rate,OCR)与叠氮反应数据的差值[20],ATP相关呼吸为基础 OCR与DCCD抑制后数据的差值,呼吸潜力为基础OCR与FCCP解耦数据的差值,质子泄露为DCCD抑制与叠氮反应数据的差值。在每个阶段测量时的前几次数据会有波动,因此,选择4个连续稳定的点并将其平均值作为该阶段的数据来源(图8C)。使用GraphPad Prism(version 8.0)进行数据分析并统计作图。使用非配对t 检验对3次生物学重复的平均值进行统计分析,图中显示平均数和标准差。P<0.05表示差异具有统计学意义。
4 讨论和展望
随着人工智能的发展,越来越多软件和插件被开发以替代人工半定量方法,从而提高可重复性、扩充可分析参数。本文提供了实用性和普适性较强的代码块,以帮助科研工作者快速批量处理大规模图片数据。然而计算机基于二维像素点获得的结果可能忽略了更高维度的生物学现象,因此,研究者基于人类视觉判断的结果依旧值得重视。在交给软件完成任务之前,对所有原始数据进行全局性的观察,对于记录感兴趣点和未知现象尤为重要。此外,所有处理后图像均需单独保存,特别是局部选择框的信息要保留在图中,以便后续复证查核。
Mitochondria Analyzer插件适用于管状线粒体的统计(如肌肉线粒体)。MiNA插件的优势为可使用Ridge Detection代替Skeletonize生成骨架,使得其在处理网络状线粒体(如表皮线粒体)时有更多的算法拟合选择。两者区别在于:Skeletonize通过迭代删除外部像素来生成骨架,直到保留一个像素宽的结构,该方法必须有很强的信噪比才能将紧密相邻的线粒体完全分割,否则容易生成错误骨架;Ridge Detection则通过荧光强度本身来生成骨架,同时嵴检测也被纳入其中,该法生成的骨架更符合实际(图5C和5D)。值得注意的是,MiNA插件在计算面积时使用的是Auto Threshold算法,该算法不能很好地获取同一图像不同位置信号强弱差异较大图像的信息,而Mitochondria Analyzer插件可以很好地完成信息的提取。因此,后者仍在计算获取面积信息时被建议使用(图5C和5E)。
Seahorse实验在线虫中主要用于药物和突变体筛选。本文对已有的方法进行了总结,旨在提供一套标准方法供后续研究使用。Seahorse仪器原本为细胞研究开发,该仪器没有降温功能,因此,必须关闭加热器并严格控制室温。实验结果取决于环境温度,通常仪器在运行过程中温度会升高2 ~ 4 ℃。已有研究表明,该温差不会对线虫的OCR造成显著影响[19]。但根据以往经验,温度最好维持在24 ℃以下。除房间空调外,可在仪器周围铺满冰盒,并用电风扇吹风以帮助降温。
对于年老线虫的选择,首先尝试使用成虫期第10天的线虫,结果发现,无法得到相对平稳的数据。由于线虫从成年期第10天开始就会发生死亡,推测可能与该时期线虫对DCCD和FCCP的响应的个体差异过大有关。
线虫与大部分试验样品的另一个差异在于,线虫会在每次混合时随着探针的上下运动而漂浮。笔者尝试使用胰岛捕获微孔板(在标准微孔板基础上增加一层将样品固定于底部的网筛)后发现,基线明显平稳,但均一化后每条线虫的变化幅度减小。结果显示,网筛被染色,提示可能有化合物的吸附,因此,若要使用筛板需重新摸索药物浓度。
[引用本文]
宋梦娇, 沈义栋. 秀丽隐杆线虫的线粒体形态和功能研究方法及应用实例[J]. 实验动物与比较医学, 2025, 45(6): 726-737. DOI: 10.12300/j.issn.1674-5817.2025.119.
SONG M J, SHEN Y D. Approaches and application examples forstudying mitochondrial morphology and function inCaenorhabditis elegans[J]. Lab Anim Comp Med, 2025, 45(6): 726-737. DOI: 10.12300/j.issn.1674-5817.2025.119.
医学伦理声明
本研究涉及的动物实验均遵照中国实验动物相关法律法规条例要求进行。
Medical Ethics Statement
All animal experimental procedures were performed in accordance with the requirements of laws and regulations related to laboratory animals in China.
作者贡献
宋梦娇负责方法设计与实验操作、结果分析、论文构思及撰写,以及图表绘制;
沈义栋负责方案策划、项目管理、资助获取、论文修改及定稿。
利益冲突声明
所有作者均声明本文不存在利益冲突。
参考文献
MICOS and the mitochondrial inner membrane morphology–when things get out of shape
[J].
Mitochondrial morphology and dynamics in yeast and multicellular eukaryotes
[J].
Hallmarks of aging: an expanding universe
[J].
Mitochondrial DNA: distribution, mutations, and elimination
[J].
Guidelines for the use and interpretation of assays for monitoring autophagy (3rd edition)
[J].
The nematode Caenorhabditis elegans as a model for aging research
[J].
Does perturbation in the mitochondrial protein folding pave the way for neurodegeneration diseases?
[J].
High-throughput behavioral screen in C. elegans reveals Parkinson's disease drug candidates
[J].
A small-molecule screen identifies novel aging modulators by targeting 5-HT/DA signaling pathway
[J].
Caenorhabditis elegans as an emerging high throughput chronotherapeutic drug screening platform for human neurodegenerative disorders
[J].
Extracellular flux assay (Seahorse assay): Diverse applications in metabolic research across biological disciplines
[J].
Maintenance of C. elegans
[J].
Axin-mediated regulation of lifespan and muscle health in C. elegans requires AMPK-FOXO signaling
[J].
Age-dependent changes in mitochondrial morphology and volume are not predictors of lifespan
[J].
Peroxiredoxin 2 regulates DAF-16/FOXO mediated mitochondrial remodelling in response to exercise that is disrupted in ageing
[J].
A pipeline for multidimensional confocal analysis of mitochondrial morphology, function, and dynamics in pancreatic β-cells
[J].
A simple ImageJ macro tool for analyzing mitochondrial network morphology in mammalian cell culture
[J].
Measurement of respiration rate in live Caenorhabditis elegans
[J].
Oxygen consumption measurements in Caenorhabditis elegans using the seahorse XF24
[J].
A moderate static magnetic field promotes C. elegans longevity through cytochrome P450s
[J].
Rates of behavior and aging specified by mitochondrial function during development
[J].
Mitochondrial and metabolic dysfunction in ageing and age-related diseases
[J].
The mitochondrial basis of aging
[J].
Systemic effects of mitochondrial stress
[J].
Age-dependent changes in mitochondrial morphology and volume are not predictors of lifespan
[J].
Age-dependent changes and biomarkers of aging in Caenorhabditis elegans
[J].
Mitochondrial bioenergetic changes during development as an indicator of C. elegans health-span
[J].
A hyperfused mitochondrial state achieved at G1–S regulates cyclin E buildup and entry into S phase
[J].
Loss of PINK1 function promotes mitophagy through effects on oxidative stress and mitochondrial fission
[J].