建立大鼠慢性肾功能不全血管钙化模型是研究CKD的常用手段。目前建立大鼠慢性肾功能不全血管钙化模型的手段较多[3-8],其中肾切除联合维生素D摄入是较为经典的慢性肾功能不全主动脉钙化模型建立方法。研究发现,啮齿类动物经肾切除加上高磷饮食或高维生素D摄入后能获得较为理想的血管钙化表型,并且肾切除相较于药物诱导肾脏衰竭来说个体差异更小[7]。另有学者研究发现,肾切除术后加用大剂量骨化三醇(一种活化的维生素D)能较好地诱导主动脉钙化[9],并且骨化三醇能在一定程度上改善慢性肾功能不全引起的甲状旁腺亢进症状,能提高建模期间大鼠的存活率,提示肾切除联合骨化三醇摄入是较为理想的大鼠慢性肾功能不全血管钙化模型建立方法。然而,以上方法需要对大鼠进行手术,创伤较大,甚至严重影响大鼠生存,因此需要选择合理的手术方式将大鼠的手术创伤降至最小。目前,构建该模型的手术方式多种多样,有不同的手术入路、不同的肾切除顺序[10-13],并且本课题组在预实验中发现不同手术方式对大鼠生存有较显著的影响。基于此,本研究先将36只SD大鼠分为不同肾脏切除术式的4组进行探索性实验,评估优化手术方式后再选取24只SD大鼠进行慢性肾功能不全建模和血管钙化诱导,然后验证模型动物的主动脉钙化效果,旨在探索大鼠CKD血管钙化模型的最优手术方案。
1 材料与方法
1.1 实验动物
SPF级SD雄性大鼠60只,8周龄,体重(210 ± 10.8)g, 购自广西医科大学动物实验中心 [SCXK(桂)2020-0003],质量合格证号为2024235。动物饲养于广西医科大学SPF级动物实验室[SYXK(桂)2020-0004],环境温度为(23 ± 3)℃,相对湿度为(50 ± 5)%,人工照明且控制12 h明暗交替;动物可以全天自由饮水,全程常规进食。所有实验操作遵循动物福利伦理要求,并获得广西医科大学实验动物伦理委员会审查批准(批号202312005);术后允许大鼠自由活动,自由饮食饮水。
1.2 实验设备及试剂
超低温冰箱(型号MDF-782VE)购自冰山松洋生物科技(大连)有限公司;倒置显微镜(型号CKX53)购自日本Olympus公司;全波长酶标仪(型号Multiskan SkyHigh)购自美国Thermo Fisher Scientific公司;实时荧光定量PCR仪(型号qTOWER3G)购自德国耶拿分析仪器股份公司(AnalytikJena);RWD动物气体麻醉机购自深圳瑞沃德生命科技股份有限公司。
血清磷浓度检测试剂盒(批号BC1655)、尿素氮(尿素)含量检测试剂盒(批号BC1535)、钙检测试剂盒(邻甲酚酞络合酮比色法,批号BC8333)和骨化三醇(批号SC8910)均购自北京索莱宝科技有限公司;肌酐(creatinine,CRE)测定试剂盒(批号C011-2-1)购自南京建成生物工程研究所;2%茜素红S染色液(批号G1038-100 mL)、von Kossa染色液(批号G1043-1)均购自武汉赛维尔生物(Servicebio)科技有限公司;HE染色液(批号G1005-500 mL)购自武汉赛维尔生物(Servicebio)科技有限公司;二甲基亚砜(dimethyl sulfoxide,DMSO)(批号D6370)购自北京博奥拓达(Biotopped)科技有限公司;异氟烷(批号2025021501)购自深圳市瑞沃德生命科技股份有限公司;卡洛芬(批号M81424-1G)购自上海迈瑞尔生化科技有限公司;细胞/组织总RNA提取试剂盒(批号RC11201)购自南京诺唯赞(Vazyme)生物科技股份有限公司;逆转录试剂盒(批号RR092A)和快速荧光定量PCR试剂盒(批号CN830A)均购自日本TaKaRa公司。
1.3 大鼠肾功能不全模型构建术式优化
1.3.1 实验分组
为探索不同手术方式的效果,将36只SD大鼠分为4个实验组:A组12只,从腹腔入路先切2/3左肾后,二期切除右全肾;B组6只,从腹腔入路2/3左肾及右全肾同时切除;C组6只,背入路先切右全肾后,二期切除2/3左肾;D组12只,背入路先切除2/3左肾,再二期切除右全肾。
1.3.2 腹腔入路肾脏切除术
在RWD动物气体麻醉机的麻醉诱导盒中使用4%异氟烷/氧气对大鼠进行麻醉诱导,再用1.5%异氟烷/氧气混合气体维持麻醉,腹部备皮并用75%乙醇溶液消毒,用组织剪剪开腹中线皮肤及腹白线,打开腹腔。2/3左肾切除:以1号外科缝线缝合腹壁作为牵引提拉腹壁,用棉签将小肠及降结肠向右侧拨开,并置入棉球挡开肠管使暴露左侧肾脏。暴露左肾下极,沿包膜钝性分离左肾下极,沿包膜继续向上钝性分离左肾上极,将左肾游离。以无损伤镊子轻持左肾上极,高温电凝刀切割左肾皮质,标记切割范围,以组织剪沿预切线剪除肾下极,以电凝刀灼烧止血[14];用同样方法处理左肾上极。使用同样的方法暴露右肾,以无损伤镊子轻持右侧肾脏,向上外轻轻提起暴露右侧肾蒂,以止血钳夹闭肾蒂血管组织,用组织剪剪断肾蒂,完整切除右肾。以1号外科缝合线结扎右侧肾蒂,确定无出血后,取出棉球恢复肠道位置,连续缝合腹壁,皮下注射少量1%利多卡因(<0.1 mL)用于术后止痛,随后将大鼠置于恒温电热毯上复苏。如进行分期肾切除术,则在2/3左肾切除术后1周,再按上述操作切除右侧全肾。
1.3.3 背入路肾脏切除术
按照1.3.2节方法对大鼠进行麻醉,背部备皮并用75%乙醇溶液消毒,术前可触摸肾脏大概位置,取第13肋脊点下方0.5 cm偏外侧0.5 cm做1.5~2 cm切口(位于竖脊肌外侧)。2/3左肾切除:剪开皮肤浅筋膜,暴露背阔肌,透过背阔肌可见下方黄色的肾周脂肪即为正确位置,剪开背阔肌暴露后腹腔;用左手食指于腹腔触摸肾脏并将其挤出切口,以镊子提起左侧肾下极脂肪筋膜,暴露筋膜与肾包膜解剖间隙,以中弯钳或棉签沿间隙钝性分离肾筋膜,完全暴露肾脏及肾蒂结构;以无损伤镊子轻持左肾下极,用高温电凝刀切割左侧肾皮质标记切割范围,组织剪沿预切线剪除左肾下极,以电凝刀灼烧止血;以同样方法处理左肾上极,确定无出血,肾蒂无扭曲后将左侧肾脏还纳后腹腔;连续缝合背阔肌,间断缝合皮肤,皮下注射少量(<0.1 mL)1%利多卡因用于术后止痛。1周后行右侧肾全切术:用相同的方法暴露右肾,由于右肾不方便触及,可先找到脂肪筋膜,反复提起脂肪筋膜可见到肾下极,将右肾挤出切口外侧;以镊子提起肾下极脂肪筋膜,暴露筋膜与肾包膜解剖间隙,以中弯钳或棉签沿间隙钝性分离肾筋膜,完全暴露右侧肾脏及右侧肾蒂结构;以无损伤镊子轻持右侧肾脏,以1号外科缝合线尽量远离肾门将肾蒂结扎,以剪刀剪断肾蒂将右肾完整取出;确定结扎牢固无出血后,连续缝合背阔肌,间断缝合皮肤。若先切除右侧肾则将右肾切除的顺序与左肾部分切除顺序调换,手术方式不变。皮下注射1%利多卡因(<0.1 mL),随后将大鼠置于恒温电热毯上复苏。
1.3.4 手术后实验大鼠的生存情况分析
术后大鼠不予束缚,可自由活动,正常摄食摄水。术后每日按5 mg/kg剂量皮下注射卡洛芬溶液(使用无水乙醇溶解卡洛芬粉剂配制成10 mg/mL保存液,再使用生理盐水稀释成2.5 mg/mL溶液)一次,连续注射3 d进行术后止痛。记录各组大鼠术后生存状况,以各组大鼠存活数量及实验时间为变量,分析同一时间内各组大鼠存活数量,使用概率乘积法计算不同时间点的生存概率,绘制Kaplan-Meier曲线进行生存分析,对肾切除术后60 d内各组大鼠的累积生存概率进行Log-Rank检验。
1.4 肾功能不全主动脉钙化模型构建
1.4.1 实验分组及钙化诱导
1.4.2 建模后动物生存状态观察及安死术后取材
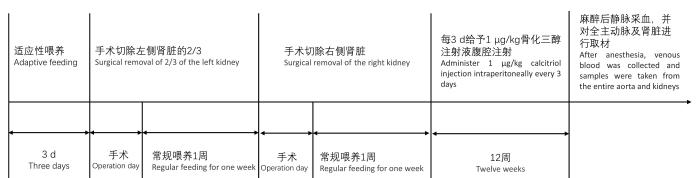
骨化三醇诱导主动脉钙化期间观察各组大鼠的存活情况,包括精神状态、摄食量、毛发、体重等。3个月即12周后,使用2%异氟烷/氧气混合气体麻醉各组大鼠,行下腔静脉采血用于血清生化检测,血液样本采集完成后继续放血安乐死动物。然后进行剖检,肉眼观察大鼠残余肾脏形态,取材并制成肾冠状切面的石蜡切片后进行HE染色,同时进行肾小球计数。另外取各组大鼠的全主动脉,以肾动脉为界分别采集胸主动脉及腹主动脉两部分,每部分取1/2的主动脉组织以4%多聚甲醛溶液固定,用于免疫组织化学染色,包括茜素红S染色、von Kossa染色;剩下的主动脉组织经液氮快速冷冻,48 h后置于-80 ℃冰箱冻存,用于实时荧光定量PCR检测。大鼠尸体包装后贮存在-20 ℃的冰柜中,待专业公司进行无害化处理。慢性肾脏病主动脉钙化模型构建实验流程如图1所示。
图1
图1
SD大鼠慢性肾脏病主动脉钙化建模及评价实验流程图
Figure1
Flowchart of the experimental process for modeling and evaluating aortic calcification in SD rats with chronic kidney disease
1.5 模型大鼠的血清生化指标测定
采用下腔静脉采血法抽取大鼠全血约2.5 mL置入干燥管或促凝管,3 000 r/min离心15 min,取上清液即为大鼠血清。分别使用血磷浓度检测试剂盒、尿素氮(尿素)含量检测试剂盒、钙检测试剂盒(邻甲酚酞络合酮比色法)和CRE测定试剂盒,按说明书步骤测定所有实验大鼠的血清磷和钙离子浓度、血清尿素氮和肌酐含量。
1.6 大鼠肾脏HE染色观察
将大鼠肾脏组织沿冠状面切开固定于4%多聚甲醛溶液中,常规石蜡包埋,制备厚度为5 μm的肾脏冠状面组织切片。使用二甲苯浸泡切片,脱蜡后分别使用无水乙醇、95%和75%乙醇溶液进行脱水,使用纯水和去离子水洗涤各2次,每次5 min。随后加入苏木精染液染色5 min,使用1%的盐酸乙醇溶液去除多余染料,并用氨水处理10 s使部分变蓝,再通过流水冲洗30 s,去离子水反复洗10 min。加入伊红染液染色2~3 min,纯水洗3 次后,将组织切片依次置于75%、95%以及无水乙醇溶液中浸泡各3 min,二甲苯溶液中浸泡2次各5 min。于切片上滴加中性树脂,盖上盖玻片进行封固。光学显微镜下观察肾脏结构,并用Image View软件辅助进行肾小球计数。
1.7 大鼠主动脉组织化学染色观察
1.7.1 茜素红S染色
将大鼠主动脉组织固定于4%多聚甲醛溶液中,常规石蜡包埋,制备厚度为5 μm的组织切片。使用二甲苯浸泡切片脱蜡后,分别使用无水乙醇、95%和75%乙醇溶液进行脱水,然后用2%茜素红S染色液浸染20 min。再用95%乙醇溶液和无水乙醇各脱水2次,二甲苯透明,最后用中性树脂封固。在光学显微镜下观察主动脉中膜染色情况。
1.7.2 von Kossa染色
1.7.3 染色结果的半定量数据分析
主动脉组织切片染色图像使用Windows11系统的Microsoft照片2025处理软件智能去除背景后,使用Image J软件进行图片处理:将图片Type设置成8 bit灰阶,设置Enhance Contrast为0.3%。对于von Kossa染色切片,设置Threshold为0~168可得到满意的染色面积,0~251可得到主动脉总面积;对于茜素红S染色,Threshold设置为0~163可得到满意的染色面积,0~251可得到主动脉总面积。以主动脉染色面积占主动脉总面积的百分比评估主动脉钙化程度。
1.8 大鼠主动脉组织中相关基因的荧光定量PCR检测
采用实时荧光定量PCR法测定主动脉组织中平滑肌肌动蛋白相关蛋白α(smooth muscle actin-associated protein α,Sm22)以及骨组织相关的骨桥蛋白(osteopontin,OPN)、Runt相关转录因子2(Runt-related transcription factor 2,Runx2)表达量,以此来反映模型建立后血管平滑肌成骨样表型转变的情况[4]。采用TRIzol法提取主动脉组织中总RNA,酶标仪测定RNA浓度后于-80 ℃冰箱保存。在250 μL离心管中加入RNA 1 000 μg,用 DEPC水定容至14 μL,后加入8×DNA酶2 μL,置入PCR仪进行反应,反应条件为42 ℃ 2 min,4 ℃保存,以清除DNA杂质。反应完成的离心管中加入5×逆转录酶4 μL,置入PCR仪进行反应,反应条件为37 ℃ 10 min,85 ℃ 5 s,4 ℃保存,得到产物为cDNA,可在-80 ℃保存或直接用于荧光定量PCR。实时荧光定量PCR体系包括PCR正反向引物各0.8 μL、SYBR Green Master Mix PCR反应试剂10 μL、cDNA模板2 μL、无菌无酶水6.4 μL;其中PCR引物序列信息见表1,由TaKaRa公司设计并合成。PCR反应流程:95 ℃预变性30 s;95 ℃变性5 s,60 ℃退火延伸10 s,共40个循环。PCR扩增完成后计算2-△△Ct值,以反映目的基因的表达水平。
表1 PCR引物序列信息
Table 1
目标基因名称 Target gene name | NCBI基因序列号 NCBI reference sequence | 引物序列信息 Primer sequence information | 扩增片段大小/bp Amplification fragment size/bp |
|---|---|---|---|
| Sm22 (Tagln) | NC-086026.1 | F:5’-CAGATGGAACAGGTGGCTCAA-3’ | 161 |
| R:5’-GCCCAAAGCCATTACAGTCCTC-3’ | |||
| OPN (Spp1) | NC-086032.1 | F:5’-GCCGAGGTGATAGCTTGGCTTA-3’ | 145 |
| R:5’-TTGATAGCCTCATCGGACTCCTG-3’ | |||
| Runx2 | NC-086027.1 | F:5’-GGATGCCTTAGTGCCCAAATG-3’ | 120 |
| R:5’-CACCCTGTGAGGTGGCTGAA-3’ | |||
| β-actin | NC-086030.1 | F:5’-CACCCGCGAGTACAACCTTC-3’ | 207 |
| R:5’-CCCATACCCACCATCACACC-3’ |
1.9 统计学分析
采用SPSS 20.0软件对实验结果数据进行统计学分析。计量资料先进行Shapiro-Wilk正态性检验,符合时数据用平均数 ± 标准差表示,两组间比较采用独立样本 t 检验,多组间比较采用秩和检验。生存分析采用Kaplan-Meier方法进行统计,使用Log-Rank检验计算P值,使用R软件4.3.1版本“survival”包进行生存分析,使用“survminer”包进行生存分析可视化绘制Kaplan-Meier曲线。P<0.05提示差异有统计学意义。
2 结果
2.1 不同手术方式构建的慢性肾功能不全模型大鼠存活情况
采用不同手术方式建立的慢性肾功能不全模型大鼠的术后60 d累积生存概率有明显差异(图2,P<0.05)。其中腹腔入路2/3左肾及右全肾同时切除的B组及背入路先切右全肾后二期2/3左肾切除的C组大鼠在术后10 d内出现大量死亡(死亡率>50%),背入路先行2/3左肾切除再行右全肾切除的D组大鼠相较其他组的术后60 d累积生存概率最高(P<0.05),因此后续采用该术式进行CKD建模。
图2
图2
不同手术方式构建的慢性肾功能不全模型组大鼠的Kaplan-Meier生存曲线分析
Figure 2
Kaplan-Meier survival curve analysis of rats in chronic renal insufficiency model groups constructed using different surgical methods
2.2 CKD主动脉钙化建模大鼠的效果评估
2.2.1 术后大鼠生存状态及其肾脏、主动脉观测
用优化的肾脏切除术式联合高剂量骨化三醇注射法建立CKD主动脉钙化模型期间,12只实验组大鼠中分别于右肾切除后第7、9、40天各死亡1只,总共死亡3只;而12只对照组大鼠全部存活。实验组大鼠出现精神萎靡、摄食量减少、毛发稀疏,以及消瘦等表现。对实验组所有存活大鼠行安乐死后剖检,结果显示实验组大鼠残余肾脏苍白水肿,主动脉呈现僵硬改变,缺乏弹性,动脉壁可触及环状钙化沉积。
2.2.2 血生化检测结果
分别取9只实验组大鼠及12只对照组大鼠的血清样本检测血生化指标,结果数值见表2。统计分析结果显示,实验组大鼠的血清钙离子浓度显著低于对照组(P<0.05),而血清磷离子浓度以及肌酐和尿素氮的含量均显著高于对照组(P<0.05)。
表2
实验组与对照组大鼠血清生化指标对比 (
Table 2
血生化指标 Biochemistry index | 实验组(n=9) Experimental group | 对照组(n=12) Control group | t值 t value | P值 P value |
|---|---|---|---|---|
血清钙 c/(mmol·L-1) Serum calcium ions | 1.876±0.036 | 1.929±0.042 | 3.431 | 0.004 |
血清磷c/(mmol·L-1) Serum phosphate ions | 2.059±0.333 | 1.580±0.271 | 3.046 | 0.014 |
血清肌酐c/(μmol·L-1) Serum creatinine | 119.960±35.640 | 21.164±8.076 | 8.984 | <0.000 1 |
血清尿素氮c/(mmol·L-1) Serum urea nitrogen | 57.991±8.745 | 22.609±8.058 | 6.895 | <0.000 1 |
2.2.3 肾脏HE染色结果
图3
图3
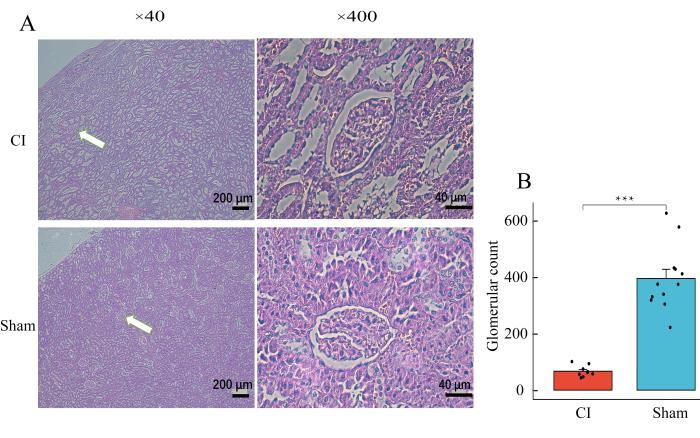
实验组与对照组大鼠的肾脏HE染色观察
Figure 3
HE staining observation of kidneys from rats in the experimental and control groups
2.2.4 主动脉钙化染色结果
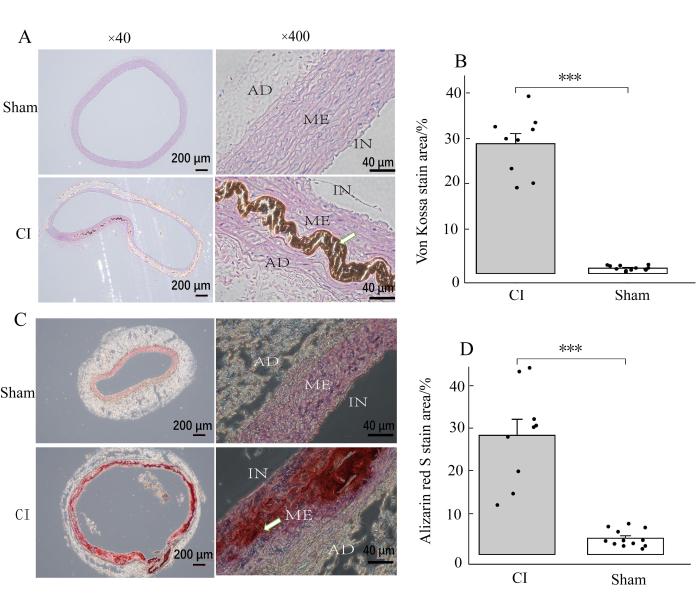
分别取9只实验组大鼠及12只对照组大鼠的胸腹主动脉制作石蜡切片,行茜素红S染色及von Kossa染色(图4)。结果可见,实验组主动脉中膜深染,有明显的银盐及茜素红S染液沉积,可见部分细胞坏死,符合慢性肾脏疾病动脉中膜钙化的特点;对照组可见主动脉形态完整,未见染色沉积。使用Image J软件对染色面积进行相对定量分析(即每例大鼠取胸主动脉及腹主动脉染色面积占比的平均值进行对照分析),实验组的茜素红S及von Kossa染色面积占比(染色面积与该切面主动脉总面积之比)明显大于对照组(P<0.05),提示实验组的主动脉钙化明显。
图4
图4
实验组和对照组大鼠的主动脉von Kossa染色及茜素红S染色观察
Figure 4
Observation of von Kossa and Alizarin red S staining in the aorta of rats from the experimental and control groups
2.2.5 主动脉组织细胞PCR结果
图5
图5
实时荧光定量PCR检测实验组和对照组大鼠的主动脉组织细胞中OPN、Runx2及Sm22基因表达
Figure 5
Real-time fluorescence quantitative PCR detection of OPN, Runx2, and Sm22 gene expression in aortic tissue of rats from the experimental and control groups
3 讨论
事实上已有较多学者对CDK血管钙化模型进行过评估,但大多是论证不同手术所带来的效果差异[7,20-22],鲜少针对手术的实施细节进行论证,也少有人对建模失败的原因进行分析。本研究对手术建模的操作细节进行了比较分析,发现不同的手术方案带来的建模效果有可能会大不相同。首先,本研究对手术入路进行对比分析。经生存分析发现,腹腔入路肾切除术较背入路手术的大鼠生存状况要差(图2)。这可能要归因于经腹入路暴露肾脏时对腹腔肠管扰动较大,易导致术后肠粘连发生;而且大鼠腹腔大网膜组织极不发达,炎症在腹腔易于扩散,从而影响模型大鼠的生存状况;而背入路肾切除术在定位准确的情况下仅需打开一层背阔肌即可暴露肾脏,无其他组织阻挡,操作相对简单,对腹腔脏器几乎无干扰,大鼠生存状况较好。其次,本研究对肾脏切除时机也进行了对比分析。目前大部分学者采用的方式为分期手术[4-7,20-23],但也有学者提出一期手术的可能性[20]。本研究结果显示,先行肾脏部分切除术,间隔1周的代偿缓冲时间后再行另侧全肾切除术的效果更好。同时对双肾进行手术,或先切除单侧全肾均会导致实验大鼠短期内死亡,其原因可能是短时间切除过多肾脏组织,会导致残余肾功能没有足够时间代偿,从而导致急性肾衰竭。
骨化三醇作为活性维生素D,具有调节钙磷平衡的作用,是治疗CDK患者的常用药物;但高剂量的骨化三醇会扰乱体内钙磷平衡,加速血管钙化。使用骨化三醇作为钙化诱导剂可减少慢性肾功能不全大鼠磷酸盐异常造成的机体损伤[22],亦符合临床上CDK患者血管钙化的病理生理改变,但缺点是诱导时间较长。而高嘌呤饮食诱导的大鼠CDK主动脉钙化模型虽然建模时间短[16],但易导致血管壁损伤[24],从而影响后续实验结果的准确性。有学者认为在完成手术后使用高磷高钙饮食可以增强钙化效果[22]。但本课题组在前期实验中发现,高磷高钙饮食的大鼠在进食2周后出现食欲减退、懒于进食的情况,这可能与高磷高钙饮食影响大鼠味觉、磷酸盐负荷过高加速细胞衰老有关[25],增加了实验大鼠的痛苦。综合来说,单纯使用高剂量骨化三醇作为慢性肾功能不全术后血管钙化诱导剂较为理想。
需要指出,由于客观条件限制,本研究中各组大鼠数量较少;并且前期实验发现,B、C组两种手术方式建模的大鼠死亡率较高,为了遵循动物福利原则,术式探索实验时减少了这两组大鼠的数量(分别为6只)。因此,4组实验大鼠的数量不同,得出的结果可能会具有一定的偏倚。此外,腹腔注射高剂量骨化三醇的给药方法也可能导致实验大鼠的肠粘连、肠梗阻发生,一定程度上影响模型成功率。笔者认为,在实验过程中尽可能减少腹腔刺激(如使用呼吸麻醉、药物灌胃等方式)是提高实验动物存活率的关键。
综上所述,采用背入路先切除2/3左肾再进行右侧全肾切除联合高剂量骨化三醇摄入方法建立的SD大鼠CDK主动脉钙化模型能提高模型成功率及动物存活率。
[引用本文]
潘颐聪, 蒋汶洪, 胡明, 等. 慢性肾脏病大鼠主动脉钙化模型的术式优化及效果评价[J]. 实验动物与比较医学, 2025, 45(3): 279-289. DOI:10.12300/j.issn.1674-5817.2024.128.
PAN Y C, JIANG W H, HU M, et al. Optimization of surgicalprocedure and efficacy evaluation of aortic calcification model inrats with chronic kidney disease [J]. Lab Anim Comp Med, 2025, 45(3): 279-289. DOI: 10.12300/j.issn.1674-5817.2024.128.
医学伦理声明
本研究涉及的所有动物实验均已通过广西医科大学实验动物伦理委员会审查批准(批件号:202312005)。所有实验过程均遵照中国实验动物相关法律法规条例要求进行。
Medical Ethics Statement
All animal experiments involved in this study have been approved by the Experimental Animal Ethics Committee of Guangxi Medical University (Approval Number: 202312005). All experimental processes were conducted in accordance with relevant laws, regulations, and rules on experimental animals in China.
作者贡献声明
潘颐聪负责实验操作和论文撰写及修改;
蒋汶洪为项目负责人,负责实验构思,辅助动物实验操作;
胡明、覃晓负责动物实验技术指导和质量监督。
利益冲突声明
所有作者均声明本文不存在利益冲突。
参考文献
The roles of collagen in chronic kidney disease and vascular calcification
[J].
2019年«中国慢性肾脏病矿物质和骨异常诊治指南»解读
[J].
Interpretation of Chinese Guideline for Diagnosis and Treatment of Chronic Kidney Disease-Mineral and Bone Disorder (2019 version)
[J].
Repression of the antiporter SLC7A11/glutathione/glutathione peroxidase 4 axis drives ferroptosis of vascular smooth muscle cells to facilitate vascular calcification
[J].
Shox2促进血管钙化的作用及机制研究
[D].
The role and mechanism of Shox2 in promoting vascular calcification
[D].
五羟色胺对慢性肾脏病大鼠血管钙化的作用及其机制研究
[D].
Study on the effect and mechanism of serotonin on vascular calcification in rats with chronic kidney disease
[D].
二氢杨梅素抑制慢性肾脏病大鼠血管钙化及其机制研究
[D].
Study on the inhibition of vascular calcification and its mechanism by dihydromyricetin in rats with chronic kidney disease
[D].
Vascular calcification in animal models of CKD: a review
[J].
Bone marrow mesenchymal stem cell-derived exosomal microRNA-381-3p alleviates vascular calcification in chronic kidney disease by targeting NFAT5
[J].
不同剂量骨化三醇对慢性肾衰竭大鼠主动脉钙化的影响
[D].
Effects of different doses of calcitriol on aortic calcification in rats with chronic renal failure
[D].
ENPP1 ameliorates vascular calcification via inhibiting the osteogenic transformation of VSMCs and generating PPi
[J].
Curcumin attenuates vascular calcification via the exosomal miR-92b-3p/KLF4 axis
[J].
Spermidine inhibits vascular calcification in chronic kidney disease through modulation of SIRT1 signaling pathway
[J].
Trimethylamine-N-oxide promotes vascular calcification through activation of NLRP3 (nucleotide-binding domain, leucine-rich-containing family, pyrin domain-containing-3) inflammasome and NF-κB (nuclear factor κB) signals
[J].
Correction of vascular calcification and hyperphosphatemia in CKD rats treated with ASARM peptide
[J].
PDK4 promotes vascular calcification by interfering with autophagic activity and metabolic reprogramming
[J].
Upacicalcet, a positive allosteric modulator of the calcium-sensing receptor, prevents vascular calcification and bone disorder in a rat adenine-induced secondary hyperparathyroidism model
[J].
CDC42 promotes vascular calcification in chronic kidney disease
[J].
Intermedin1-53 attenuates vascular calcification in rats with chronic kidney disease by upregulation of α-Klotho
[J].
Vascular calcification-new insights into its mechanism
[J].
急性肾损伤动物模型构建方法与研究现状
[J].
Research approaches and status of animal models for acute kidney injury
[J].
急性肾损伤动物模型及体外模型研究进展
[J].
Advances in animal models and in vitro models of acute kidney injury
[J].
Research models for studying vascular calcification
[J].
Kidney disease models: tools to identify mechanisms and potential therapeutic targets
[J].
Rodent models of AKI-CKD transition
[J].
Vascular calcification in rodent models-keeping track with an extented method assortment
[J].