树鼩(Tupaia belangeri,tree shrew)是近年来新兴的实验动物,相较于灵长目猴科动物而言具有动物体型小、繁殖周期短、饲养简单且价格便宜等优点。与小鼠等啮齿类实验动物相比,树鼩与灵长类动物具有更近的亲缘关系,在生理代谢、免疫、遗传等诸多方面与人类相似性较高[1-2]。因此,利用树鼩研究一些人类相关疾病基因,能更真实地反映人类多种疾病的发生、发展和转归。但是相对于其他成熟的实验动物(如小鼠、大鼠、家兔)来说,树鼩的基础生物学数据和特异性检测试剂较为缺乏[3]。在功能学研究中,单克隆抗体作为发展最为迅速的生物技术衍生分子工具之一[4],在生物医学研究领域当中展现出较高的研究价值[5-7],在疾病的诊断、预防和治疗中也发挥着重要的作用[8-9]。通过制备高纯度、高特异性的单克隆抗体对细胞或组织中某一蛋白的表达进行检测,是一种较为快速且灵敏的检测方法。目前已报道的有多种树鼩多克隆抗体,包括瑶山亚种树鼩干扰素β、干扰素γ[10]、干扰素刺激基因15[11]、树鼩IgG[12]等多克隆抗体,但对于树鼩单克隆抗体的报道较少。
Vasorin(VASN)是一种由VASN基因编码的Ⅰ型跨膜糖蛋白,最初发现它是一种转化生长因子抑制剂,主要在新生血管内膜中发挥作用[13-14]。VASN在多种肿瘤中呈高表达,是一种潜在的生物标志物[15-16]。例如,VASN在肺癌组织中表达上调,可通过抑制自噬介导的细胞凋亡促进支气管上皮细胞的转化[17]。但是关于VASN异常表达的原因、促进肿瘤恶性发生发展的机制以及VASN的生理功能尚不清楚。本课题组在前期研究中发现,VASN是维持肝细胞自噬上游肝糖原代谢稳态的必需因子[18],在肝细胞癌信号传导及转录激活蛋白3(signal transducer and activator of transcription 3,STAT3)信号通路的激活中起着至关重要的作用[19],同时也有许多研究发现VASN的异常表达与多种疾病的发生发展有关[20-21]。为更好地利用树鼩开展与VASN相关的多种疾病模型研究,本研究制备了树鼩VASN特异性单克隆抗体,并评估了其在体外模型中的反应性,为深入研究树鼩疾病模型中VASN的生物学功能奠定基础。
1 材料与方法
1.1 实验动物
SPF级雌性BALB/c小鼠,共11只,6周龄,体重约为26 g,购自广东维通利华实验动物技术有限公司[SCXK(粤)2020-0063],饲养于广西医科大学实验动物中心[SYXK(桂)2020-0004];在饲养阶段,小鼠饮水自由,喂食标准饲料,且昼夜循环照明,相对湿度50%~60%,温度控制在22~25 ℃;小鼠实验经广西医科大学实验动物福利与伦理委员会批准后实施,动物免疫与腹水制备的实验审批号分别为202304007和202307013。1只普通级成年雄性树鼩购自昆明医科大学实验动物中心[SCXK(滇)K2020-0004],体重为120 g,饲养于广西医科大学实验动物中心[SYXK(桂)2020-0004],动物伦理由广西医科大学实验动物福利与伦理委员会审查(审批号为202212016)。所有动物实验操作均遵循实验动物伦理福利原则。
1.2 细胞与菌株
SP2/0骨髓瘤细胞购自中国科学院细胞库,树鼩永生化成纤维细胞由广西医科大学实验动物中心惠赠,DH5ɑ感受态细胞购于昂羽生物技术股份有限公司,大肠杆菌BL21(DE3)和pET-30a质粒由本实验室保存。
1.3 主要试剂与仪器
引物由南宁捷尼斯生物科技有限公司合成。RNA提取试剂盒(批号AK1701)、反转录试剂盒(批号AL61877A)均购自日本TaKaRa公司;限制性核酸内切酶BamHⅠ(批号0000245201)和SalⅠ(批号000 0202285)均购自美国Promega公司;T4连接酶(批号10218)购自北京全式金生物技术股份有限公司;2×Phanta Max Master Mix(批号7E690H2)购自南京诺唯赞生物科技股份有限公司;辣根过氧化物酶(horseradish peroxidase,HRP)山羊抗小鼠IgG(批号BST18L01A20A51)购自武汉博士德生物工程有限公司;磷酸盐缓冲溶液(phosphate buffered saline,PBS)(批号20231104)、异丙基-β-D-硫代半乳糖苷(isopropyl β-D- thiogalactoside,IPTG)(批号1213I 054)、石蜡油(批号5540319001)、琼脂糖凝胶亲和层析介质rProtein G(批号816J011)、牛血清白蛋白(bovine serum albumin,BSA)(批号128P055)、RIPA组织/细胞裂解液(批号240010008)购自北京索莱宝科技有限公司;硫酸卡那霉素(批号21283327)、细胞爬片(批号BS-14-RC)、苏木精(批号22248956)购自北京兰杰柯科技有限公司;LB肉汤(批号1804121)购自北京陆桥技术股份有限公司;质粒DNA提取试剂盒(批号D6950010000J26W161)购自美国Omega公司;KCI(批号20200923)购自天津市大茂化学试剂厂;弗式完全/不完全佐剂(批号SLCJ8308)、50×胸腺嘧啶核苷(hypoxanthine-thymidine,HT)(批号SLCN1323)、50×黄嘌呤和胸腺嘧啶核苷混合剂(hypoxanthine-aminopterin-thymidine,HAT)(批号SLCK2064)、50%聚乙二醇(批号RNBG7124)均购自美国Sigma公司;激活剂(批号1000119999)购自加拿大STEMCELL Technologies公司;脱脂奶粉(批号EZ66608B40)购自德国BioFroxx公司;DNA纯化试剂盒(批号111722230508)、BCA蛋白浓度测定试剂盒(批号A2242240430)购自上海碧云天生物技术股份有限公司;316L不锈钢研磨珠(批号SS-2.0)购自杰灵仪器制造(天津)有限公司;甲醇(批号2018052 101)购自成都市科隆化学品有限公司;DAB显色试剂盒(批号240010216)、免疫组织化学通用二步法试剂盒(批号2425A0203)均购自北京中杉金桥生物技术有限公司。猪视黄醇结合蛋白4(retinol-binding protein 4,RBP4)重组蛋白、人VASN-富含亮氨酸重复序列(leucine rich repeat,LRR)重组蛋白为本课题组前期生产的两个重组蛋白,于-80℃冰箱长期保存。
梯度PCR仪(型号Simpliamp)、荧光定量PCR仪(型号QuantStudio 7 Flex)、蛋白成像分析系统(型号iBright 1500)、高速冷冻小型离心机(型号Fresco21)、连续光谱扫描式酶标仪(型号Multiskan GO)、超微量紫外分光光度计(型号NanoDrop One)均购自美国Thermo Fisher Scientific公司;石蜡包埋与切片机(型号RM2235)和生物显微镜(型号BX53)均购自德国Leica公司;台式冷冻离心机(型号Centrifuge 5430R)购自德国Eppendorf公司;超声波细胞粉碎机(型号SCIENTZ-ⅡD)购自宁波新芝公司;二层振荡恒温培养箱(型号MQD-S2R)购自上海旻泉仪器有限公司;组织细胞破碎仪(型号Tissueprep)购自杰灵仪器制造(天津)有限公司。
1.4 树鼩<italic>VASN</italic>基因的扩增
采用异氟烷麻醉后颈椎脱臼处死树鼩,将树鼩浸泡在75%乙醇溶液中6~10 min。紫外消毒超净台0.5 h后,将树鼩固定在超净台上(腹面朝上),剪开皮肤并剥离腹膜,暴露腹腔脏器,找到两侧肾脏并用镊子分离。其余器官组织取一部分在4%多聚甲醛溶液中固定,另一部分置于液氮中保存。按照RNA提取和反转录试剂盒的实验步骤,先提取树鼩肾脏的总RNA,然后将其反转录成cDNA。引物由南宁捷尼斯生物科技有限公司合成,上游引物ts-VASN-F3(BamHⅠ)序列为5'-AAAGGATCCCTGCAGCTCCTGGACCTGT-3',下游引物ts-VASN-R3(SalⅠ)序列为5'-GGGGT CGACGGCTCCAAGGGGGCC-3'。利用反转录得到的cDNA模板,通过聚合酶链式反应扩增得到树鼩VASN基因的全长序列。
1.5 构建树鼩pET-30a-VASN重组质粒
按照DNA纯化试剂盒步骤对扩增后的产物进行纯化,将纯化后的VASN基因片段和pET-30a质粒用BamHⅠ和SalⅠ分别进行酶切,酶切产物用T4连接酶进行连接,之后将连接产物转化到DH5ɑ感受态细胞中,并将其涂布到含25 μg/mL卡那霉素的培养平板上,37 ℃过夜培养。次日随机挑取5个单克隆菌落转接至新鲜的含卡那霉素的培养平板,继续37 ℃过夜培养以获得扩大培养的菌落。在无菌条件下,用灭菌牙签挑取单克隆菌落悬浮于9 μL无菌水中,加入10 μL 2×Phanta Max Master Mix和VASN基因特异性引物各0.5 μL进行聚合酶链式反应。反应程序为:95 ℃预变性15 min,随后95 ℃变性30 s、61 ℃退火30 s、72 ℃延伸45 s,35个循环;最后72 ℃延伸5 min。扩增产物经琼脂糖凝胶电泳分析,在约1 600 bp处出现明显条带的菌株可初步判定为阳性克隆菌株。提取聚合酶链式反应阳性单克隆菌的质粒,用BamHⅠ和Sal Ⅰ对重组质粒(pET-30a-VASN)进行双酶切鉴定。将酶切鉴定为阳性的单克隆菌落送至生工生物工程(上海)有限公司进行基因测序。
1.6 树鼩VASN重组蛋白的原核表达和纯化
将测序正确的树鼩重组质粒(pET-30a-VASN)转化到大肠杆菌BL21(DE3)中,得到树鼩pET-30a-VASN重组工程菌株。用牙签接种少许重组工程菌株到含25 μg/mL卡那霉素的10 mL LB液体培养基中,在37 ℃、200 r/min条件下过夜孵育。次日按1∶10的比例将重组工程菌株接种到含25 μg/mL卡那霉素的50 mL LB液体培养基中,在37 ℃、200 r/min条件下孵育菌液至吸光度(A)值约为0.7时,各取出15 mL含重组工程菌株的LB培养液加入到两个150 mL新的LB培养液中,分别为IPTG诱导组和未诱导组,待其吸光度(A)值为0.7时,IPTG诱导组加入终浓度为1 mmol/L的IPTG诱导剂,在37 ℃、200 r/min条件下进行蛋白诱导表达4 h;而未诱导组不加入IPTG诱导剂,其余条件与IPTG诱导组一致。在诱导表达4 h后,于4 ℃、2 500×g离心7 min,用移液枪弃上清,保留菌体沉淀。在冰浴条件下对菌体沉淀进行破胞处理,超声破碎20 min(5 s开、5 s关)后于4 ℃、2 500×g离心25 min,弃上清,保留沉淀包涵体。采用10%的SDS-PAGE蛋白胶电泳分离蛋白。待电泳结束后,取下蛋白胶置于250 mmol/L的KCl溶液中,直到出现一条边界清晰的乳白色条带,切下条带,在PBS中浸泡至无色透明状,在含PBS的离心管中捣碎胶条,4 ℃摇床过夜,用截留分子量为50 kDa的超滤管对上清液进行浓缩、过滤,重悬后得到纯化的树鼩VASN重组蛋白溶液。最后采用BCA蛋白定量试剂盒测定蛋白质量浓度,并根据测定结果用PBS调整蛋白质量浓度至1 μg/μL,分装后置于-80 ℃冰箱保存备用。
1.7 免疫BALB/c小鼠及小鼠血清效价的评定
将纯化的1 μg/μL树鼩VASN重组蛋白溶液作为免疫抗原,采用皮下注射的方式免疫6只6周龄的雌性 BALB/c小鼠。将重组蛋白VASN(150 μL/只)和等体积的弗氏完全佐剂混匀,进行首次免疫。2周后,减少重组蛋白的剂量,将重组蛋白VASN(80 μL/只)和等体积的弗氏不完全佐剂混匀,进行第2次免疫。之后每隔两周,以相同剂量(80 μL/只)分别进行第3次和第4次免疫。另取一只雌性BALB/c小鼠,皮下注射等体积的PBS作为阴性对照。在完成第4次免疫后的第7天,抽取每只经重组蛋白VASN免疫的小鼠以及阴性对照小鼠的尾静脉血约100 μL,4 ℃、3 000×g离心10 min,取血清。采用酶联免疫吸附(enzyme-linked immunosorbent assay,ELISA)法测定小鼠血清效价,取质量浓度为2 μg/mL的重组蛋白VASN,按100 μL/孔包被到酶标板上,4 ℃过夜孵育。次日每孔加入300 μL的PBST洗涤液,重复洗涤3次。每孔加入100 μL 1% BSA封闭液,在37 ℃条件下孵育30 min。取1 μL血清加入到1 mL的PBS中,进行1∶1 000的初始稀释。随后用PBS将血清依次进行3倍梯度稀释,最终得到最高稀释度数为1∶19 683 000的血清。每孔依次加入100 μL不同稀释度数的血清,在37 ℃条件下孵育60 min。取1 μL二抗(HRP山羊抗小鼠IgG)加入到10 mL的PBS中,每孔加入100 μL稀释后的二抗,在37 ℃条件下孵育30 min。以上每次孵育结束后,均用PBST洗涤3次。清洗后每孔加入100 μL显色剂,室温避光孵育30 min后,加入50 μL终止液终止反应。随后测定酶标板在450 nm处的吸光度(A)值。以P/N值≥2.1(P为阳性血清A450 nm值,N为阴性血清A450 nm值)对应的稀释比值作为小鼠的血清效价。
1.8 小鼠脾脏细胞与骨髓瘤细胞融合
选取血清效价大于1∶10 000的免疫小鼠的脾细胞,采用麻醉后颈椎脱臼法处死实验动物,将小鼠尸体完全浸没在75%乙醇溶液中消毒8 min。在已紫外消毒的超净工作台内,将消毒后的小鼠固定于解剖板上,沿腹中线依次剪开皮肤和肌层,使用无菌器械仔细分离并摘取脾脏,并将脾脏转移至预冷的无血清RPMI-1640培养基中。去除脾脏被膜及周围结缔组织后,将脾脏组织平铺于细胞筛网上,用10 mL无血清培养基润洗,以无菌注射器活塞轻柔研磨使细胞通过筛网,收集细胞悬液至15 mL离心管中,最终获得单细胞悬液用于后续融合实验。骨髓瘤细胞和小鼠脾细胞在50%聚乙二醇溶液的作用下进行细胞融合。融合过程中,前30 s使用1 mL移液器以45°角沿管壁缓慢滴加37 ℃预热的50% 聚乙二醇溶液,后30 s改为边加边旋转混匀的方式,维持细胞悬浮状态。在20% HAT选择培养液中对融合细胞进行培养。10 d后,采用ELISA对杂交瘤细胞的培养液进行检测,以P/N≥2.1作为阳性判定标准,筛选出阳性杂交瘤细胞。随后对阳性杂交瘤细胞进行3次亚克隆筛选,得到阳性单克隆细胞株。
1.9 单克隆抗体腹水的制备、纯化和鉴定
选取4只6周龄雌性BALB/c小鼠,腹腔注射石蜡油(500 μL/只),7 d后,以同样的方式注射单克隆杂交瘤细胞(1×106个/只)。观察到小鼠的腹部胀大后,用1 mL注射器收集所有小鼠的腹水,4 ℃、10 000×g离心6 min,弃去上层油脂。通过rProtein G介质填充的亲和层析柱纯化腹水,得到纯化后的单克隆抗体,收集亲和层析柱洗脱液,用截留分子量为50 kDa的超滤管对洗脱液进行过滤,得到抗树鼩VASN单克隆抗体浓缩液,用BCA蛋白定量试剂盒测定抗体质量浓度。按棋盘方阵法测定单克隆抗体的亲和力,将树鼩VASN重组蛋白梯度稀释为4 μg/mL、2 μg/mL、1 μg/mL和0.5 μg/mL;单克隆抗体按照3倍梯度稀释,从1∶1 000稀释到1∶729 000,每个浓度制备3个复孔,同时取0.1% BSA溶液作为空白孔,加入按1∶10 000稀释的二抗(HRP山羊抗小鼠IgG),反应结束后测定450 nm处的吸光度(A)值。根据下式计算结合常数Ka:Ka=(n-1)/2×(n[Ab']t-[Ab]t),n=[Ab]t/[Ab']t,式中[Ab']t和[Ab]t分别为2个不同抗原包被浓度对应的抗体浓度(μmol/L),求其平均结合常数。
分别取树鼩VASN重组蛋白、猪RBP4重组蛋白、人VASN-LRR重组蛋白和BSA标准蛋白各2.0 μg,进行SDS-PAGE电泳;另取树鼩VASN重组蛋白,分别以0.5 μg、1.0 μg、1.5 μg、2.0 μg的蛋白质量进行SDS-PAGE电泳。电泳结束后,在冰浴的条件下恒流200 mA转膜1.5 h,转膜结束后,以5%脱脂奶粉作为封闭液,室温摇床封闭2 h之后加入树鼩VASN单克隆抗体(1∶6 000稀释),4 ℃孵育过夜,之后加入HRP山羊抗鼠IgG(1∶10 000稀释),室温避光摇床孵育1 h,TBST洗涤3次后进行化学发光显色。
1.10 蛋白质印迹法检测树鼩主要组织中VASN的表达水平
采用蛋白质印迹法对树鼩主要组织(心脏、肝脏、脾脏、肺脏、肾脏、肌肉)中VASN的表达水平进行检测。从液氮中取出前期在同一只树鼩上收集到的心脏、肝脏、脾脏、肺脏、肾脏和肌肉组织,各剪取约1 mg,加入含有1 μL蛋白酶抑制剂苯甲基磺酰氟的100 μL RIPA裂解液中,随后加入不锈钢研磨珠研磨组织至无明显团块,冰上裂解30 min,每隔10 min振荡一次。4 ℃、3 000×g离心10 min,收集上清液即为组织总蛋白。BCA蛋白定量试剂盒测定蛋白质量浓度,将树鼩各组织总蛋白(30 μg),进行SDS-PAGE电泳。电泳结束后,冰浴的条件下恒流200 mA转膜1.5 h,转膜结束后,以5%脱脂奶粉作为封闭液,摇床封闭2 h之后加入树鼩VASN单克隆抗体(1∶1 000稀释),4 ℃过夜孵育,之后加入HRP山羊抗小鼠IgG(1∶6 000稀释),摇床孵育1 h,TBST洗涤3次后进行化学发光显色。
1.11 实时荧光定量PCR法检测树鼩主要组织中<italic>VASN</italic> mRNA的表达水平
使用RNA提取试剂盒,从树鼩的心脏、肝脏、脾脏、肺脏、肾脏和肌肉组织中提取RNA;再使用反转录试剂盒将RNA反转录成cDNA,反转录条件为50 ℃ 5 min,85 ℃ 5 s。引物由南宁捷尼斯生物科技有限公司合成,基因VASN上游引物序列为5'-CCCTTGGTAT CGAGCCAGTG-3',下游引物序列为5'-GGCATGACG CAGATGGAGTA-3';基因GAPDH的上游引物序列为5'-AGCCCCATCACCATCTTCC-3',下游引物序列为5'-AATGAGCCCCAGCCTTCTC-3'。实时荧光定量PCR检测基因VASN的mRNA的相对表达水平,反应条件为94 ℃ 30 s预变性;94 ℃ 5 s,60 ℃ 30 s,循环扩增40次,利用2-ΔΔCt 公式计算出基因VASN相对内参GAPDH的比值。
1.12 细胞爬片法检测树鼩永生化成纤维细胞中VASN的表达水平
将树鼩永生化成纤维细胞系接种于24孔板细胞爬片上,每孔约5×104个细胞;将其置于细胞培养箱培养5 h后,弃去细胞培养液,于冰上每孔加入500 μL冰甲醇,静置15 min;PBS洗涤三次后,将爬片置于4 ℃冰箱待用。取出待用爬片,将抗树鼩VASN单克隆抗体浓缩液稀释至2 μg/μL,滴加3∼4滴纯化后的树鼩VASN抗体(1∶500稀释),4 ℃过夜孵育。根据免疫组织化学通用二步法试剂盒中的操作步骤滴加二抗酶标羊抗鼠/兔lgG聚合物工作液,37 ℃孵育15 min,最后加 DAB显色液显色孵育3 min,以上各步骤间均使用PBS清洗3次,以去除前一步中的溶液。苏木精复染,脱水、透明、封片,于显微镜下观察染色效果。
1.13 免疫组织化学法检测树鼩脾脏组织和肺脏组织中VASN的表达水平
选取VASN表达水平相对较高的树鼩脾脏组织和肺脏组织切片进行免疫组织化学检测。将抗树鼩VASN单克隆抗体浓缩液稀释至2 μg/μL,滴加纯化后的树鼩VASN抗体(1∶250稀释)至组织切片上,4 ℃过夜孵育,滴加酶标羊抗鼠/兔lgG聚合物工作液4 ℃孵育15 min,最后加 DAB显色液显色3 min,以上各步骤间均使用PBS清洗3次,以去除上一步残留的溶液。最后进行苏木精复染,脱水、透明、封片,于显微镜下观察染色效果。
1.14 统计学分析
应用GraphPad Prism 8.0 软件进行统计分析与绘图,实验结果采用
2 结果
2.1 树鼩<italic>VASN</italic>基因的克隆与pET-30a –VASN质粒的构建
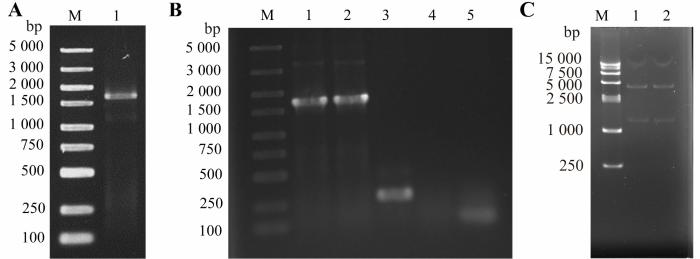
以树鼩cDNA为模板扩增VASN基因,扩增出了大小约为1 600 bp的条带,与理论大小基本相符(图1A)。挑取单克隆菌落进行聚合酶链式反应验证,随机挑取的5个单克隆菌落中有2个单克隆菌落经聚合酶链式反应可扩增出约为1 600 bp的条带,基本符合理论的树鼩VASN基因大小(图1B)。采用BamHⅠ和SalⅠ对pET-30a-VASN重组质粒进行双酶切鉴定,所得条带大小与pET-30a载体(约5 000 bp)和树鼩VASN基因片段(1 679 bp)的大小相近(图1C)。将上述重组单克隆菌株进行测序验证,结果显示其序列与树鼩VASN基因片段的序列完全一致,表明成功构建了正确的pET-30a-VASN质粒。
图1
图1
pET-30a-VASN质粒的构建
Figure 1
Construction of the pET-30a-VASN recombinant plasmid
2.2 树鼩VASN重组蛋白的获得
图2
图2
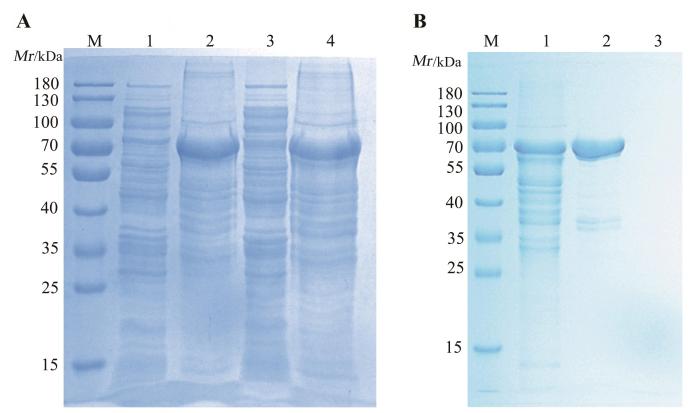
VASN重组蛋白的表达与纯化
Figure 2
Expression and purification of VASN recombinant protein
2.3 高纯度、高特异性的树鼩VASN单克隆抗体的制备
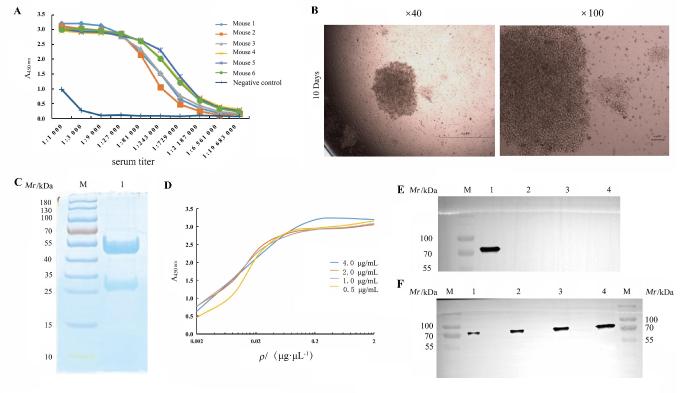
用纯化的重组蛋白VASN免疫小鼠后,小鼠血清抗体效价均可达到1∶729 000(图3A)。将小鼠脾脏细胞和SP2/0骨髓瘤细胞进行融合(图3B),对阳性细胞株进行亚克隆筛选后得到1株单克隆杂交瘤细胞株,命名为TV5-B11。用腹水诱导法诱导小鼠产生大量抗体,SDS-PAGE检测抗体的纯度,结果显示,纯化后的树鼩VASN单克隆抗体在分子量45 kDa(重链)和30 kDa(轻链)处有明显的条带(图3C),表明本研究成功得到了高纯度的单克隆抗体。选取纯化的TV5-B11单克隆抗体,采用ELISA方法检测其结合常数。结果显示,该单克隆抗体的平均结合常数为2.59×107 L/mol,亲和力较强(图3D)。蛋白质印迹结果显示,在分子量约70 kDa处可见一条明显且背景清晰的条带,表明抗树鼩VASN单克隆抗体能特异性识别树鼩VASN重组蛋白;该抗体与猪RBP4重组蛋白、人VASN-LRR重组蛋白、BSA标准蛋白均无交叉反应(图3E),且蛋白质印迹检测结果的信号强度随着VASN重组蛋白剂量的增加而增强(图3F),证明该单克隆抗体与树鼩重组VASN蛋白具有高度特异性的结合能力。
图3
图3
树鼩VASN单克隆抗体的制备
Figure 3
Preparation of monoclonal antibody to tree shrews VASN
2.4 树鼩细胞与组织中VASN的检测
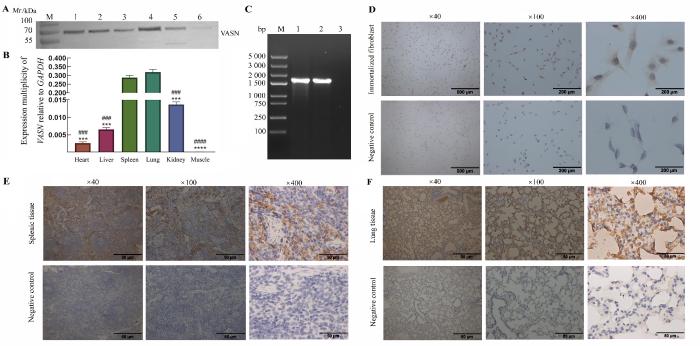
蛋白质印迹法结果显示,抗树鼩VASN单克隆抗体与树鼩的主要器官组织(心脏、肝脏、脾脏、肺脏、肾脏、肌肉)蛋白均可发生特异性反应,在分子量约70 kDa位置出现一条明显的条带,且背景清晰(图4A)。通过实时荧光定量PCR法检测树鼩主要器官组织中VASN的表达水平,结果显示树鼩脾脏组织和肺脏组织中基因VASN的mRNA相对表达水平较高(P<0.05,图4B)。免疫组织化学结果显示,该抗体特异性良好。在树鼩永生化成纤维细胞中,VASN蛋白定位于细胞质中,呈棕黄色阳性信号(图4C);在树鼩脾脏组织(图4D)和肺脏组织(图4E)中,可同样检测到棕黄色阳性信号;而在mRNA相对表达水平较低的心脏和肝脏组织中,免疫组织化学检测结果为阴性,所有阴性对照组(不加一抗)的检测结果也均为阴性。
图4
图4
树鼩VASN抗体的应用
Figure 4
Application of tree shrews VASN antibody
3 讨论
树鼩是一种小型哺乳动物,在分类学上属于介于灵长目与食虫目之间的树鼩目[22]。由于树鼩与灵长类动物的进化关系比啮齿类动物更接近,因此有大量学者以树鼩为实验动物模型,研究了许多基因在疾病中的作用机制[23-25]。单克隆抗体作为抗原物质的分子识别工具,在生物医学基础研究中具有重要作用[26]。在单克隆抗体的制备技术中,杂交瘤技术是经典且广泛应用的方法,该技术通过将免疫后的小鼠B淋巴细胞与骨髓瘤细胞融合,形成杂交瘤细胞,从而能够稳定地分泌特异性单克隆抗体。通过单克隆抗体制备技术制备出的杂交瘤细胞不仅具有在体外不断增殖的能力,而且也能产生针对特定抗原表位的抗体[27-28]。近年来,随着分子生物学技术的发展,重组抗体技术[29]逐渐成为重要的替代方案。通过基因工程手段,可以直接从抗体基因库中筛选和表达特异性抗体片段,如单链抗体或纳米抗体[30]。这种技术不仅缩短了抗体制备周期,还能够针对特定抗原进行定向设计和优化,同时避免了传统动物实验可能涉及的伦理问题。此外,噬菌体展示技术和单细胞测序技术的结合[31],进一步提高了抗体的筛选效率和多样性。与杂交瘤技术相比,重组抗体技术在灵活性和效率上具有明显的优势,但其生产成本较高,且在某些情况下所得抗体的稳定性和亲和力可能不如传统方法。因此,本研究通过传统的杂交瘤技术制备出针对树鼩VASN的单克隆抗体TV5-B11,并对该抗体进行初步的应用研究,为VASN在树鼩中的基础研究提供一种新的分子研究工具,也有助于深入研究VASN的作用机制及其参与的生理功能。
本研究选用E.coli原核表达系统表达出了树鼩VASN重组蛋白,该系统表达的重组蛋白在诊断试剂开发及生物制药领域占据核心地位[32-33]。采用高纯度树鼩VASN重组蛋白对小鼠进行免疫,可减少非特异性抗体的产生。相较于短周期、高剂量免疫原的免疫程序,采用长周期、低剂量免疫原的免疫程序可获得更好的免疫应答效果。实验检测结果证明,经免疫获得的6只小鼠血清抗体效价均可达1∶729 000,而后通过亚克隆的方法筛选出了能够产生高效价、高特异性抗体的单克隆细胞株。采用小鼠腹水诱生法制备出大量树鼩VASN单克隆抗体,通过亲和层析柱纯化得到了高纯度、高效价的树鼩VASN单克隆抗体。特异性检测结果表明,TV5-B11能够与树鼩VASN蛋白发生特异性结合,与其他种属蛋白(猪RBP4重组蛋白、人VASN-LRR重组蛋白及BSA标准蛋白)均未发生交叉反应,TV5-B11对树鼩VASN的表位识别具有高度种属特异性,可能归因于其靶向的抗原表位在进化过程中存在种间序列差异或空间构象特异性。这种特性使得TV5-B11成为研究树鼩VASN功能的理想工具,尤其在跨物种比较研究中可避免其他种属同源蛋白的干扰。此外,在树鼩的主要器官组织(包括心脏、肝脏、脾脏、肺脏、肾脏和肌肉)中,该抗体在相对分子质量约70 kDa处均检测到明显条带,其他位置未见明显杂带,提示该抗体识别稳定性良好,且可在组织裂解液的复杂成分中保持高特异性,为其在免疫组织化学、蛋白质印迹等应用中的可靠性提供了实验依据。由于目前没有专门针对树鼩的商业化内参抗体,因此在图4A中没有内参,本研究只探究了自主研发的树鼩VASN单克隆抗体是否能应用于检测树鼩各主要器官组织的蛋白表达。
通过利用自主研发的树鼩VASN单克隆抗体检测了树鼩永生化成纤维细胞中VASN的表达,发现树鼩TV5-B11能够有效地结合树鼩永生化成纤维细胞抗原,在VASN相对表达水平较高的树鼩脾脏和肺脏组织中也能有效地结合抗原位点,表明自主研发的树鼩VASN单克隆抗体可应用于细胞和组织的免疫组织化学染色检测。VASN在不同组织中的分布与其生物学功能密切相关,在VASN基因敲除(Knockout,KO)小鼠模型中,小鼠肺部出现了与肺损伤模型小鼠相似的病理特征[21],同时在VASN KO小鼠中也发现因VASN基因缺陷导致的小鼠心肌结构异常、心脏肥大[34]以及心肌纤维化的现象[35];此外,VASN KO小鼠的肝脏比重显著降低,并伴有肝功能异常、肝损伤的病理特征[13]。总体而言,VASN在不同组织中的分布反映了其在维持组织稳态、修复损伤以及调控疾病发生发展中的重要作用。
综上所述,本研究通过对树鼩VASN基因的扩增,成功构建出树鼩VASN重组质粒,并用大肠杆菌原核表达系统成功表达出了树鼩VASN重组蛋白,经纯化得到了纯度为90%的重组蛋白。而后进一步利用杂交瘤融合技术和细胞的亚克隆筛选,得到了能够产生抗树鼩VASN单克隆抗体的细胞株,为VASN在树鼩中的基础研究提供一种新的分子研究工具。本研究的不足之处在于,采用腹水诱生法制备抗体所需动物实验时间较长,且长时间的实验过程对实验动物会有一定的伤害。后续实验将优化实验流程,通过非动物来源的抗体生产系统来生产抗体。
引用本文
欧美珍, 李泳锋, 温莎, 等. 树鼩Vasorin单克隆抗体的制备及其应用探索[J]. 实验动物与比较医学, 2025, 45(5): 611-622. DOI: 10.12300/j.issn.1674-5817.2025.027.
OU M Z, LI Y F, WEN S, et al. Preparation of monoclonal antibody to Vasorin in tree shrew and exploration of its application[J]. Lab Anim Comp Med, 2025, 45(5): 611-622. DOI: 10.12300/j. issn. 1674-5817.2025.027.
作者贡献声明
欧美珍负责实验方案设计,实验操作、数据分析、初稿写作和文章修改;
李泳锋和温莎参与各项实验的实施;
廖舟翔和黄雪静参与实验指导和写作指导;
何敏和杨丽超负责提供项目资助、实验方案设计以及稿件审阅和修订。
医学伦理声明Medical Ethics Statement
本研究涉及的所有动物实验均已通过广西医科大学实验动物福利与伦理委员会审批(审批号:202212016、202304007、202307013)。所有实验过程均遵照中国实验动物相关法律法规条例要求进行。
Medical Ethics Statement
All animal experiments involved in this study have been approved by the Laboratory Animal Welfare and Ethics Committee of Guangxi Medical University (Approval Number: 202212016, 202304007, 202307013). All experimental operations have been carried out in accordance with the requirements of the relevant laws and regulations on laboratory animals in China.
利益冲突声明
本文所有作者均声明不存在利益冲突。
参考文献
树鼩在人类疾病动物模型中应用研究进展
[J].
Development of application of tree shrew in human disease animal models research
[J].
树鼩的标准化研究与应用进展
[J].
Standardization and application progress of tree shrew
[J].
树鼩的生物学特性研究概述
[J].
Introduction to biological characteristics of tree shrew
[J].
The potential of monoclonal antibodies for colorectal cancer therapy
[J].
单克隆抗体在肾移植免疫抑制治疗中的应用进展
[J].
The application of monoclonal antibodies in immunosuppressive strategies of renal transplantation
[J].
Cancer therapy with antibodies
[J].
Antibody-based approaches to target pancreatic tumours
[J].
The present and future of bispecific antibodies for cancer therapy
[J].
Revolutionizing cancer immunotherapy: unleashing the potential of bispecific anti-bodies for targeted treatment
[J].
瑶山亚种树鼩IFN-β和IFN-γ原核表达及其多克隆抗体制备
[J].
Prokaryotic expression and polyclonal antibody preparation of IFN-β and IFN-γ of Tupaia belangeri yaoshanensis
[J].
瑶山亚种树鼩ISG15蛋白表达及其多克隆抗体制备
[J].
Expression of ISG15 protein of Tupaia belangeri yaoshanensis and preparation of its polyclonal antibody
[J].
树鼩IgG纯化鉴定及其多克隆抗体制备和检测
[J].
Purification of tree shrews(Tupaia) immunoglobulin G and preparation of anti-IgG polyclonal antibody
[J].
ADAM17 (TACE) regulates TGF-β signaling through the cleavage of vasorin
[J].
Vasorin, a transforming growth factor beta-binding protein expressed in vascular smooth muscle cells, modulates the arterial response to injury in vivo
[J].
Vasorin promotes endothelial differentiation of glioma stem cells via stimulating the transcription of VEGFR2
[J].
VASN promotes colorectal cancer progression by activating the YAP/TAZ and AKT signaling pathways via YAP
[J].
Vasorin/ATIA promotes cigarette smoke-induced transformation of human bronchial epithelial cells by suppressing autophagy-mediated apop-tosis
[J].
Vasorin deletion in C57BL/6J mice induces hepatocyte autophagy through glycogen-mediated mTOR regulation
[J].
Vasorin promotes proliferation and migration via STAT3 signaling and acts as a promising therapeutic target of hepatocellular carcinoma
[J].
VASN promotes the aggressive phenotype in ARID1A-deficient lung adenocar-cinoma
[J].
Vasorin contributes to lung injury via FABP4-mediated inflammation
[J].
Study of tree shrew biology and models: a booming and prosperous field for biomedical research
[J].
A tree shrew glioblastoma model recapitulates features of human glioblastoma
[J].
Structure and function of cholesteryl ester transfer protein in the tree shrew
[J].
Tree shrews as a new animal model for systemic sclerosis research
[J].
A comprehensive review of monoclonal antibodies in modern medicine: tracing the evolution of a revolutionary therapeutic approach
[J].
Of mice and men: hybridoma and recombinant antibodies
[J].
The development of methods for obtaining monoclonal antibody-producing cells
[J].
基因工程重组抗体技术的研究进展
[J].
Research progress of recombinant antibody technology in genetic engineering
[J].
纳米抗体的研究进展及其应用现状
[J].
Research progress and application of nanobodies
[J].
抗体技术的研发现状与展望
[J].
Development and prospect of antibody technology
[J].
Recombinant protein expression in E. coli: a historical perspective
[J].
Recombinant protein expression in Escherichia coli: advances and challenges
[J].
Vasorin deficiency leads to cardiac hypertrophy by targeting MYL7 in young mice
[J].
VASN knockout induces myocardial fibrosis in mice by downregulating non-collagen fibers and promoting inflammation
[J].