目前用于DENV体外研究的细胞模型有非洲绿猴肾细胞Vero、叙利亚仓鼠肾细胞BHK-21、幼蚊细胞C6/36、人非小细胞肺癌细胞A549及人脐静脉内皮细胞HUVEC等,它们对DENV有较高的敏感性[6-8]。然而,DENV在C6/36细胞中的复制动力学及细胞免疫应答特征可能与人体生理反应有所不同[9];DENV在Vero、BHK-21细胞中连续传代会出现毒力减弱的情况[8-10]。此外,Vero细胞存在Ⅰ型干扰素(typeⅠ interferons,IFN-Ⅰ)分泌缺陷[11],该细胞用于DENV机制研究可能导致结果出现偏差。由于常用细胞系存在一定不足,需要筛选更多易感细胞系,为不同的研究目的提供更多选择。已有研究结果证实,从树鼩不同组织分离的多种细胞可用于病毒感染研究。例如,Zhao等[12]证实,原代树鼩肝细胞易受丙型肝炎病毒感染;Zhang等[13]发现,树鼩肾、肺、肝、皮肤和主动脉的原代细胞易受寨卡病毒感染,并诱导原代皮肤和原代胸主动脉细胞产生先天性抗病毒反应;Kayesh等[14]发现,树鼩肺成纤维细胞对4种血清型的DENV都具有易感性;丁相荣等[15]发现,DENV在树鼩角膜基质细胞(tree shrew corneal stromal cells,TCSCs)上出现病变的时间早于Vero细胞。以上研究表明,树鼩细胞在DENV相关研究中具有较大潜力。然而,树鼩细胞系对DENV的易感性及感染特征数据十分匮乏。
1 材料与方法
1.1 细胞与病毒株
8种树鼩细胞系包括树鼩主动脉内皮细胞(tree shrew aortic endothelial cells,TAECs)、树鼩主动脉平滑肌细胞(tree shrew aortic smooth muscle cells,TASMCs)、树鼩肝细胞(tree shrew hepatocytes,THs)、原代树鼩肾上皮细胞(primary tree shrew renal epithelial cells,pTRECs )、树鼩皮肤成纤维细胞(tree shrew skin fibroblasts,TSFs)、TCSCs、树鼩脑微血管内皮细胞(tree shrew brain microvascular endothelial cells,TBMECs)、树鼩视网膜微血管内皮细胞(tree shrew retinal microvascular endothelial cells,TRMECs),均由本实验室分离鉴定,稳定传代后保存。
4种阳性对照细胞系包括C6/36细胞(由中国医学科学院医学生物学研究所孙强明研究员惠赠,并由本实验室稳定传代后保存),以及A549细胞、Vero细胞和BHK-21细胞(均为本实验室传代保存)。
DENV Ⅱ型43株(GenBank: AF204178),由清华大学程功实验室惠赠,由本实验室经C6/36扩增后保存。
1.2 主要试剂与仪器
DMEM/F-12(1∶1)培养基(VivaCell,C3130-0500)和PBS(VivaCell,C3580-0500)为上海逍鹏生物科技有限公司产品;RPMI 1640培养基(C11875500BT)、青霉素-链霉素溶液(Gibco,15140-122)和胰蛋白酶(Gibco,25200-056)为美国Thermo Fisher Scientific公司产品;胎牛血清(CellBox,CF-01P-02)为长沙赛尔博克斯生物科技有限公司产品;QIAamp®病毒RNA小提试剂盒(52906)为德国Qiagen公司产品;One Step Prime ScriptTM RT-PCR试剂盒(RR064A)为日本TaKaRa公司产品;低熔点琼脂糖(Biosharp,BS384)和结晶紫染色液(Solarbio,G1062)为北京杰兰柯科技有限公司产品;引物和探针由生工生物工程(上海)股份有限公司合成。
35 mm细胞培养皿(706001)为无锡耐思生命科技股份有限公司产品;细胞计数仪(TC20)为美国Thermo Fisher Scientific公司产品;定时定量PCR仪(BFX-950)为美国Bio-Rad公司产品;生物安全柜(1287)和恒温培养箱(CO2T/C)为美国FORMA公司产品;倒置荧光相差显微成像系统(ECLIPSE Ti-S)为日本Nikon公司产品。
1.3 实验室生物安全条件
依据《人间传染的病原微生物目录》(国卫科教发〔2023〕24号)和《病原微生物实验室生物安全管理条例》(2018年3月19日修订版),DENV体外研究所需生物安全实验室等级为BSL-2。本研究在中国医学科学院医学生物学研究所药物安全评价中心病原微生物安全实验室开展,实验室的生物安全备案证号为2024SW0025。
1.4 细胞培养及病毒接种
所有细胞复苏后接种于T25培养瓶。C6/36细胞使用RPMI 1640完全培养基(含10%胎牛血清、1%青霉素-链霉素),于5% CO2、28 ℃培养箱培养;其他细胞使用DMEM/F-12(1∶1)完全培养基(含10%胎牛血清、1%青霉素-链霉素),于5%CO2、37 ℃培养。当细胞生长至80%~90%时,接种于多个35 mm直径的细胞培养皿,过夜培养12 h以上。细胞汇合度约为60%~70%时,计数。弃去原培养液,用PBS洗一次。感染组加入500 μL维持液(含2%胎牛血清、1%青霉素-链霉素的培养基),以感染复数(multiplicity of infection,MOI)为0.02的剂量分别将病毒液接种于感染组培养皿中,孵育2 h;所有树鼩细胞和阳性对照细胞设置未感染的阴性对照组,仅加入等体积维持液。弃去培养液,PBS洗一次,加入2 mL维持液(含2%胎牛血清、1%青霉素-链霉素的培养基),继续培养。
1.5 细胞病变观察
每隔12 h在倒置显微镜下观察感染组和对照组的细胞形态,拍照并记录细胞病变效应(cytopathic effect,CPE);同时取4份感染组培养皿,封口后移入-80 ℃冰箱冻存。各组均观察至病变终点(≥95%CPE)或未感染细胞老化死亡。未见CPE记为“-”;疑似CPE记为“±”;0%~25%CPE记为“+”;26%~50%CPE记为“++”;51%~75%CPE记为“+++”;76%~100%CPE记为“++++”。
1.6 病毒增殖检测
将冻存的细胞培养皿于-80 ℃冻融两次,使细胞充分裂解。将培养皿内所有液体,连同细胞碎片,一同移入离心管后,1 200×g、4 ℃离心10 min,收集上清液。用QIAamp®病毒RNA小提试剂盒提取病毒基因组RNA。用One Step Prime ScriptTM RT-PCR试剂盒进行实时荧光定量PCR,检测病毒核酸载量。DENV C基因引物设计参考文献[18],正向引物(DENV-F)序列为:5'-AATTAGAGAGCAGATCTCTGATGAA-3',反向引物(DENV-R)序列为5'-AGCATTCCAAGTG-AGAATCTCTTTGT-3';探针(Probe)序列为5'-FAM-CTGTTGTACAGTCGACACGCGGTTTCTC-BHQ1-3'。反应体系包括2×一步式RT-PCR反应液Ⅲ 10 μL,TaKaRa Ex Taq HS聚合酶(5 U/μL)、PrimeScript RT酶混合液Ⅱ、正反向引物(10 μmol/L)和探针各0.4 μL,RNase Free ddH2O 7 μL,总RNA 1 μL,反应条件:42 ℃ 5 min,95 ℃ 10 s;95 ℃ 5 s,55 ℃ 20 s,循环40次。分别以感染后小时数(hours post infection,hpi)和起始模板量对数值(log10 copies/μL)的平均值,绘制不同树鼩细胞中的病毒增殖曲线,并与阳性对照细胞进行比较。
1.7 病毒滴度测定
当细胞病变程度达到75%~80%时(即CPE刚达到最大),病毒的复制和释放达到相对较高的水平,此时是收获病毒的适宜时间。根据1.6节中获得的病毒核酸载量检测结果,选择载量最高的前5种细胞用于DENV的培养。在各培养细胞病变达到75%~80 %时收获病毒液,并采用噬斑实验测定不同细胞的病毒感染性滴度。步骤如下:用维持液(含2%胎牛血清、1%青霉素-链霉素的培养基)10倍梯度稀释病毒液(10-1~10-5),接种于长成单层的Vero细胞,每个梯度接种2孔,对照孔加入不含病毒的维持液,置于细胞培养箱中孵育2 h;弃去孵育液,PBS洗涤;将2%低熔点琼脂糖和培养基(含4%胎牛血清、2%青霉素-链霉素)按1∶1混合,待温度降至37 ℃左右时将混合液覆盖于细胞孔上,继续培养7 d。待形成噬斑后,加入4%甲醛溶液固定1 h,用流水轻轻洗去覆盖物和甲醛,加入结晶紫染液后于室温孵育30 min,用水冲洗并晾干,计数噬斑形成单位(plaque forming unit,PFU)。根据公式计算滴度:病毒滴度(PFU/mL)=平均噬斑形成单位×稀释倍数/每孔接种体积(mL)。
1.8 数据统计分析
采用GraphPad Prism 8软件进行统计分析和制图。实验结果以
2 结果
2.1 DENV感染后7种树鼩细胞发生显著病变
在DENV接种后观察的6 d(144 h)内,所有细胞均出现光学显微镜下可分辨的细胞病变,出现CPE的时间见表1。TSFs产生可分辨病变的时间最早,为感染后24 h;4种树鼩细胞TAECs、TASMCs、THs、pTRECs以及C6/36均于感染36 h出现病变;TCSCs以及2种常用细胞BHK-21、A549于感染48 h出现病变;TBMECs和Vero于感染60 h出现病变;而树鼩细胞TRMECs的病变始终不明显。
表1 登革病毒感染不同细胞后的细胞病变效应变化
Table 1
细胞 Cell | 接种后时间/h Time post-infection/h | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 12 | 24 | 36 | 48 | 60 | 72 | 84 | 96 | 108 | 120 | 132 | 144 | |
| TAECs | - | - | + | ++ | +++ | ++++ | ++++ | ++++ | ||||
| TASMCs | - | - | + | ++ | +++ | ++++ | ++++ | ++++ | ||||
| THs | - | - | + | + | ++ | +++ | ++++ | ++++ | ||||
| pTRECs | - | ± | + | ++ | +++ | ++++ | ++++ | ++++ | ||||
| TSFs | ± | + | ++ | +++ | +++ | ++++ | ++++ | ++++ | ||||
| TCSCs | - | - | ± | + | + | ++ | +++ | +++ | ++++ | ++++ | ||
| TBMECs | - | - | - | ± | + | ++ | +++ | +++ | ++++ | ++++ | ||
| TRMECs | - | - | - | ± | ± | + | + | + | + | + | ||
| Vero | - | - | - | ± | + | + | + | + | ++ | ++ | +++ | ++++ |
| BHK-21 | - | - | - | + | ++ | +++ | +++ | ++++ | ++++ | ++++ | ++++ | |
| A549 | - | - | ± | + | + | ++ | ++ | +++ | +++ | +++ | ++++ | ++++ |
| C6/36 | - | - | + | + | ++ | ++ | +++ | +++ | +++ | +++ | +++ | ++++ |
5种树鼩细胞TAECs、TASMCs、THs、pTRECs和TSFs于感染72~84 h时病变达到最大,早于阳性对照细胞BHK-21(96 h)、A549(132 h)、C6/36(144 h)和Vero(144 h);2种树鼩细胞TCSCs和TBMECs于108 h时病变程度达到最大,早于阳性对照细胞A549、C6/36和Vero。
2.2 DENV感染后7种树鼩细胞形态变化
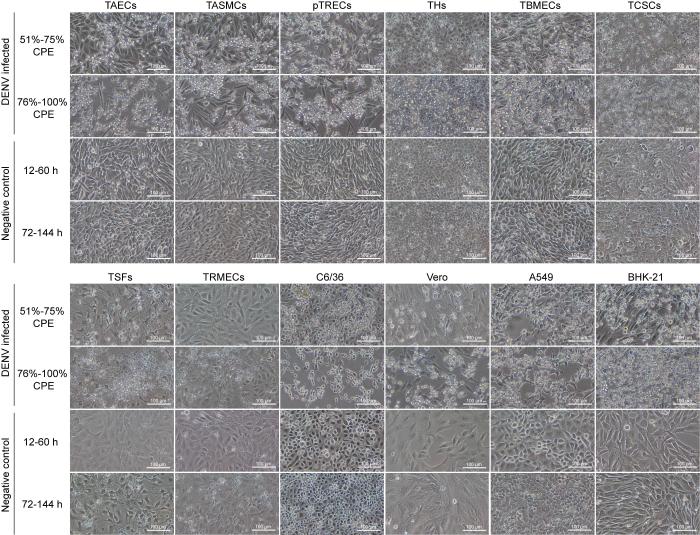
在倒置显微镜下,树鼩细胞TAECs、TASMCs、pTRECs及TBMECs呈梭形或多角形,具有相似的CPE特征(图1):在病变中期(51%~75%CPE),部分细胞变圆、脱落,导致胞间隙增大,细胞呈拉丝状,此后细胞快速大量脱落;在病变晚期(76%~100% CPE),少量仍贴壁的细胞呈细长梭形或不规则形,边缘粗糙、颗粒增多;TBMECs同时出现空泡化,最后全部脱落。而另外4种树鼩细胞的CPE不明显:THs呈圆形或多边形,发生病变的细胞变圆、脱落,可见细胞碎片,最终细胞碎片和死细胞黏附在底部残留的细胞骨架上;TSFs呈梭形,病变细胞快速裂解,呈剧烈拉丝状,虽然未感染TSFs也出现了拉丝状,但感染组明显更加严重;TCSCs呈梭形至多角形,病变细胞裂解或变圆脱落,平皿底部残留细胞骨架。TRMECs被感染后出现拉丝状,但未感染的TRMECs也出现拉丝,虽然感染组相较于未感染对照组产生更多细胞脱落和拉丝现象,但对比不明显。
图1
图1
倒置显微镜下不同来源的树鼩细胞和阳性对照细胞感染登革病毒前后的形态学变化(×200)
Figure 1
Morphological changes in tree shrew cells of different tissues and positive control cells before and after dengue virus (DENV) infection under inverted microscope (×200)
依照各种细胞的特点,DENV引起树鼩细胞发生的CPE类型可分为:①细胞变圆、脱落(见于本实验中所有细胞);②细胞伸长、拉丝(见于TAECs、TASMCs、pTRECs、TBMECs和TSFs);③细胞空泡化(见于TBMECs);④细胞碎裂(见于THs和TCSCs)。以上结果表明,7种树鼩细胞感染DENV后产生了不同程度的CPE。
2.3 DENV感染后不同树鼩细胞的病毒载量
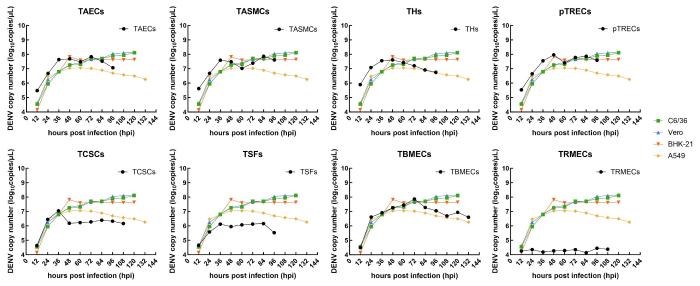
感染DENV后,每12 h采用实时荧光定量PCR法检测各种细胞培养物中的病毒载量,共4次。由图2可知,除TRMECs外,其他7种树鼩细胞对DENV均易感,而且在感染DENV后病毒载量呈先升后降的趋势,达到峰值后病毒载量水平能维持一段时间。
图2
图2
实时荧光定量PCR检测感染不同来源的树鼩细胞后登革病毒的增殖曲线
Figure 2
Viral proliferation curves of tree shrew cells of different tissues after dengue virus (DENV) infection via real-time fluorescent quatitative PCR
各种细胞感染后病毒载量达到峰值的时间见表2,树鼩细胞中pTRECs的病毒载量最高(9.18×107拷贝/μL),最接近阳性对照细胞C6/36和Vero的病毒载量,其次为TBMECs(7.43×107拷贝/μL)、TASMCs(7.27×107拷贝/μL)、TAECs(6.87×107拷贝/μL)和THs(4.08×107拷贝/μL),这5种树鼩细胞的病毒拷贝数均高于4×107拷贝/μL,处于阳性对照细胞峰值载量最高值(Vero)和最低值(A549)之间。
表2 各种细胞感染后病毒载量峰值及达到峰值的时间
Table 2
细胞 Cell | 病毒载量峰值/(拷贝·μL-1) Peak viral load/ (copies·μL-1) | 时间/h Time/ h |
|---|---|---|
| pTRECs | (9.18±0.21)×107 | 48 |
| TBMECs | (7.43±0.75)×107 | 72 |
| TASMCs | (7.27±0.43)×107 | 84 |
| TAECs | (6.87±0.30)×107 | 72 |
| THs | (4.08±0.02)×107 | 48 |
| TCSCs | (1.11±0.05)×107 | 36 |
| TSFs | (1.50±0.05)×106 | 84 |
| Vero | (1.39±0.22)×108 | 120 |
| C6/36 | (1.28±0.21)×108 | 120 |
| BHK-21 | (6.73±0.13)×107 | 48 |
| A549 | (1.13±0.05)×107 | 60 |
2.4 不同树鼩细胞的DENV滴度
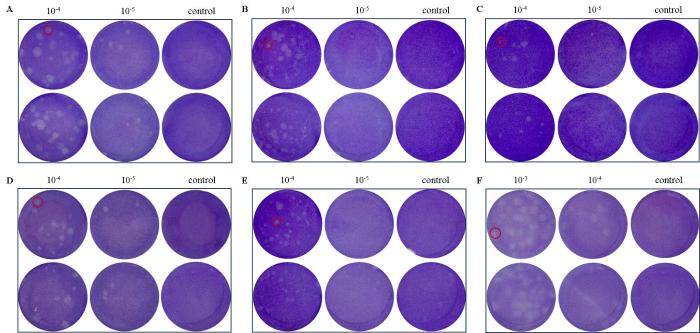
检测病毒感染性的噬斑实验结果见图3,噬斑区为不染色区域,斑块较大、轮廓较清晰,可用于噬斑计数。选择10-4和10-5这2个病毒液稀释度,每个稀释度设2个重复孔,即共4个孔进行计数,然后计算病毒滴度。5种树鼩细胞均可产生感染性子代病毒,其中TAECs中增殖的DENV滴度最高[(3.13±0.61)×105 PFU/mL],接近于阳性对照细胞C6/36[(3.85±1.95)×105 PFU/mL];其次为THs[(2.03±0.68)×105 PFU/mL]、pTRECs[(1.58±0.66)×105 PFU/mL],与阳性对照细胞C6/36相比明显降低(P<0.05);TASMCs中DENV滴度为[(1.03±0.05)×105 PFU/mL],TBMECs中DENV滴度为[(0.29±0.14)×105 PFU/mL],均显著低于阳性对照细胞(P<0.01)。
图3
图3
噬斑实验测定不同树鼩细胞中登革病毒的病毒滴度
Figure 3
Quantification of dengue virus (DENV) titer in tree shrew cells of different tissues via plaque assay
3 讨论
已知DENV感染伊蚊后,首先在肠道中进行复制,进而被转运到唾液腺。在伊蚊叮咬人的过程中,病毒通过唾液被接种到皮肤的真皮层(少量释放入血),被皮下组织的单核细胞吞噬,传播至单核-巨噬细胞系统,病毒增殖后进入血液,引起病毒血症;随后病毒在组织的网状内皮系统和淋巴组织中增殖,再次入血引起病毒血症[19]。DENV可通过多种途径引起复杂多样的临床症状。研究表明,DENV与抗体形成的免疫复合物以及病毒NS1蛋白介导可引起血管通透性增加和凝血系统障碍,从而导致多种组织器官的血浆渗漏、出血;重症登革热可导致休克、肝损伤、肾损伤、神经系统并发症、眼病、横纹肌溶解等多个器官系统受累[16,20]。然而,重症登革热的具体机制至今未完全阐明。现有研究认为,多种因素如细胞因子风暴、抗体依赖性增强效应、病毒变异等均参与了DENV的致病过程[21-22]。
DENV感染易感细胞后引起细胞病变是构成感染的直接标志,同时细胞内的信号转导途径发生变化,从而导致了可从组织学、免疫组织化学、分子水平等各种方法检测的感染表征[23]。这些表征是理解病毒与细胞互作机制的基础,也是体内实验的重要参考。据文献报告,常用于DENV体外研究的非洲绿猴肾细胞Vero对多种病毒易感是因为干扰素基因表达缺陷[24],虽然其获得了广谱病毒易感性,也可能由于无IFN-Ⅰ的环境而忽略了病毒在与宿主免疫系统互作时的某些关键适应机制,或放大了药物的有效性,因此限制了该细胞在某些病毒感染机制研究中的应用。另外两种常用的幼蚊细胞C6/36和叙利亚仓鼠肾细胞BHK-21因物种亲缘关系与人较远,在机制研究中不具有明显优势。因此,需要在与人类亲缘关系近的物种中寻找合适的细胞,以帮助研究者理解DENV感染、致病机制和跨物种传播风险。
综上,本研究选择的8种树鼩细胞中,有7种细胞(TAECs、TASMCs、THs、pTRECs、TSFs、TCSCs和TBMECs)发生了可明确辨别的CPE,表现出差异的敏感性和不尽相同的病变特征,且与相应的人源细胞和病例报告在某些方面相符合。同样地,病毒增殖的分子水平检测结果也提示这7种树鼩细胞能够支持DENV复制和感染,而且病毒拷贝数随感染时间而升高;其中5种树鼩细胞pTRECs、TBMECs、TASMCs、TAECs和THs与阳性对照细胞相当,均能产生感染性子代病毒;3种树鼩细胞TAECs、THs、pTRECs与阳性对照细胞C6/36的子代病毒滴度相当。本研究结果表明,树鼩细胞具有作为DENV感染机制研究和抗病毒药物开发工具的潜力,它们可能也是DENV在树鼩体内的感染位点。值得注意的是,相较于常用的Vero和BHK-21细胞,树鼩细胞生长速度更快,对病毒感染更敏感,DENV感染树鼩细胞后更早达到75%~80% CPE(尤其是TAECs、pTRECs、THs),且产生的病毒载量和滴度噬斑数达到了常用细胞系水平,因此在病毒制备时能够兼顾病毒产量和生产效率。
综上所述,本研究选择的7种树鼩细胞对DENV均具有易感性,其中pTRECs、TAECs、THs是发展为DENV病毒培养工具的潜力细胞。同时本研究提示,这些树鼩细胞来源的体内组织器官可能是DENV感染的致病部位,建议研究人员在整体动物造模时应关注这些组织器官。
[引用本文]
刘欣, 杞梦迪, 王文广, 等. 登革病毒对树鼩不同组织来源细胞的易感性及感染特性研究[J]. 实验动物与比较医学, 2025, 45(2): 229-238. DOI: 10.12300/j.issn.1674-5817.2024.178.
LIU Xin, QI Mengdi, WANG Wenguang, et al. Study on Susceptibility and Infection Characteristics of Dengue Virus in Cells Sourced from Different Tissues of Tree Shrews[J]. Laboratory Animal and Comparative Medicine, 2025, 45(2): 229-238. DOI: 10.12300/j.issn.1674-5817.2024.178
作者贡献声明
刘欣负责实验方法设计、结果可视化和初稿写作;
杞梦迪、王文广负责提供资源,参与有效验证或监督指导;
罕园园负责监督指导、写作审编;
陆美丽、李娜参与有效验证或研究项目管理;
代解杰负责研究方案策划、方法设计、监督指导和论文修订;
陆彩霞负责获取项目资助和管理,以及实验监督指导。
利益冲突声明
所有作者均声明本文不存在利益冲突。
参考文献
Dengue viruses cleave STING in humans but not in nonhuman primates, their presumed natural reservoir
[J].
Dengue vaccine development: challenges and prospects
[J].
Molecular mechanisms in the pathogenesis of dengue infections
[J].
Mammalian animal models for dengue virus infection: a recent overview
[J].
High-throughput quantitative proteomic analysis of dengue virus type 2 infected A549 cells
[J].
Nuclei ultrastructural changes of C6/36 cells infected with virus dengue type 2
[J].
登革病毒感染C6/36、Vero、BHK-21和THP-1细胞CPE的比较及病毒检测
[J].
CPE caused by dengue virus in C6/36, Vero, BHK-21 and THP 1 cells and virus test
[J].
Ⅲ型登革病毒在C6/36及Vero细胞中复制对其毒力的影响
[J].
Effect of replication of dengue virus type Ⅲ in C6/36 and Vero cells on virulence
[J].
Dengue type 4 live-attenuated vaccine viruses passaged in vero cells affect genetic stability and dengue-induced hemorrhaging in mice
[J].
Regulation of the interferon system: evidence that vero cells have a genetic defect in interferon production
[J].
Primary hepatocytes of Tupaia belangeri as a potential model for hepatitis C virus infection
[J].
Infectivity of Zika virus on primary cells support tree shrew as animal model
[J].
Susceptibility and initial immune response of Tupaia belangeri cells to dengue virus infection
[J].
树鼩角膜基质永生化细胞系的构建及其在病毒感染性方面的研究
[J].
Construction of immortalized tree shrew corneal stromal cell line and investigation of viral infectivity
[J].
Dengue infection
[J].
Clinical characteristics and outcomes among travelers with severe dengue: a GeoSentinel analysis
[J].
登革1型病毒和登革2型病毒在C6/36细胞及白纹伊蚊体内共感染的研究
[D].
Research on co-infection of DENV-1 and DENV-2 in C6/36 cells and Aedes albopictus
[D].
Dengue: a minireview
[J].
Progress towards understanding the pathogenesis of dengue hemorrhagic fever
[J].
Knowledge gaps in the epidemiology of severe dengue impede vaccine evaluation
[J].
Evaluation of cell substrates for the production of biologicals: Revision of WHO recommendations. Report of the WHO Study Group on Cell Substrates for the Production of Biologicals, 22-23 April 2009, Bethesda, USA
[J].
人用疫苗生产用细胞基质使用现状及研究进展
[J].
Current status and research progress of cell substrate for human vaccine production
[J].
Cell substrates for the production of viral vaccines
[J].
Vero细胞传代过程中致瘤性的检测
[J].
Experimental investigation on tumorigenicity of Vero cell in the process of passage
[J].
Dengue: Another viral infection with mucocutaneous manifestations
[J].
Assessment of prolonged dengue virus infection in dermal fibroblasts and hair-follicle dermal papilla cells
[J].
Mechanisms of programmed cell death associated to severe dengue in human renal lesions
[J].
Apoptosis in dengue virus infected liver cell lines HepG2 and Hep3B
[J].
A 66-year old woman with large vessel vasculitis after a dengue virus infection
[J].
Dengue virus infection of primary human smooth muscle cells
[J].
登革3型病毒感染人脑微血管内皮细胞的机制研究
[D].
Mechanism study of dengue virus type 3 infecting the human brain microvascular endothelial cells
[D].
Dengue fever ophthalmic manifestations: a review and update
[J].
Dengue eye disease
[J].