基因修饰小鼠在生命科学和医药学中的应用需求与日俱增[1-3]。小鼠在繁育过程中会出现由繁殖方案不合适、感染、疾病或自身品种品系因素等导致的生殖障碍,特别是一些特殊的基因敲除小鼠品系会出现繁殖力低下等问题[4-7]。对于仅存少量中老龄个体的小鼠品系,辅助生殖技术是挽救濒危小鼠品系的重要技术手段。常规的辅助生殖技术包括体外受精(in vitro fertilization,IVF)[8]、卵胞质内单精子注射(intracytoplasmic sperm injection,ICSI)[9]、胚胎移植(embryo transfer,ET)[10]和卵巢移植[11]等。本文总结分析浙江大学实验动物中心小鼠生物净化团队在2020年12月至2024年3月间,利用辅助生殖技术开展基因修饰小鼠品系挽救工作的成功实例,为同行挽救中老龄、濒危的基因修饰小鼠品系提供技术参考。
1 材料与方法
1.1 实验动物
中老龄的雄性不育基因修饰小鼠28种品系,共31只,9~18月龄;同品系的青年基因修饰可育雄性小鼠各1只,共28只,3~6月龄,作为中老龄组的对照组。雄性小鼠均由浙江大学各个课题组提供,品系背景为C57BL/6J,用于IVF-ET法挽救基因修饰小鼠品系。
用于体外受精、收集受精卵的SPF级3~4周龄C57BL/6J雌性小鼠,用于代孕的SPF级6~8周龄ICR雌性小鼠,用于制备假孕雌性小鼠的SPF级6~8周龄ICR雄性小鼠,均购自上海斯莱克实验动物有限责任公司[SCXK(沪)2017-0005]和江苏集萃药康生物科技股份有限公司[SCXK(苏)2018-0008]。其中ICR雄性小鼠在屏障环境内适应性饲养1周后进行输精管结扎手术。
不孕的基因修饰雌性小鼠12种品系,共18只,8~18月龄,由浙江大学各个课题组提供,品系背景为C57BL/6J。SPF级6周龄C57BL/6J卵巢受体雌性小鼠购自江苏集萃药康生物科技股份有限公司[SCXK(苏)2018-0008],用于卵巢移植技术挽救基因修饰小鼠品系。
所有小鼠均饲养在浙江大学实验动物中心屏障环境[SYXK(浙)2018-0016]的独立通风饲养笼盒内。雄性小鼠单笼饲养,同基因型雌性小鼠每笼5只饲养。小鼠可自由饮食饮水。饲养间内温度为22~24 ℃,相对湿度为40%~70%,光照周期为12 h/12 h明暗交替。所有实验方案经浙江大学实验动物福利与伦理委员会审核批准(批准号分别为ZJU20220403、ZJU20230022)。所有实验严格依照实验动物福利的“3R”原则进行,并在动物饲养与实验过程中予以人道关怀。
1.2 体外受精-胚胎移植技术
主要技术流程为雌性小鼠超数排卵及卵子团的收集、雄性小鼠精子团的采集、体外受精、胚胎移植假孕雌性小鼠的准备、2-细胞期胚胎的清洗和移植以及仔鼠的基因型鉴定。
图1
图1
雄性小鼠采集精子团及获能1 h后的精子状态
Figure 1
Sperm masses collected from male mice and sperm status after 1 h of capacitation
1.3 卵巢原位移植技术
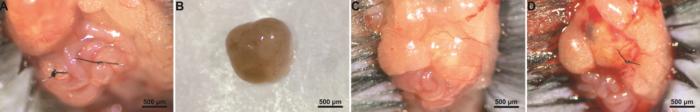
受体雌性小鼠单侧输卵管结扎:依据供体雌性小鼠卵巢数量及重量,麻醉相应数量的受体雌性小鼠,固定卵巢、输卵管和子宫的方法同胚胎移植,用非吸收缝线(10-0)分别在输卵管两处进行结扎,并用眼科角膜剪小心离断结扎点之间的输卵管(图2A)。然后将卵巢、输卵管和子宫放入小鼠腹腔,分别缝合肌肉层和皮肤。
图2
图2
小鼠卵巢移植手术
Figure 2
Ovarian transplantation surgery in mice
分离供体小鼠卵巢:将供体小鼠腹腔注射1.25%阿佛丁(美国Sigma-Aldrich公司,货号T48402-5G)麻醉,备皮并消毒皮肤,分层剪开腹部皮肤和腹壁肌肉层,分离出双侧卵巢并称重记录(图2B)。迅速将供体卵巢放入37 ℃预热的M2培养液(美国Sigma-Aldrich公司,货号M7167)中清洗,待移植。
受体雌性小鼠自体对侧卵巢摘除:在受体小鼠另一侧以同样的方式固定卵巢、输卵管和子宫(图2C),在输卵管伞口对侧的卵巢囊膜上剪开一个适度大小的切口,将自体卵巢从囊膜中小心剥离出来,并用眼科角膜剪剪断卵巢蒂,摘除完整的卵巢。
供体卵巢原位移植:根据供体卵巢重量和大小,将完整或1/2卵巢轻轻放入受体小鼠已去除自体卵巢的卵巢囊膜内,用缝线(10-0)将卵巢囊膜缝合(图2D),将植入卵巢、输卵管和子宫放回小鼠腹腔,逐层缝合肌肉层和皮肤。
受体雌性小鼠合笼繁育:术后将受体雌性小鼠放置在37 ℃保温毯上直至苏醒,雌性小鼠饲喂实验鼠生长繁殖饲料(江苏省协同医药生物工程有限责任公司,货号XTI01FZ-010),并在笼中放置适量的高温高压灭菌过的做窝材料。待移植术后21 d按1∶1将其与同背景、8周龄野生型雄性小鼠合笼进行繁育。仔鼠出生后,进行基因型鉴定。统计自合笼之日至6个月内受体小鼠的生产情况,如有阳性子代小鼠存活,记为成功挽救的小鼠品系。
1.4 数据处理及统计
实验结果数据经Excel 2016软件整理,数据用均数±标准差表示,并以GraphPad Prism 8软件绘图。采用SPSS 16.0统计软件对结果进行单因素方差分析(ANOVA检验)和t检验,以P<0.05表示差异有统计学意义。采用SPSS 16.0中相关性分析程序,分析小鼠年龄与IVF受精率之间的关系,通过Pearson相关系数检验进行验证。当P<0.05时,为相关性显著;当P<0.01时,为相关性极显著。
各变量计算公式如下:经IVF-ET技术挽救小鼠成功率(%)=经IVF-ET技术获得阳性仔鼠的品系数/生殖障碍供精雄性小鼠品系总数×100;受精率(%)=2-细胞期胚胎数/(2-细胞期胚胎数+未受精卵数+异形卵子数)×100;异形卵率(%)=异形卵子数/(2-细胞期胚胎数+未受精卵数+异形卵子数)×100;仔鼠出生率(%)=出生仔鼠数/移植2-细胞期胚胎数×100;卵巢移植受体妊娠率(%)=卵巢移植后妊娠受体只数/卵巢移植后存活受体总数×100;卵巢移植受体活产率(%)=受体妊娠、产下活仔且仔鼠存活至离乳的受体只数/卵巢移植后存活受体总数×100;经卵巢移植挽救小鼠成功率(%)=经卵巢原位移植后获得阳性仔鼠的品系数/生殖障碍供卵小鼠品系总数×100。
2 结果
2.1 利用IVF-ET法挽救基因修饰小鼠品系的结果统计
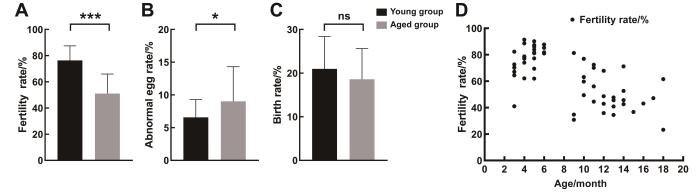
本研究中,生殖障碍供精雄性小鼠品系共28种,利用IVF-ET技术共挽救28种基因修饰小鼠品系,成功率100%。其中25种品系经一轮IVF-ET实验即成功获得阳性子代小鼠,首轮实验成功率为89.29%(25/28);另外3种品系通过两轮实验最终获得阳性子代小鼠,成功被挽救。不育基因修饰小鼠经IVF-ET的异形卵率、受精率及仔鼠出生率见表1。中老龄组平均受精率为(51.01±14.97)%(n=28,统计最终成功的28种品系28只雄性小鼠的数据,以下均同此),较青年组(76.37±11.16)%(n=28)有极显著性差异(P<0.001)(图3A);中老龄组异形卵率为(9.03±5.28)%(n=28),较青年组(6.57±2.71)%(n=28)有显著差异(P<0.05)(图3B);中老龄组仔鼠出生率(18.60±7.03)%(n=28)较青年组(20.96±7.44)%(n=28)略低,但差异无统计学意义(P>0.05)(图3C)。
表1
经体外受精-胚胎移植挽救的不育基因修饰小鼠的异形卵率、受精率及仔鼠出生率 (
Table 1
不育雄性小鼠月龄/月 Age of Infertile male mice/month | 动物数量 n | 异形卵率/% Abnormal egg rate/% | 受精率/% Fertility rate/% | 仔鼠出生率/% Birth rate/% |
|---|---|---|---|---|
| 9 | 3 | 4.35±2.21 | 48.99±28.09 | 19.87±13.93 |
| 10 | 4 | 11.55±8.29 | 62.34±11.32 | 16.84±5.43 |
| 11 | 4 | 9.38±2.35 | 60.85±10.46 | 17.41±10.46 |
| 12 | 4 | 7.14±1.12 | 48.87±13.72 | 19.04±5.31 |
| 13 | 4 | 9.50±6.44 | 42.21±5.86 | 19.68±1.92 |
| 14 | 4 | 13.15±7.72 | 53.07±12.79 | 16.51±4.60 |
| 15 | 1 | 6.13 | 36.79 | 12.82 |
| 16 | 1 | 5.04 | 43.17 | 15.00 |
| 17 | 1 | 9.09 | 47.20 | 20.00 |
| 18 | 2 | 8.31±3.53 | 42.45±27.12 | 27.66±10.50 |
图3
图3
青年组与中老龄组受精率、异形卵率和仔鼠出生率的比较
Figure 3
Comparison between the young group and the middle-aged and aged group in their fertility rates, abnormal egg rates, and birth rates
通过SPSS 16.0软件分析得出:IVF受精率与供精雄性小鼠年龄呈极显著负相关(P<0.01),相关系数为-0.682,提示随着雄性小鼠日龄增长,IVF受精率呈下降趋势(图3D);异形卵率与供精雄性小鼠年龄呈正相关,相关系数为0.214,但相关性无统计学意义(P>0.1);仔鼠出生率与供精雄性小鼠年龄呈负相关,相关系数为-0.203,其相关性同样无统计学意义(P>0.1)。
统计自雌性小鼠注射第一针孕马血清促性腺激素(pregnant mare serum gonadotropin,PMSG)(宁波三生生物科技股份有限公司,兽药字110914564,1 000 U/瓶冻干粉)之日(记为第1天)至仔鼠出生的时间,IVF-ET技术平均获得仔鼠时间为(25.79±7.56)d(n=28)。除3种品系经两轮IVF实验获得仔鼠所需时间分别为41 d、43 d和55 d外,其余品系自IVF之日(19~21)d仔鼠即出生。
2.2 利用卵巢移植技术挽救基因修饰小鼠品系的结果统计
采用卵巢原位移植技术将12种基因修饰小鼠品系共18只老龄雌性小鼠的单/双侧卵巢移植入40只受体小鼠体内。供体小鼠左侧卵巢平均重量(3.19±1.20)mg(n=16,18只老龄雌性小鼠中有2只鼠的左侧卵巢有囊肿,弃用;取剩余16只雌性小鼠的左侧卵巢),右侧卵巢平均重量(4.06±1.76)mg(n=18,取18只老龄雌性小鼠的右侧卵巢)。
术后除1只受体雌性小鼠死亡外,其余39只均存活,并于术后21 d开始与8周龄野生型C57BL/6J雄性小鼠合笼。合笼后,仅13只受体雌性小鼠妊娠并生产,卵巢移植受体妊娠率为33.33%(13/39),其中7只受体雌性小鼠产下活仔且仔鼠存活至离乳,卵巢移植后受体活产率为17.95%(7/39)。统计自合笼日(记为第1天)至首窝仔鼠出生时间,平均为(88.92±36.60)d(n=13,统计13只妊娠雌性小鼠的数据)。综上,经卵巢移植技术共挽救老龄基因修饰小鼠品系4种,供体雌性小鼠月龄分别为10月龄、15月龄、15月龄和18月龄,妊娠率及活产率见表2。经卵巢移植技术挽救基因修饰小鼠成功率为33.33%(4/12)。
表2 经卵巢移植成功挽救的不育基因修饰小鼠的供体小鼠月龄、妊娠率和活产率
Table 2
供体雌性小鼠月龄/月 Age of donor mice/month | 左侧卵巢移植的受体小鼠数/只 The number of recipients for donor’s left ovarian transplantation | 右侧卵巢移植的受体小鼠数/只 The number of recipients for donor’s right ovarian transplantation | 妊娠率/% Pregnancy rate/% | 活产率/% Live birth rate/% |
|---|---|---|---|---|
| 10 | 1 | 1 | 100.00 (2/2) | 100.00 (2/2) |
| 15 | 1 | 1 | 50.00 (1/2) | 100.00 (1/1) |
| 15 | 1 | 2 | 66.67 (2/3) | 100.00 (2/2) |
| 18 | 1 | 1 | 100.00 (2/2) | 100.00 (2/2) |
3 讨论
超过6~8月龄的基因修饰小鼠可能由于多种原因出现繁殖障碍,如亲本小鼠更新不及时、繁殖小鼠过晚配繁、繁殖笼内雌性小鼠年龄过大等[14-16],或同时合并多种因素,如亲本小鼠老龄且患病,或特殊品种品系的低繁殖力等。多重因素的叠加会增加辅助生殖技术的难度,同时品系丢失的风险也随之增大。本研究观察到,不育基因修饰雄性小鼠虽然异形卵率较青年组有显著差异,提示精子质量随年龄增大而下降,且体外受精的胚胎发育率较适龄雄性小鼠显著降低,但大部分仍可通过常规IVF-ET技术获得阳性子代。IVF体系的稳定性至关重要,在开展实验前应确保各批次试剂及实验条件均已通过预实验测试,且在正式实验中不随意更改实验参数。值得注意的是,一定要选择3~4周龄的雌性小鼠(不少于5只)进行一轮IVF实验,因为若促排卵雌性小鼠年龄过大或数量太少,将无法保证获取足够多的卵细胞,加之不育雄性小鼠的精子质量不可控,易最终导致实验失败。对于仅剩1~2只雄性小鼠的品系,建议麻醉雄性小鼠采集单侧附睾尾中精子团进行体外受精,如最终获得子代小鼠数量太少,可择日取该雄性小鼠另一侧附睾尾再进行一轮IVF-ET实验。对于无法通过常规体外受精获得足够多2-细胞期胚胎的不育雄性小鼠,可采用ICSI技术,但需要较高的成本投入,技术门槛也更高,所以建议优先选择IVF-ET技术[17]。
卵巢内卵泡的发育受下丘脑-垂体-卵巢轴的调控[18]。神经内分泌功能障碍、卵泡储备下降和老龄雌性卵巢分泌物均能导致生殖功能下降[19],因此雌性小鼠的最适繁育年龄段较雄性小鼠更短,一旦配种不及时,易出现生殖障碍而导致该品系丢失。以往国内文献有关小鼠卵巢移植的研究,供体雌性小鼠多为新生小鼠或适龄小鼠[20-21],而对于老龄雌性小鼠卵巢移植的研究鲜有报告。2009年,Niikura等[22]研究表明,老龄雌性小鼠的卵巢组织中仍存在极少量减数分裂前的生殖细胞,将20月龄雌性小鼠的卵巢移植入2月龄雌性小鼠卵巢囊膜中,老龄雌性小鼠卵巢内休眠的干细胞仍能被重新激活并产生卵母细胞,但这些卵母细胞是否具备受精能力并能由受体小鼠产出活体小鼠,该研究并未深入探索。本研究发现18月龄不孕雌性小鼠的卵巢经原位移植到年轻雌性小鼠体内后,不但能定植、产生卵母细胞,且能正常受精并活产小鼠至离乳。
通过对比郁丽丽等[20]的研究结果,同为C57BL/6J背景的小鼠,经卵巢原位异体移植后,10日龄的供体小鼠可获得最高移植后妊娠率,为100%(n=5);20日龄供体小鼠移植后妊娠率为60%(n=5);4周龄供体小鼠移植后妊娠率仅为40%(n=5)。左琴等[21]将10日龄C57BL/6J雌性小鼠的新鲜卵巢原位移植到4周龄C57BL/6J雌性小鼠体内,妊娠率为80%(n=5)。以上研究结果均显示,卵巢移植成功率与供体小鼠的年龄呈负相关[20-21]。裴承斌等[23]将6~8周龄ICR雌性小鼠的卵巢原位异体移植120 h后腹腔注射10 U/只PMSG,48 h后取出卵巢组织,经切片、HE染色后观察卵泡形态并作分类计数。与对照组(未做卵巢移植的6~8周龄ICR雌性小鼠)相比,移植后卵巢内的次级卵泡数和窦卵泡数均低于对照组(n=6,P<0.05)。此结果也与李宇彬等[24]的研究结果一致,提示即使对于较为年轻的雌性小鼠,卵巢原位移植操作仍可能造成一定程度的生育力损失。本研究也观察到,老龄雌性小鼠卵巢移植后活产率并不高,可能与供体小鼠年龄较大,其卵巢储备很可能已近衰竭有关。已有研究报告表明,卵巢组织经分离、切割和移植后,机械损伤和缺血性损伤会导致原卵巢组织中大量卵泡的丢失[25-26],这可能是影响本研究中卵巢移植后受体雌性小鼠活产率的重要原因。卵巢移植技术的关键在于受体和供体小鼠必须具备组织相容性,否则,供体卵巢将因排异而坏死,从而导致移植失败;因此,一般建议使用裸小鼠、NSG等免疫缺陷小鼠作为供体小鼠[11]。本研究选择使用与供体小鼠同遗传背景的C57BL/6J小鼠。
以往的研究中,卵巢原位移植为多采用摘取受体双侧卵巢,并移植供体双侧卵巢的方法,且多将供体卵巢放入卵巢囊膜后即将其回纳入腹腔[20-21,27]。此方法不需要缝合卵巢囊膜,操作更简便且用时更短,但弊端是移植后的供体卵巢组织容易从囊膜内滑出,或者由于术后移植卵巢不能被很好地固定,影响血供和血管重建,最终导致移植失败。李茗薇等[27]在C57BL/6J雌性小鼠卵巢原位移植术后35 d观察卵巢组织形态学,发现有10%的卵巢消失,40%的卵巢萎缩,推测这是由于卵巢囊膜无法将游离的供体卵巢组织固定于原位,小鼠在活动中卵巢组织滑脱或血供不足引起萎缩所致。因此,针对老龄不孕供体小鼠,本研究优化了卵巢原位移植术,即结扎并离断一侧输卵管,摘除另一侧卵巢并移植供体卵巢的方法,保留受体小鼠的一侧卵巢正常分泌激素的功能,以帮助受体小鼠在卵巢移植后快速建立下丘脑-垂体-卵巢轴功能,促进卵母细胞成熟。同时,本研究还优化了手术细节,即缝合卵巢囊膜,此法可避免供体卵巢从囊膜中滑出,有助于供体卵巢的定植和移植后的血管重建。手术过程中的要点包括:卵巢囊膜的开口不宜过大,移除受体卵巢时应注意不要剪破卵巢蒂底部的卵巢囊膜,否则易致供体卵巢滑脱;由于卵巢囊膜很薄,缝线点不宜与切口边缘过近,打结不宜过紧,以防止缝线从囊膜上拉脱;应选择粗细适中的手术缝合线,建议用10-0手术缝合线,视卵巢囊膜的切口大小缝合1~2针。
综上所述,本研究证实,对于具有明显生殖障碍表型的基因修饰小鼠可以通过IVF-ET技术和卵巢移植技术等辅助生殖技术进行品系挽救。此外,相较于IVF-ET技术,卵巢移植技术获得子代时间较长且时间不可控,对操作人员的手法精准度和熟练程度要求较高,且成功率相对较低,可应用于在仅剩不孕中老龄雌性小鼠或珍贵雌性小鼠突然死亡的情况下,也可作为IVF-ET技术挽救濒危基因修饰小鼠品系的技术补充。
[引用本文]
王芊芊, 陶斯珏, 卫振, 等. 利用辅助生殖技术挽救基因修饰小鼠的实例分析[J]. 实验动物与比较医学, 2025, 45(1): 79-86. DOI: 10.12300/j.issn.1674-5817.2024.107.
WANG Q Q, TAO S J, WEI Z, et al. A case study of using assisted reproductive technology to rescue genetically modified mice with reproductive disorder phenotypes[J]. Lab Anim Comp Med, 2025, 45(1): 79-86. DOI: 10.12300/j.issn.1674-5817.2024.107.
医学伦理声明
本研究涉及的所有动物实验均已通过浙江大学实验动物福利与伦理委员会审批(批准号:ZJU20220403;ZJU20230022)。所有实验过程均遵照中国实验动物相关法律法规条例要求进行。
Medical Ethics Statement
All animal experiments involved in this study were approved by the Laboratory Animal Welfare and Ethics Committee of Zhejiang University (Approval number: ZJU20220403; ZJU20230022). All experimental procedures were conducted in compliance with the requirements of Chinese laws and regulations related to laboratory animals.
作者贡献声明
王芊芊负责资助项目申请、研究方案策划、实验设计、实验数据统计和初稿写作;
陶斯珏、卫振负责实验数据处理和分析,图表制作;
金晖晖负责所有实验小鼠的饲养繁育和生产数据统计;
刘平负责部分小鼠体外受精和胚胎移植实验,以及实验试剂配制;
汪洌负责项目管理和修改文稿。
利益冲突声明
所有作者声明不存在利益冲突。
参考文献
A brief history of use of animals in biomedical research and perspective on non-animal alternatives
[J].
转基因技术和转基因动物的发展与应用
[J].
The development and application of transgenic technology and transgenic animals
[J].
The application of transgenic and gene knockout mice in the study of gastric precancerous lesions
[J].
Loss of TDP-43 in male germ cells causes meiotic failure and impairs fertility in mice
[J].
AKR7A5基因敲除对雄性小鼠生殖的影响
[J].
Effects of AKR7A5 gene knockout on reproduction of male mouse
[J].
LSS基因功能缺失对雄性小鼠生殖的影响
[J].
The effects of knockout of LSS on female mice fertility
[J].
DRD1基因敲除影响雄性生育的分子机理研究
[J].
Study on molecular mechanism of male mice reproduction in DRD1 knockout
[J].
In vitro fertilization in mice
[J].
Improving the generation of genomic-type transgenic mice by ICSI
[J].
Embryo transfer surgery
[J].
Mouse ovary transplantation
[J].
精子数量对小鼠体外受精与胚胎早期发育的影响
[J].
Effects of sperm counts on in vitro fertilization and early embryonic development of mice
[J].
小鼠生物净化技术平台的设计、运行及维护
[J].
Design, operation, and maintenance of the technology platform of mouse rederivation
[J].
SPF级C57BL/6J小鼠生长发育和繁殖性能指标的测定
[J].
Characterization of growth and reproductive performance in SPF C57BL/6J mice
[J].
6种常用SPF级大小鼠繁殖性能测定与分析
[J].
Measurement and analysis of the reproductive performance in six commonly used SPF mice and rats
[J].
胎间隔和交配间隔时间对昆明小鼠繁殖性能的影响
[J].
Effects of fetal interval and mating interval on reproductive performance in KM mice
[J].
濒危基因编辑小鼠品系拯救技术及其应用探讨
[J].
Rescue technology and its application of endangered gene-edited mice
[J].
The ovary: basic biology and clinical implications
[J].
Aging of the hypothalamo-pituitary-ovarian axis: hormonal influences and cellular mechanisms
[J].
同品系小鼠卵巢移植方法的建立
[J].
Established a method of ovarian heterotopically transplantation in same strain
[J].
遗传工程小鼠冻存卵巢异体原位移植比较研究
[J].
Study for cryopreservation and orthotopic transplantation of genetically engineering mice ovary
[J].
Aged mouse ovaries possess rare premeiotic germ cells that can generate oocytes following transplantation into a young host environment
[J].
小鼠卵巢异体不同部位无血管吻合移植后的血管重建及对促性腺激素的反应
[J].
Vascular remodeling and response to gonadotropin in different parts of transplantation in mice without vascular anastomosis
[J].
去势手术方式对小鼠卵巢组织自体皮下移植效果的影响
[J].
Influence of castration methods on the subcutaneous auto- transplantation of mouse ovaria
[J].
Follicle activation is a significant and immediate cause of follicle loss after ovarian tissue transplantation
[J].
FERTILITY PRESERVATION: Follicle reserve loss in ovarian tissue transplantation
[J].