生殖毒性研究是药物临床前安全性评价的重要内容之一,主要是通过动物试验反映受试物对哺乳动物生殖功能和发育过程的影响,预测其对亲代生殖机能、子代胚胎-胎儿发育以及出生后胎儿发育的潜在不良影响[1]。
一般情况下,可根据受试物选择合适的动物进行毒理学研究,常用的哺乳动物包括大鼠、家兔、食蟹猴、犬、小型猪等[1]。在非临床生殖毒性试验中,无论研究对象是亲代动物还是子代动物,首先要确保亲代动物可成功交配。但在试验过程中,除受试物可能有的毒性干扰外,运输应激、环境改变、营养状况、性成熟和动情周期掌握不准确等因素也常导致动物的交配成功率低,这也是研究者和技术人员常面临的难题,本文就其中的部分难点及应对策略进行总结分析,以供同行交流与探讨。
1 大鼠假孕及其动情周期鉴定
利用啮齿类动物开展生殖毒性研究时,一般首选大鼠,其次是小鼠。大鼠发育快,性成熟早。雄性大鼠出生后第30~35天,睾丸降入阴囊,约14 d后可产生精子,60 d左右即达性成熟,90 d左右达体成熟。雌性大鼠一般在阴道开口后初次排卵,80 d左右达到体成熟。雌性大鼠自发排卵,动情周期为4~5 d,根据阴道涂片的细胞类型变化,分为动情前期、动情期、动情后期和间情期4个阶段。雌性大鼠是常年多动情动物。当雌性大鼠在没有雄性大鼠的环境中群养时,其动情周期可被抑制。而当雌性大鼠与雄性大鼠混养或接触雄性大鼠的排泄物时,可被诱导进入动情期[2]。另外,相关文献表明,当雌性大鼠进入围绝经期后,其动情周期也可能有所延长[3]。
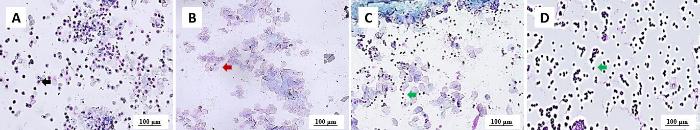
在大鼠生殖毒性试验中,假孕是最常见的问题,一般可以通过阴道涂片和孕中期触诊等方式诊断动物是否受孕。本机构的实验操作人员,在工作期间将大鼠阴道涂片进行HE染色并在镜下进行观察。阴道涂片如图1A~D所示,动物阴道分泌物中的细胞主要有红细胞、白细胞、有核上皮细胞和无核角化细胞等,与先前研究一致[4]。当雌性大鼠处于动情前期时,可以观察到阴道涂片一般以有核上皮细胞为主(图1A);而雌性大鼠处于动情期时,角化上皮细胞呈落叶状堆积(图1B);若观察到阴道涂片清亮并且上皮细胞数量较少时,雌性大鼠可能处于动情后期和间情期(图1C~D)。根据阴道涂片观察到的细胞类型来确定雌性大鼠动情周期的方法操作简单,容易掌握,且鉴定结果较为准确,相比于其他鉴定方法优势更大。因此,目前该方法在国内外得到了广泛的应用。
图1
图1
成年雌性大鼠动情周期各阶段的典型阴道组织涂片
Figure 1
Typical vaginal smear characteristics from adult female rats at each stage of estrous cycle
2 家兔的发情和常见诱导发情的方式
利用非啮齿类动物开展生殖毒性研究一般选择家兔。家兔的性成熟时间因其品种而异。大型兔比如比利时兔、哈白兔和塞北兔等,它们的性成熟年龄约在5~6月龄,初配年龄为6~7月龄,初配体重须达到3.5 kg;而中型兔如新西兰白兔、加利福尼亚兔和日本大耳白兔等,它们性成熟较早,约在4~5月龄,初配年龄为5~6月龄,初配体重须达到3 kg;小型兔如荷兰兔、中国白兔等,它们性成熟更早,约在3~4月龄,建议4~5月龄进行初配,体重须达到2.5~3 kg[10]。由此可见,不同品种家兔性成熟、体成熟及初配体重等繁殖指标存在明显差异,应选择合适年龄和体重的家兔进行生殖毒性试验。
在药物非临床安全性评价中,一般选用中型兔如新西兰白兔进行研究。雌兔属于诱发性排卵动物,交配后10~12 h排卵。雄兔无固定动情周期,全年具备交配能力。与雄兔不同的是,雌兔在发情阶段可出现性欲活跃期,一般表现为活跃、不安、少食,外阴稍有肿胀、潮红等情况[11],所以一般可通过观察外阴的肿胀程度判定雌兔的发情情况。
家兔试验中常见的问题有雌兔不发情和假孕。虽然家兔自然交配的配怀率较高[12],但在封闭的实验动物设施内,由于多因素的影响,用于生殖毒性研究的家兔配怀率往往不稳定,主要表现为动物不发情、不同批次间动物发情情况差异大、动物交配失败等。雌兔不发情与其体内激素水平密切相关,这是导致同批次雌兔发情不稳定的主要原因之一[13]。当雌兔和雄兔在不同的饲养间或间隔较远时,由于外激素的传递受限,雌兔不容易发情。当改变饲养位置(雌兔和雄兔邻近饲养),该情况可以得到改善。除了外激素外,雌兔体内性激素的调节往往也直接影响它们的发情,其中雌激素与孕激素为雌兔发情周期的重要调控因素之一,它们对雌兔的卵泡发育、卵子发生与胚胎发育等均具有重要影响[14]。而性激素的分泌和昼夜节律密切相关,通过人工调整光照影响节律,刺激下丘脑中促性腺激素释放激素(gonadotropin-releasing hormone,GnRH)的释放,雌兔的发情状况往往得以改善。
除此之外,增加饲料中蛋白质的含量(即氮元素的摄入)也能促进雌兔发情,其原因可分为两方面:一方面,蛋白质可以提供合成性激素所需的氨基酸,促进性激素的合成;另一方面,蛋白质的摄入也可以刺激动物体内的代谢活动,如神经肽利尿激素通过脑-肠轴调节刺激动物发情[16]。在实验室饲养工作中,虽然常规的生长繁殖饲料的营养配比已经满足拟交配动物的生理需求,但不同机构使用的商品化颗粒饲料的营养成分可能存在差异,为了避免新入室动物因突然更换饲料而引发应激,建议按照一定的比例(如3∶1、1∶1、1∶3)进行饲料过渡。经过兽医或相关试验责任人评估许可后,可按需供给干草,如提摩西干草或苜蓿草等,该方法既能增加饲料的适口性,还能提高动物粗蛋白的摄入[17]。
家兔在不同生理阶段的营养需求有所不同,应选择合适的饲喂量以满足家兔的需求。雌兔在不同生理阶段的饲喂方式有所差异。按照一天一次的饲喂频率,空怀期建议饲喂量为每只每次约200 g,并额外增加5%~10%的粗蛋白含量。妊娠前期饲喂频率和饲喂量仍和空怀期一致;当动物处于妊娠中期和妊娠后期时,保持一天一次饲喂频率的同时,饲喂量提高至每只每次220~260 g。同样,经过兽医或相关试验责任人评估许可后,针对妊娠前、中和后期的动物,可额外增加3%~5%含量的粗蛋白[10]。除此之外,可考虑除常规饲料中蛋白的摄入外,额外增加蛋白的饲喂,如黄豆等植物蛋白。但该方法可能会增加动物消化道负担,引起肠道问题,应结合动物的健康情况评估后谨慎实施。但要注意,家兔对于环境的改变较为敏感,雌兔体质较弱,日粮蛋白质应控制在17%~18%[18]。
3 非人灵长类动物的性成熟和妊娠鉴定
非人灵长类动物围青春期发生在2.5~5.5岁的年龄范围内,其年龄跨度较大,并且性成熟时期动物的年龄以及体重之间都显示出巨大的个体差异[23]。对55只性成熟食蟹猴的体重进行统计发现,其体重范围为2.3~6.3 kg[24]。灵长类动物体重和性成熟状态无显著的相关性,主要原因是其幼年时体内的神经肽Y和γ-氨基丁酸(γ-aminobutyric acid,GABA)对性腺轴中GnRH的抑制性调控作用[25],使动物出生后体内的GnRH分泌呈现 “up-down-up”的模式,经历了漫长的生殖轴静止期[26]。因此,通过单一指标如年龄、体重、齿式和供应商记录等信息来判定灵长类动物是否性成熟通常不可靠。
一般可以从有规律的月经出血来判定雌性非人灵长类动物性成熟,但月经初潮并不能单独作为判定其是否性成熟的依据。在实际操作过程中,由于动物经期出血时间可能较短,需要通过每天采集阴道拭子来进行监测,当连续监测到2 d及以上的出血,并且在至少间隔20 d后能够再次观察到出血时,说明雌性非人灵长类动物达到性成熟水平。
除此之外,有文献显示非人灵长类动物性成熟前后的肠道微生物群组成、代谢物谱和基因表达有显著性差异。雄性猕猴中参与精子发生的基因(如TSSK2、HSP90AA1、SOX5、SPAG16和SPATC1)显著上调,表明性成熟的雄性动物具有更强的精子活力。而在雌性猕猴中,性成熟前后的差异大部分与色氨酸代谢有关,如吲哚-3-乙酸和吲哚乙醛的水平发生显著变化,表明性成熟的雌性非人灵长类动物表现出更强的神经调节和肠道免疫力[29]。
其次,非人灵长类动物的交配及交配确认也是生殖毒性试验过程中的难点之一。非人灵长类动物在生产环境下,一般采用雄∶雌=1∶6或1∶8的比例进行繁殖生产,动物的交配成功率一般可控制在79.86%左右[32]。但在试验环境下,因为干预了动物自然交配的模式,并且动物的性情、交配的空间以及合笼的时间等因素都比较随机,所以动物交配行为的发生往往也比较随机。若采用1∶1的比例进行交配,会增大交配成功的难度。
一般情况下,在试验开始前,会将雌性和雄性非人灵长类动物饲养在同一空间内进行适应性饲养,并保证它们能够进行视觉、听觉甚至肢体接触的交流,一定程度上能避免出现合笼后动物不相容的情况;合笼后,选择空间较大的笼具,同时增加环境丰容措施,并提供安静的环境,能提高它们交配成功的概率。
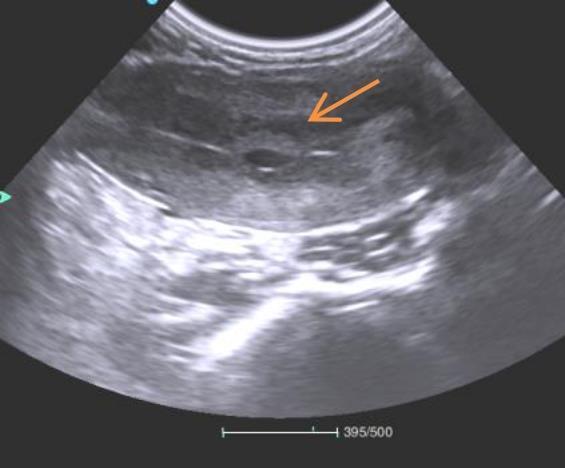
另外,非人灵长类动物的交配行为并不能像家兔和大鼠一样容易被观察到,对于试验过程中它们是否成功交配也成为该类试验开展过程中的技术难点之一。实际操作过程中,在雌猴月经开始后的11~15 d,将雌性和雄性非人灵长类动物1∶1合笼,可设定3 d的交配期,在交配期后的20~25 d进行B超诊断。本机构兽医在食蟹猴妊娠早期,通过B超检查方式发现如图2所示的孕囊结构。可通过观察非人灵长类动物有无明显孕囊来判断其是否妊娠,但这需要经验丰富的临床兽医制定完善的B超检查方法。
图2
图2
妊娠初期雌猴孕囊B超切面
Figure 2
Ultrasound cross-sectional view of gestational sac in a female monkey during early pregnancy
除此之外,还可以通过雌性动物体内性激素的变化水平来推测动物的妊娠阶段。但需要特别注意的是,当通过性激素水平来评估动物的妊娠阶段时,需要同时考虑采样方式和环境温度等因素对激素的合成或释放的影响。另外,对动物进行频繁地采血也可能会造成孕猴应激。
4 讨论和总结
生殖毒性研究是药物非临床安全性评价的重要内容,它与急性毒性、长期毒性、遗传毒性等毒理学研究有着密切的联系。然而不同国家的相关法规标准存在差异,对于动物妊娠的管理要求各不相同,这常导致生殖毒性试验的开展面临诸多困难。本文围绕药物非临床生殖毒性试验动物妊娠环节中存在的难点和改善措施展开讨论。
大鼠可应用于生育力评估与早期胚胎发育毒性试验(Ⅰ段)、胚胎-胎仔发育毒性试验(Ⅱ段)和围产期毒性试验(Ⅲ段),试验中一般采用一雌一雄合笼的方式实现交配,次日通过阴道栓检查判断是否发生交配行为,以准确记录妊娠时间,但该种方式会增加雄性大鼠的使用数量或延长试验周期,且无法改善雌性大鼠假孕的情况。根据阴道涂片观察到的细胞类型来明确雌性大鼠动情周期,有效筛查大鼠动情情况,提高大鼠妊娠率。
家兔一般应用于胚胎-胎仔发育毒性试验(Ⅱ段),通过雄性家兔和处于发情期的雌性家兔合笼后发生交配行为,判断受孕时间。试验中常出现雌性家兔发情不典型、不同批次家兔间发情情况差异大、动物交配失败等问题,可通过延长光照时间、增加蛋白质摄入、选择合适的交配方式、改变饲养环境(雌兔和雄兔邻近饲养)等方式改善家兔的发情情况,提升家兔的交配成功率。但家兔的发情率提升并不意味着家兔交配的成功率增加,还需根据实际情况进行综合分析。
非人灵长类动物一般应用于围产期毒性试验(Ⅲ段),可通过综合评估动物年龄、体重和睾丸体积等指标综合判断雄性非人灵长类动物是否性成熟,一般年龄在4.5岁以上,体重大于4.5 kg,单侧睾丸体积超过10 mL,双侧睾丸总体积大于20 mL的雄性猕猴预示着性成熟。可通过超声检查是否能观察到明显孕囊或通过雌性动物体内性激素水平的变化来推测雌性非人灵长类动物的妊娠阶段,但需考虑采样方式和环境温度对激素合成或释放的影响。另外,建议选择非人灵长类动物的自然交配繁殖旺季7~12月开展试验。
引用本文
刘鹍, 兰青, 易兵, 等. 药物非临床生殖毒性试验中动物妊娠的主要难点及应对方法[J]. 实验动物与比较医学, 2025, 45(4): 449-456. DOI:10.12300/j.issn.1674-5817.2024.177.
LIU K, LAN Q, YI B, et al. Key challenges and mitigation strategies for animal pregnancy in non-clinical reproductive toxicity testing of drugs[J]. Lab Anim Comp Med, 2025, 45(4): 449-456. DOI: 10.12300/j.issn.1674-5817.2024.177.
作者贡献声明
刘鹍负责初稿写作(含制作图1~2)与文章修改;
兰青参与文稿写作;
易兵负责文献收集及整理;
谢晓婕负责文章构思设计。
利益冲突声明
所有作者声明不存在利益冲突。
参考文献
生殖毒理学研究动物模型的建立方法及应用评价
[J].
Establishment methods and application evaluation of animal models in reproductive toxicology research
[J].
SD大鼠毒性试验生殖指标参考值建立及不同体重大鼠孕后生殖指标分析
[J].
Establishment of reference value for reproductive index in SD rats toxicity test and analysis of post-pregnancy reproductive index in rats of different body weights
[J].
围绝经期大鼠动情周期变化的研究
[J].
Changes of estrous cycle of perimenopausal rats
[J].
不同阴道涂片方法的比较及对大鼠动情周期的判断
[J].
Comparison of different vaginal smears and judgment of estrous cycle in rats
[J].
大鼠阴道细胞涂片技术及其HE染色方法的研究
[J].
Study on smear technique and HE staining of rat vaginal cells
[J].
阴道分泌物在动物发情鉴定中的研究进展
[J].
Research progress of vaginal secretions in animal estrus identification
[J].
雄性大鼠性动机的检测方法与评价指标研究进展
[J].
Detection methods and evaluation indexes of sexual motivation in male rats: an update
[J].
性成熟雌性SD大鼠动情周期的观察
[J].
Observation of the estrous cycle in sexually mature female sd rats
[J].
大鼠发情周期各阶段的阴道细胞变化观察
[J].
Observation on the vaginal smear photographs for each stage of estrus cycle in rats
[J].
兔生殖毒性评价试验中动物的选择及饲养管理要求
[C].
Animal selection and husbandry requirements in rabbit reproductive toxicity evaluation tests
[C].
家兔生殖生理特点与提高繁殖力措施
[J].
Reproductive physiological characteristics of rabbits and measures to improve their fertility
[J].
临床促进杂交母兔发情受孕实用技巧
[J].
Practical skills of promoting estrus pregnancy of hybrid female rabbits in clinic
[J].
不同光源对闽西南黑母兔发情及激素GnRH水平影响
[J].
Effect of different light sources on estrus and GnRH level of female black rabbit in southwest Fujian
[J].
高原鼠兔发情周期性激素与性器官变化特征
[J].
Characteristics of sex hormone level and sex organ histology in estrus cycle of plateau pika(Ochotona curzoniae)
[J].
LED单色光对兔行为及同期发情影响的机理研究
[J].
Effects of different LED light colors on estrus synchronization of rabbits and their molecular regulation mechanism through retina-pineal gland pathway
[J].
A nutrient-specific gut hormone arbitrates between courtship and feeding
[J].
实验用新西兰兔压力水平的探究
[J].
Preliminary exploration of pressure level in experimental New Zealand rabbits
[J].
秋季种母兔管理要点
[J].
Key management points for breeding rabbits in autumn
[J].
如何成功开展药物非临床生殖毒性试验
[J].
How to successfully carry out non-clinical reproductive toxicity study on new drugs
[J].
人工授精对母兔繁殖性能的影响
[J].
Effect of artificial insemination on reproductive performance of female rabbits
[J].
非人灵长类动物模型在女性不孕症研究中的运用
[J].
The use of non-human primate models in female infertility research
[J].
重庆地区雌性恒河猴生殖生理的季节性变化
[J].
Seasonal changes of reproductive physiology in female Rhesus monkey in Chongqing
[J].
Functional assessment of sexual maturity in male macaques (Macaca fascicularis)
[J].
A simple orchidometric method for the preliminary assessment of maturity status in male Cynomolgus monkeys (Macaca fascicularis) used for nonclinical safety studies
[J].
Neurobiological bases underlying the control of the onset of puberty in the Rhesus monkey: a representative higher primate
[J].
Kisspeptin and the regulation of the hypothalamic–pituitary–gonadal axis in the Rhesus monkey (Macaca mulatta)
[J].
非人灵长类模型在生殖发育毒性评价中的应用
[J].
Nonhuman Primates as animal models for developmental and reproductive toxicity study
[J].
Effects of social housing of sexually mature male Cynomolgus monkeys during general and reproductive toxicity evaluation
[J].
Multi-omics analysis reveals changes in tryptophan and cholesterol metabolism before and after sexual maturation in captive macaques
[J].
Embryo fetal development studies in nonhuman primates
[J].
Reproductive/developmental toxicity and immunotoxicity assessment in the nonhuman primate model
[J].
人工饲养恒河猴、食蟹猴的繁殖性能初报
[J].
Preliminary study on the reproductive characteristics of Rhesus and Cynomolgus monkeys bred in captivity in Beijing area
[J].
昆明地区食蟹猴种群繁殖规律与繁殖率的分析
[J].
Analysis of reproductive rule and reproductive rate of Cynomolgus monkey population in Kunming area
[J].