SD大鼠使用范围广,是90 d喂养试验常用的啮齿类动物[5]。本文归纳了2020—2023年期间国家药物安全评价监测中心的大鼠90 d喂养试验项目,通过收集并分析其中空白对照组(未给药大鼠)的相关数据,建立动物体重、摄食量、血液学、血清生化、凝血功能、尿液生化指标及病理学相关背景数据库,以期为相关试验的结果分析提供参考依据。
1 材料与方法
1.1 实验动物
120只SPF级SD大鼠,雌雄各半,购自北京维通利华实验动物技术有限公司[SCXK(京)2021-0006],购入时6批次大鼠平均日龄约28 d(雄性体重范围为81.5~97.9 g;雌性体重范围为81.2~98.8 g)。动物饲养设施为中国食品药品检定研究院国家药物安全评价监测中心屏障系统[SYXK(京)2021-0072]。大鼠在屏障系统内网盖开放式笼盒饲养,自由摄食。饲养环境保持在温度20~26 ℃,相对湿度40%~70%,每小时换气15次以上,明暗时间每天各12 h。6批次实验动物质量合格证编号分别为110011201108368514/110011201108368663、1100112111105761041/11001121 11105760983、110011221100776562/1100112211007764 26、110011211108735352/110011211108735467、110011 221111465612/110011221111465513和1100112211102 75328/110011221110275481。研究方案均通过国家药物安全评价监测中心实验动物福利伦理委员会(Institutional Animal Care and Use Committee,IACUC)的伦理审查(审查批件编号为IACUC-2020-110、IACUC-2021-041、IACUC-2022-032、IACUC-2022-042、IACUC-2022-139和IACUC-2022-140)。
1.2 主要试剂和仪器
钴60放射灭菌鼠全价颗粒饲料购自北京科澳协力饲料有限公司(批号21023213、21033213、21073213、22013213、22043213、22053213、22093213和22116113);全血细胞计数试剂(货号T01-3620-52)、尿十项试纸(干化学检测法)[货号Multistix 10 SG Reagent Strips(REF:2169)]和血凝一次性反应杯SUC-400A(货号064-1481-0)购自德国SIEMENS AG公司;碱性磷酸酶测定试剂盒(货号996-63891)、丙氨酸氨基转移酶测定试剂盒(货号994-62591)、天门冬氨酸氨基转移酶测定试剂盒(货号998-61891)和谷氨酰转肽酶测定试剂盒(货号992-63491)购自日本Wako公司;总胆汁酸测定试剂盒(货号CH0101005)、尿素测定试剂盒(货号CH0101051)和甘油三酯测定试剂盒(货号CH0101151)购自四川迈克生物科技股份有限公司。
BCE2201-1CCN型电子天平为德国Sartorius公司产品;H500FR型台式高速冷冻离心机为日本Kokusan公司产品;MINIAM4290尿分析仪为日本Aution公司产品;ADVIA120血液分析仪为德国SIEMENS AG公司产品;CA-1500血凝分析仪为日本Sysmex公司产品;7180型全自动生化分析仪为日本Hitachi公司产品;TEC5EMJ-2型自动包埋机、DRS-2000自动染色机及封片机为日本Sakura公司产品;80iBF-TUW光学显微镜为日本Olympus公司产品。
1.3 实验设计
汇总国家药物安全评价监测中心2020—2023年完成的6个独立的SD大鼠90 d喂养试验中空白对照组大鼠的背景数据。检疫期(4 d)结束后,动物继续观察90 d。动物以1 mL/kg剂量腹腔注射舒泰(50 mg/mL)进行麻醉,之后从下腔静脉取血,完全放血法安乐死并解剖。
1.4 检测指标
研究期间每天观察大鼠临床症状,包括是否死亡、濒死、活动状况、外观及被毛、有无外伤、粪便情况等;每周测定大鼠体重及摄食量2次,根据体重和摄食量计算每周的食物利用率[每周大鼠摄入100 g饲料所增长的体重数值,即体重(g)/饲料量(100 g)];90 d观察结束前做尿液检查。大鼠经麻醉后从下腔静脉取血,用于血液学检查、凝血功能及血清生化学检查。随后完全放血处死。完整摘取并称重主要脏器[脑、胸腺、心脏、肺脏、肝脏、肾脏、肾上腺、脾脏、睾丸/子宫(带子宫颈)、附睾/卵巢],成对的脏器合并称重。根据末次体重测量值,计算脏体比[脏器质量/末次体重×100=脏体比值(g/100 g)][6]。保存组织,包括脑(含垂体)、甲状腺、胸腺、心脏、肺脏、肝脏、肾脏、肾上腺、脾脏、胰腺、胃、肠(起于胃幽门,止于肛门)、睾丸、附睾、前列腺、卵巢、子宫、膀胱、肠系膜淋巴结、颌下淋巴结和腮腺淋巴结。睾丸用Davidson固定液固定,其他脏器用10%中性缓冲福尔马林溶液固定。将组织固定后修块,梯度乙醇溶液脱水,石蜡包埋,切片机切片(厚约3 µm),使用苏木精-伊红(hematoxylin-eosin,HE)染色,光学显微镜下进行检查。
血液学指标包括白细胞(white blood cell,WBC)、中性粒细胞(neutrophil,Neut)、淋巴细胞(lymphocyte,Lymph)、单核细胞(monocyte,Mono)、嗜酸性粒细胞(eosinophil,Eos)、嗜碱性粒细胞(basophil,Baso)、红细胞数(red blood cell count,RBC)、血红蛋白浓度(hemoglobin,HGB)、红细胞比容(hematocrit,HCT)、平均红细胞容积(mean corpuscular volume,MCV)、平均红细胞血红蛋白量(mean corpuscular hemoglobin,MCH)、平均红细胞血红蛋白浓度(mean corpuscular hemoglobin concentration,MCHC)、血小板数(platelet count,PLT)、网织红细胞(reticulocyte,Retic)、凝血酶原时间(prothrombin time,PT)和活化部分凝血激酶时间(activated partial thromboplastin time,APTT)。
血清生化指标包括丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、碱性磷酸酶(alkaline phosphatase,ALP)、肌酸磷酸激酶(creatine phosphokinase,CK)、乳酸脱氢酶(lactate dehydro-genase,LDH)、总胆红素(total bilirubin,TBIL)、尿素氮(blood urea nitrogen,BUN)、肌酐(creatinine,CRE)、葡萄糖(glucose,GLU)、总胆固醇(total cholesterol,CHO)、甘油三酯(triglyceride,TG)、总蛋白质(total protein,TP)、白蛋白(albumin,ALB)、白蛋白/球蛋白(albumin/globulin ratio,A/G)、血清钠(sodium,Na+)、血清钾(potassium,K+)和血清氯(chloride,Cl-)。
尿检查指标包括尿糖、尿蛋白、胆红素、尿胆原、pH、尿比重、隐血、酮体、亚硝酸盐和WBC。
1.5 统计及数据分析
根据Tukey多重比较法和生物学意义判断体重、摄食量、血液学指标、凝血功能及血清生化检查指标、脏器质量和脏体比等数据的离群值,本研究未发现离群值。血液学指标、凝血功能及血清生化检查指标的参考区间以平均数 ± 1.96标准差(
2 结果
2.1 大鼠体重和摄食量
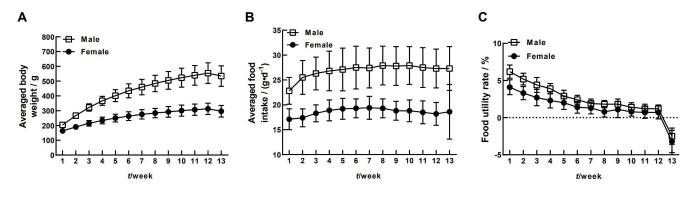
在90 d试验观察期间,大鼠体重、摄食量和食物利用率数据汇总见图1。雄性和雌性大鼠的平均体重均稳步增长,雄性大鼠体重增长幅度更为明显。90 d内雄性和雌性大鼠平均体重分别增长至500 g和300 g以上。3周后,雄性和雌性大鼠的日平均摄食量分别稳定在25~28 g/只和16~19 g/只。所有动物的食物利用率自第1周开始逐渐下降。因第13周动物在解剖前禁食,食物利用率出现负值。
图1
图1
SD大鼠体重(A)、摄食量(B)和食物利用率(C)变化趋势
Figure 1
Trends of body weight(A), food intake(B) and food utilization rate(C) in SD rats
2.2 大鼠临床生理学指标
表1
SD大鼠血液学和凝血功能指标检查结果 (n=60,
Table 1
指标 Index | 雄性 Male | 雌性 Female |
|---|---|---|
| WBC Ccell/(109·L-1) | 7.36±4.27 | 4.82±3.06 |
| %Neut /% | 14.10±9.02 | 14.50±10.58 |
| Neut Ccell/(109·L-1) | 1.04±1.04 | 0.67±0.53 |
| %Lymph /% | 80.30±10.58 | 80.00±11.96 |
| Lymph Ccell/(109·L-1) | 5.90±3.35 | 3.89±2.76 |
| %Mono /% | 2.30±1.96 | 2.20±1.37 |
| Mono Ccell/(109·L-1) | 0.17±0.20 | 0.10±0.08 |
| %Eos /% | 1.50±0.98 | 1.70±1.37 |
| Eos Ccell/(109·L-1) | 0.11±0.08 | 0.08±0.06 |
| %Baso /% | 0.2±0.2 | 0.1±0.1 |
| Baso Ccell/(109·L-1) | 0.01±0.01 | 0.01±0.01 |
| RBC Ccell/(1012·L-1) | 8.90±0.74 | 8.05±0.69 |
| HGB ρ/(g·L-1) | 155±14 | 148±10 |
| HCT /% | 50.0±5.0 | 46.5±5.0 |
| MCV /fL | 56.2±4.1 | 57.7±4.5 |
| MCH m/(pg) | 17.4±1.4 | 18.4±1.2 |
| MCHC ρ/(g·L-1) | 310±31 | 318±27 |
| PLT Ccell/(109·L-1) | 996±321 | 939±300 |
| MPV /fL | 8.2±3.7 | 8.3±2.9 |
| %Retic /% | 3.24±5.94 | 2.40±1.43 |
| Retic Ccell/(109·L-1) | 288.5±53.5 | 191.9±108.6 |
| PT /s | 10.7±5.7 | 8.5±0.8 |
| APTT /s | 16.9±5.5 | 12.8±3.9 |
表2
SD大鼠血清生化指标检查结果 (n=60,
Table 2
指标 Index | 雄性 Male | 雌性 Female |
|---|---|---|
| ALT z/(U·L-1) | 37±18 | 28±16 |
| AST z/(U·L-1) | 128±35 | 107±37 |
| ALP z/(U·L-1) | 104±45 | 53±27 |
| CK z/(U·L-1) | 747±494 | 634±439 |
| LDH z/(U·L-1) | 1 240±735 | 1 072±672 |
| GGT z/(U·L-1) | 4.52±1.84 | 2.43±0.88 |
| TBIL c/(μmol·L-1) | 2.61±0.76 | 3.16±1.31 |
| UREA c/(mmol·L-1) | 6.10±2.35 | 6.20±2.35 |
| CRE c/(μmol·L-1) | 30±8 | 34±8 |
| GLU c/(mmol·L-1) | 7.80±3.02 | 6.92±1.41 |
| CHO c/(mmol·L-1) | 1.80±0.82 | 1.97±0.98 |
| TG c/(mmol·L-1) | 0.68±0.53 | 0.56±0.51 |
| TP ρ/(g·L-1) | 64.3±10.2 | 69.0±11.4 |
| ALB ρ/(g·L-1) | 40.8±12.0 | 48.5±15.3 |
| A/G | 1.81±0.88 | 2.51±1.45 |
| K+c/(mmol·L-1) | 5.04±0.61 | 4.61±0.61 |
| Na+c/(mmol·L-1) | 144.1±3.3 | 143.1±2.5 |
| Cl-c/(mmol·L-1) | 102.9±4.3 | 103.4±5.3 |
大鼠各项尿检查数据见表3。个别大鼠的蛋白质、胆红素、尿胆原、隐血和酮体检测出现阳性结果,雄性大鼠的尿pH值范围在5.0~8.5,大多数为6.5~8.0;雌性大鼠尿pH值范围在6.5~9.0,大多数为7.0~8.5。绝大多数雄性大鼠的尿比重低于1.020,绝大多数雌性大鼠尿比重低于1.015。
表3 SD大鼠尿检查指标检查结果 (n=60)
Table 3
性别 Gender | 葡萄糖 Glucose | 蛋白质 Protein | 胆红素 Bilirubin | 尿胆原 Urobilinogen | 酸碱值 pH | 尿比重 Urine specific gravity | 隐血 Occult blood | 酮体 Ketones | 亚硝酸盐 Nitrite | 白细胞 WBC Ccell/(109·L-1) |
|---|---|---|---|---|---|---|---|---|---|---|
雄性 Male | -: 60/60 | -: 1/60 | -: 59/60 | NORMAL: 41/60 | 5.0: 2/60 | <1.005: 18/60 | -: 41/60 | -: 22/60 | -: 60/60 | -: 9/60 |
| +-: 13/60 | 1+: 1/60 | 1+: 15/60 | 5.5: 1/60 | 1.010: 18/60 | +-: 15/60 | +-: 27/60 | 25: 15/60 | |||
| 1+: 24/60 | 2+: 4/60 | 6.0: 1/60 | 1.015: 10/60 | 1+: 3/60 | 1+: 11/60 | 75: 26/60 | ||||
| 2+: 20/60 | 6.5: 7/60 | 1.020: 11/60 | 2+: 1/60 | 250: 9/60 | ||||||
| 3+: 2/60 | 7.0: 6/60 | 1.025: 2/60 | 500: 1/60 | |||||||
| 7.5: 3/60 | >1.030: 1/60 | |||||||||
| 8.0: 23/60 | ||||||||||
| 8.5: 17/60 | ||||||||||
雌性 Female | -: 60/60 | -: 29/60 | -: 60/60 | NORMAL: 50/60 | 6.5: 2/60 | <1.005: 23/60 | -: 55/60 | -: 50/60 | -: 60/60 | -: 41/60 |
| +-: 17/60 | 1+: 7/60 | 7.0: 6/60 | 1.010: 19/60 | +-: 2/60 | +-: 8/60 | 25: 10/60 | ||||
| 1+: 11/60 | 2+: 2/60 | 7.5: 3/60 | 1.015: 15/60 | 1+: 1/60 | 1+: 2/60 | 75: 7/60 | ||||
| 2+: 3/60 | 3+: 1/60 | 8.0: 22/60 | 1.020: 3/60 | 2+: 1/60 | 250: 2/10 | |||||
| 8.5: 26/60 | 3+: 1/60 | |||||||||
| 9.0: 1/60 |
2.3 大鼠脏器质量
90 d在体研究结束后,雄性和雌性大鼠的主要脏器质量和脏体比数据见表4。试验末期对大鼠心脏、肝脏、肺(含支气管)、脾脏、肾脏、脑、胸腺和肾上腺及生殖器官进行称重。因雄性大鼠体重较重,各脏器(肾上腺、生殖器官除外)的平均质量均高于雌性(P<0.05),而雌性大鼠的脏体比(肾脏、生殖器官除外)高于雄性(P<0.05)。
表4
约18周龄的SD大鼠主要脏器质量和脏体比系数 (n=60,
Table 4
脏器 Organ | 指标 Index | 雄性 Male | 雌性 Female |
|---|---|---|---|
| 心脏Heart | 质量/g | 1.685±0.209 | 1.073±0.140∗∗∗ |
| 脏体比 (g/100 g) | 0.316±0.026 | 0.364±0.035∗∗∗ | |
| 肝脏Liver | 质量/g | 12.898±2.364 | 7.411±1.106∗∗∗ |
| 脏体比 (g/100 g) | 2.402±0.221 | 2.505±0.198∗∗∗ | |
| 肺(含支气管)Lungs (with bronchi) | 质量/g | 1.869±0.247 | 1.359±0.131∗∗∗ |
| 脏体比 (g/100 g) | 0.352±0.042 | 0.464±0.054∗∗∗ | |
| 脾脏Spleen | 质量/g | 0.831±0.193 | 0.528±0.069∗∗∗ |
| 脏体比 (g/100 g) | 0.156±0.033 | 0.180±0.022∗∗∗ | |
| 肾脏Kidney | 质量/g | 3.247±0.442 | 1.837±0.298∗∗∗ |
| 脏体比 (g/100 g) | 0.609±0.059 | 0.622±0.076 | |
| 脑Brain | 质量/g | 2.158±0.107 | 2.010±0.107∗∗∗ |
| 脏体比 (g/100 g) | 0.410±0.054 | 0.688±0.080∗∗∗ | |
| 胸腺Thymus | 质量/g | 0.405±0.118 | 0.330±0.101∗∗∗ |
| 脏体比 (g/100 g) | 0.076±0.020 | 0.111±0.027∗∗∗ | |
| 肾上腺Adrenal gland | 质量/g | 0.064±0.010 | 0.083±0.086 |
| 脏体比 (g/100 g) | 0.012±0.003 | 0.029±0.036∗∗∗ | |
| 睾丸Testis | 质量/g | 3.591±0.534 | / |
| 脏体比 (g/100 g) | 0.678±0.116 | / | |
| 附睾Epididymis | 质量/g | 1.483±0.192 | / |
| 脏体比 (g/100 g) | 0.280±0.043 | / | |
| 子宫Uterus | 质量/g | / | 0.727±0.235 |
| 脏体比 (g/100 g) | / | 0.249±0.087 | |
| 卵巢Ovary | 质量/g | / | 0.117±0.321 |
| 脏体比 (g/100 g) | / | 0.040±0.012 |
2.4 组织病理学检查
所有大鼠的组织病理学检查结果中异常情况如表5所示。常见背景性病变包括肾脏单核细胞浸润和嗜碱性肾小管、炎性细胞浸润或伴心肌细胞变性/坏死、心肌病、前列腺炎性细胞浸润、肝脏小肉芽肿、肺脏泡沫样细胞聚集、肝细胞空泡变性等。
表5 SD大鼠组织病理学病变发生率
Table 5
组织器官 Tissue and organ | 异常所见 Abnormal finding | 病变发生率/% Incidence of lesions/% | |
|---|---|---|---|
雄性 Male | 雌性 Female | ||
肾脏 Kidney | 皮质/髓质/肾盂,单核细胞浸润 | 45.0 | 30.0 |
| 嗜碱性肾小管 | 33.0 | 10.0 | |
| 梗死 | 1.7 | 0 | |
| 透明管型 | 10.0 | 0 | |
| 慢性进行性肾病 | 0 | 1.7 | |
心脏 Heart | 炎性细胞浸润或伴心肌细胞变性/坏死 | 40.0 | 5.0 |
| 心肌病 | 5.0 | 3.3 | |
肝脏 Liver | 单核细胞浸润 | 5.0 | 1.7 |
| 肝细胞空泡变性 | 18.3 | 11.7 | |
| 小肉芽肿伴或不伴肝细胞坏死 | 68.3 | 68.3 | |
脾脏 Spleen | 红髓扩张 | 1.7 | 3.3 |
| 色素沉着 | 0 | 15.0 | |
| 髓外造血 | 0 | 1.7 | |
| 淋巴滤泡减少 | 1.7 | 0 | |
胸腺 Thymus | 出血 | 10.0 | 6.7 |
| 皮质,淋巴细胞/易染体巨噬细胞数目增多 | 1.7 | 1.7 | |
肺(含支气管) Lungs (with bronchi) | 被膜/间质/血管周围,炎性细胞浸润 | 6.7 | 10.0 |
| 泡沫样细胞聚集 | 16.7 | 26.7 | |
| 肺泡上皮细胞增生 | 0 | 3.3 | |
| 骨化生 | 3.3 | 0 | |
| 出血 | 3.3 | 0 | |
胰腺 Pancreas | 外分泌部,萎缩伴炎性细胞浸润 | 6.7 | 8.3 |
| 胰岛,纤维化 | 1.7 | 0 | |
颌下淋巴结 Submandibular lymph nodes | 红细胞增多/吞噬作用 | 1.7 | 1.7 |
| 髓窦,浆细胞增多 | 1.7 | 1.7 | |
肠系膜淋巴结 Mesenteric glands | 红细胞增多/吞噬作用 | 0 | 1.7 |
垂体 Pituitary gland | 囊肿 | 8.3 | 0 |
胃 Stomach | 腺腔扩张 | 3.3 | 1.7 |
颈部淋巴结 Cervical lymph node | 髓质,浆细胞增多 | 3.3 | 0 |
| 红细胞增多/吞噬作用 | 0 | 1.7 | |
| 出血 | 5.0 | 1.7 | |
肾上腺 Adrenal gland | 皮质细胞空泡变性 | 3.3 | 0 |
前列腺 Prostate gland | 间质,单核细胞浸润 | 21.7 | / |
甲状腺 Thyroid gland | 滤泡增生 | 6.7 | 0 |
| 间质,单核细胞浸润 | 0 | 1.7 | |
睾丸 Testis | 单侧或双侧,生精小管萎缩 | 1.7 | |
附睾 Epididymis | 单侧或双侧,精子减少 | 1.7 | / |
子宫 Uterus | 色素沉着 | / | 1.7 |
| 子宫腔扩张 | / | 8.3 | |
卵巢 Ovary | / | / | 0 |
3 讨论
2018年中山大学实验动物中心[10]周龄相近的SD大鼠临床生化学指标较为一致。
动物体重、摄食量、血液学和血清生化和脏器质量等指标与动物的品系、性别、年龄及营养因素有关[11],比较上述指标时需根据其上述特征进行分类。除受年龄和性别影响外,动物的各项生理指标也与其生活环境、营养水平和生理状况等因素有关[12- 13]。蒋荣荣[14]研究发现改变大鼠饲养环境中的温度、湿度、光照周期和光照强度均可导致SD大鼠血常规中RBC、HGB、MCH和MCHC改变,血清生化指标中ALT、AST、ALB升高,UREA、CRE、TG和GLU降低,但对动物脏器质量无明显影响。刘帅等[15]研究发现,SD雄性大鼠在环境丰富的条件下(提供磨牙棒和木丝筑巢材料)摄食量显著增加,TP、ALB和CHO明显增加,雌性大鼠的RBC、HGB和PLT等数值明显增加。本研究第90天时,雄性大鼠体重显著大于雌性大鼠(500 g vs 300 g),摄食量更多(25~28 g/d vs 16~19 g/d),反映雄性代谢需求更高,可能与睾酮促进蛋白质合成相关。雄性大鼠RBC、HGB、HCT、PLT等指标显著高于雌性(P<0.05),提示雄性大鼠造血功能更强或血容量更大;凝血参数(PT、APTT)的性别差异可能影响药物对凝血系统作用的评估。雄性大鼠ALT、AST、ALP、CK等肝酶及GLU、TG水平更高,可能与肝脏代谢活性或能量利用的性别特异性相关,需警惕高估药物对雄性大鼠肝脏的潜在毒性。雄性大鼠尿pH值范围更广(5.0~8.5 vs 6.5~9.0),尿比重更高,提示肾功能性别差异;雄性大鼠脏器质量更高,但雌性脏体比更大,反映体重对脏器比例的调节作用。
本研究中,组织病理学检查发现的病变多为与动物品种或年龄相关的背景性病变。肾脏嗜碱性肾小管属于一种非特异性变性,这种变化是退行性病变的结果或是细胞的更新再生过程,在发育中的青年大鼠属于正常现象,缺乏明显的基底膜增厚是其与慢性进行性肾病(chronic progressive nephropathy,CPN)区别的关键点。CPN是常用试验大鼠品种的自发性肾疾病,其中SD、Fischer 344品种慢性进行性肾病较Wistar、Brown-Norway(BN)更严重,氨基酸组成的改变以及肾小管周围基底层的羟基化和糖基化,已被证实是大鼠CPN发生的重要原因之一。肾脏单核细胞浸润可单独出现或与早期CPN相关,在皮髓质交界处或弓形动脉旁,可见自发性单核细胞浸润,为常见背景性病变,几乎没有病理学意义,浸润灶的数量会随年龄的增长而增加。自发性心肌病可见于所有品系的大鼠,幼龄大鼠及雄性大鼠发病率更高,属于自发退行性病变,目前病因未知,严重程度可能和年龄、饮食及应激因素相关[16]。此外,前列腺炎性细胞浸润的发生率也随着动物年龄增长而增加[17-18]。肝脏小肉芽肿和肺脏泡沫样细胞巨噬细胞聚集为啮齿类动物常见的背景性病变,可能与饲养环境和饲料种类等因素有关[19-20]。肝细胞空泡变性可能与饲料种类或与年龄增加有关的脂代谢改变相关[21]。在考察受试物相关的病理学改变时应注意与上述病变进行区分。
综上所述,本研究总结了国家药物安全评价监测中心SPF级SD大鼠在90 d试验期内的体重、摄食量、血液学和血清生化各项指标的背景参考值范围,并梳理了动物的背景性和自发性的组织病理学改变。本研究建立的SD大鼠生理、生化和病理背景数据库,为相关研究提供了标准化参考[25]。通过明确性别差异,可指导异常结果的性别特异性分析。其中,性别差异数据强调需分性别设置对照组,避免因基线不同掩盖或夸大受试物效应。临床试验设计中应考虑动物模型的性别因素,合理分配受试者性别比例,提高动物实验结果外推至人类的可靠性。
[引用本文]
秦超, 李双星, 赵婷婷, 等. 药物安全评价用SD大鼠90 d喂养试验的背景数据研究[J]. 实验动物与比较医学, 2025, 45(4): 439-448. DOI:10.12300/j.issn.1674-5817.2024.187.
QIN C, LI S X, ZHAO T T, et al. Study on the 90-day feedingexperimental background data of SD rats for drug safetyevaluation[J]. Lab Anim Comp Med, 2025, 45(4): 439-448. DOI:10.12300/j.issn.1674-5817.2024.187.
作者贡献声明
秦超负责试验材料准备、在体试验操作、在体数据收集,参与原稿写作;
李双星负责病理学检查与数据收集,参与数据分析与原稿写作;
赵婷婷参与试验材料准备、在体试验操作和数据收集;
蒋晨晨参与数据分析与原稿写作;
赵晶参与在体试验操作与数据收集;
杨艳伟参与试验材料准备、病理学检查与数据收集;
林志参与病理学检查和项目支持;
王三龙参与项目支持;
文海若负责研究设计、项目支持、数据分析与原稿写作。
医学伦理声明Medical Ethics Statement
本研究方案实施前已经国家药物安全评价监测中心动物管理与使用委员会审查批准(伦理批复编号:IACUC-2020-110、IACUC-2021-041、IACUC-2022-032、IACUC-2022-042、IACUC-2022-139、IACUC-2022-140)。研究中所有实验动物相关操作均严格遵守美国国家科学院实验动物资源研究所发布的《实验动物护理和使用指南》(
Ethics Approval and Patient Consent
All animal experimental procedures were approved by the Institutional Animal Care and Use Committee (IACUC) of the National Center for Safety Evaluation of Drugs (IACUC Approval No. IACUC-2020-110, IACUC-2021-041, IACUC-2022-032, IACUC-2022-042, IACUC-2022-139, IACUC-2022-140). All laboratory animal-related operations in the research strictly adhere to the Guide for the Care and Use of Laboratory Animals published by the Institute of Laboratory Animal Resources of the National Academy of Sciences (
利益冲突声明
所有作者声明不存在利益冲突。
参考文献
A 90-day rodent feeding study with grain for genetically modified maize L4 conferring insect resistance and glyphosate tolerance
[J].
A 90-day safety study of meat from MSTN and FGF5 double-knockout sheep in wistar rats
[J].
Rodent and broiler feeding studies with maize containing genetically modified event DP-915635-4 show no adverse effects on health or performance
[J].
A 90-day feeding study of genetically modified maize LP007-1 in wistar Han RCC rats
[J].
Safety assessment of phytase transgenic maize 11TPY050 in Sprague-Dawley rats by 90-day feeding study
[J].
Wistar大鼠主要脏器系数与体重相关性的探讨
[J].
Correlation between main organ coefficients and body weight in Wistar rats
[J].
Safety assessment of transgenic maize CC-2 by 90-day feeding study in Sprague-Dawley rats
[J].
不同周龄雌雄SD大鼠血液生理生化指标比较分析
[J].
Comparison of the blood physiological and biochemical indicators among SD rats of different ages and genders
[J].
SD大鼠90 d喂养试验生理生化指标正常参考值的研究
[J].
Study on the normal reference interval of hematological and serum biochemical indexes in 90 d feeding study on SD rats
[J].
不同月龄SPF级SD大鼠临床生理生化背景数据分析
[J].
Analysis of the background data of hemocytology and biochemistry in the blood of SPF Sprague Dawley rats at different ages
[J].
A histopathological analysis of spontaneous neoplastic and non-neoplastic lesions in aged male RccHan: WIST rats
[J].
Historical control background incidence of spontaneous nonneoplastic lesions of sprague dawley rats in 104-week carcinogenicity studies
[J].
Historical control background incidence of spontaneous neoplastic lesions of sprague-dawley rats in 104-week toxicity studies
[J].
温湿度等环境因素对SD大鼠福利的影响研究
[D].
Effects of environmental factors such as temperature and humidity on the welfare of SD rats
[D].
环境丰富对SD大鼠生长和血液学指标的影响
[J].
Effect of environmental enrichment on growth and hematology in SD rats
[J].
Age-related changes in lung function in National Center for Geriatrics and Gerontology Aging Farm C57BL/6N mice
[J].
The onset of age-related benign prostatic hyperplasia is concomitant with increased serum and prostatic expression of VEGF in rats: Potential role of VEGF as a marker for early prostatic alterations
[J].
Rat age-related benign prostate hyperplasia is concomitant with an increase in the secretion of low ramified α-glycosydic polysaccharides
[J].
Research-relevant conditions and pathology of laboratory mice, rats, gerbils, guinea pigs, hamsters, naked mole rats, and rabbits
[J].
Historical control background incidence of spontaneous pituitary gland lesions of Han-Wistar and Sprague-Dawley rats and CD-1 mice used in 104-week carcinogenicity studies
[J].
Review of approaches to the recording of background lesions in toxicologic pathology studies in rats
[J].
The calculation of historical control limits in toxicology: Do's, don'ts and open issues from a statistical perspective
[J].
Background data for general toxicology parameters in RccHan: wist rats at 8, 10, 19 and 32 weeks of age
[J].
Aromatase inhibition and ketamine in rats: sex-differences in antidepressant-like efficacy
[J].
SD大鼠胚胎-胎仔发育毒性试验背景数据的建立
[J].
Background data of SD rats in embryo-fetal development toxicity study
[J].