A brief history of Drosophila's contributions to genome research
1
2000
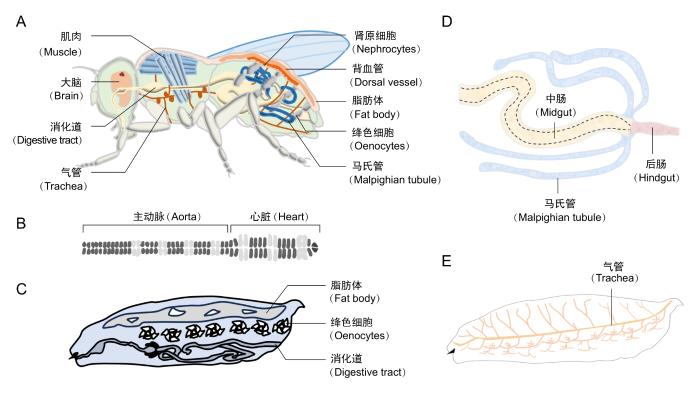
... 发育生物学的核心目标之一是解析生物体从单细胞胚胎到复杂多器官个体的构建机制,而模式生物的应用是实现这一目标的关键.自1910年摩尔根实验室将果蝇(Drosophila)引入遗传学研究以来,果蝇凭借其短生命周期、高繁殖力、低饲养成本及高效的遗传操作工具[如源自酵母的半乳糖凝集素4(galectin-4,GAL4)/上游活化序列(upstream activating sequence,UAS)基因表达调控系统、规律成簇的间隔短回文重复序列(clustered regularly interspaced short palindromic repeats,CRISPR)/CRISPR相关蛋白核酸酶9(CRISPR-associated protein 9,Cas9)基因编辑技术]等优势,迅速成为研究器官发育保守性的理想模型[1-2].尽管果蝇与哺乳动物在器官形态上差异显著,但其核心发育调控机制在6亿年的进化历程中表现出高度保守性(图1A),这种“异形态、同机制”的特征为跨物种比较研究提供了关键切入点:一方面,Hox基因家族和Wg/Wnt(wingless/wingless-type MMTV integration site family)、Hh(hedgehog)、Notch等信号通路在果蝇与哺乳动物的器官发育中均发挥保守功能[3-5];另一方面,果蝇中约61%的基因在人类中存在同源基因,且其中许多基因在器官发育中功能保守,这种保守性特征使得科研工作者可以通过研究果蝇基因,解析人类器官的发育机制. ...
A Drosophila single-cell 3D spatiotemporal multi-omics atlas unveils panoramic key regulators of cell-type differentiation
1
2025
... 发育生物学的核心目标之一是解析生物体从单细胞胚胎到复杂多器官个体的构建机制,而模式生物的应用是实现这一目标的关键.自1910年摩尔根实验室将果蝇(Drosophila)引入遗传学研究以来,果蝇凭借其短生命周期、高繁殖力、低饲养成本及高效的遗传操作工具[如源自酵母的半乳糖凝集素4(galectin-4,GAL4)/上游活化序列(upstream activating sequence,UAS)基因表达调控系统、规律成簇的间隔短回文重复序列(clustered regularly interspaced short palindromic repeats,CRISPR)/CRISPR相关蛋白核酸酶9(CRISPR-associated protein 9,Cas9)基因编辑技术]等优势,迅速成为研究器官发育保守性的理想模型[1-2].尽管果蝇与哺乳动物在器官形态上差异显著,但其核心发育调控机制在6亿年的进化历程中表现出高度保守性(图1A),这种“异形态、同机制”的特征为跨物种比较研究提供了关键切入点:一方面,Hox基因家族和Wg/Wnt(wingless/wingless-type MMTV integration site family)、Hh(hedgehog)、Notch等信号通路在果蝇与哺乳动物的器官发育中均发挥保守功能[3-5];另一方面,果蝇中约61%的基因在人类中存在同源基因,且其中许多基因在器官发育中功能保守,这种保守性特征使得科研工作者可以通过研究果蝇基因,解析人类器官的发育机制. ...
The exon junction complex regulates the splicing of cell polarity gene dlg1 to control Wingless signaling in development
1
2016
... 发育生物学的核心目标之一是解析生物体从单细胞胚胎到复杂多器官个体的构建机制,而模式生物的应用是实现这一目标的关键.自1910年摩尔根实验室将果蝇(Drosophila)引入遗传学研究以来,果蝇凭借其短生命周期、高繁殖力、低饲养成本及高效的遗传操作工具[如源自酵母的半乳糖凝集素4(galectin-4,GAL4)/上游活化序列(upstream activating sequence,UAS)基因表达调控系统、规律成簇的间隔短回文重复序列(clustered regularly interspaced short palindromic repeats,CRISPR)/CRISPR相关蛋白核酸酶9(CRISPR-associated protein 9,Cas9)基因编辑技术]等优势,迅速成为研究器官发育保守性的理想模型[1-2].尽管果蝇与哺乳动物在器官形态上差异显著,但其核心发育调控机制在6亿年的进化历程中表现出高度保守性(图1A),这种“异形态、同机制”的特征为跨物种比较研究提供了关键切入点:一方面,Hox基因家族和Wg/Wnt(wingless/wingless-type MMTV integration site family)、Hh(hedgehog)、Notch等信号通路在果蝇与哺乳动物的器官发育中均发挥保守功能[3-5];另一方面,果蝇中约61%的基因在人类中存在同源基因,且其中许多基因在器官发育中功能保守,这种保守性特征使得科研工作者可以通过研究果蝇基因,解析人类器官的发育机制. ...
A homologous protein-coding sequence in Drosophila homeotic genes and its conservation in other metazoans
0
1984
Smoothened transduces Hedgehog signal by forming a complex with Evc/Evc2
1
2012
... 发育生物学的核心目标之一是解析生物体从单细胞胚胎到复杂多器官个体的构建机制,而模式生物的应用是实现这一目标的关键.自1910年摩尔根实验室将果蝇(Drosophila)引入遗传学研究以来,果蝇凭借其短生命周期、高繁殖力、低饲养成本及高效的遗传操作工具[如源自酵母的半乳糖凝集素4(galectin-4,GAL4)/上游活化序列(upstream activating sequence,UAS)基因表达调控系统、规律成簇的间隔短回文重复序列(clustered regularly interspaced short palindromic repeats,CRISPR)/CRISPR相关蛋白核酸酶9(CRISPR-associated protein 9,Cas9)基因编辑技术]等优势,迅速成为研究器官发育保守性的理想模型[1-2].尽管果蝇与哺乳动物在器官形态上差异显著,但其核心发育调控机制在6亿年的进化历程中表现出高度保守性(图1A),这种“异形态、同机制”的特征为跨物种比较研究提供了关键切入点:一方面,Hox基因家族和Wg/Wnt(wingless/wingless-type MMTV integration site family)、Hh(hedgehog)、Notch等信号通路在果蝇与哺乳动物的器官发育中均发挥保守功能[3-5];另一方面,果蝇中约61%的基因在人类中存在同源基因,且其中许多基因在器官发育中功能保守,这种保守性特征使得科研工作者可以通过研究果蝇基因,解析人类器官的发育机制. ...
Embryonic origin and differentiation of the Drosophila Heart
2
1994
... 背血管(dorsal vessel)是果蝇主要的循环器官,相当于果蝇的“心脏”,呈细长管状结构,沿背部中轴线分布(图1A).背血管起源于中胚层背部,主要由成心肌细胞(cardioblast,CB)和围心细胞(pericardial cells,PCs)构成.成心肌细胞可形成心管并分化为收缩性心肌细胞,围心细胞则不规则地分布在背血管两侧,承担血淋巴过滤的功能[6-7].背血管在结构上具有前后极性,前部为“主动脉”,后部为“心脏本体”,二者通过一对特化的成心肌细胞形成的心血管瓣膜隔开(图1B).血淋巴作为为器官提供营养的重要流体,通过心门进入“心脏本体”,再经位于顶端的流出道排出.与脊椎动物心脏不同的是,果蝇的心管不会发生弯曲,始终保持简单的线性结构.果蝇的心肌细胞源于心脏中胚层的心脏前体细胞[6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
... [6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
Heart development in Drosophila requires the segment polarity gene wingless
1
1995
... 背血管(dorsal vessel)是果蝇主要的循环器官,相当于果蝇的“心脏”,呈细长管状结构,沿背部中轴线分布(图1A).背血管起源于中胚层背部,主要由成心肌细胞(cardioblast,CB)和围心细胞(pericardial cells,PCs)构成.成心肌细胞可形成心管并分化为收缩性心肌细胞,围心细胞则不规则地分布在背血管两侧,承担血淋巴过滤的功能[6-7].背血管在结构上具有前后极性,前部为“主动脉”,后部为“心脏本体”,二者通过一对特化的成心肌细胞形成的心血管瓣膜隔开(图1B).血淋巴作为为器官提供营养的重要流体,通过心门进入“心脏本体”,再经位于顶端的流出道排出.与脊椎动物心脏不同的是,果蝇的心管不会发生弯曲,始终保持简单的线性结构.果蝇的心肌细胞源于心脏中胚层的心脏前体细胞[6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
The gene tinman is required for specification of the heart and visceral muscles in Drosophila
1
1993
... 背血管(dorsal vessel)是果蝇主要的循环器官,相当于果蝇的“心脏”,呈细长管状结构,沿背部中轴线分布(图1A).背血管起源于中胚层背部,主要由成心肌细胞(cardioblast,CB)和围心细胞(pericardial cells,PCs)构成.成心肌细胞可形成心管并分化为收缩性心肌细胞,围心细胞则不规则地分布在背血管两侧,承担血淋巴过滤的功能[6-7].背血管在结构上具有前后极性,前部为“主动脉”,后部为“心脏本体”,二者通过一对特化的成心肌细胞形成的心血管瓣膜隔开(图1B).血淋巴作为为器官提供营养的重要流体,通过心门进入“心脏本体”,再经位于顶端的流出道排出.与脊椎动物心脏不同的是,果蝇的心管不会发生弯曲,始终保持简单的线性结构.果蝇的心肌细胞源于心脏中胚层的心脏前体细胞[6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
The patterns of wingless, decapentaplegic, and tinman position the Drosophila heart
1
2002
... 背血管(dorsal vessel)是果蝇主要的循环器官,相当于果蝇的“心脏”,呈细长管状结构,沿背部中轴线分布(图1A).背血管起源于中胚层背部,主要由成心肌细胞(cardioblast,CB)和围心细胞(pericardial cells,PCs)构成.成心肌细胞可形成心管并分化为收缩性心肌细胞,围心细胞则不规则地分布在背血管两侧,承担血淋巴过滤的功能[6-7].背血管在结构上具有前后极性,前部为“主动脉”,后部为“心脏本体”,二者通过一对特化的成心肌细胞形成的心血管瓣膜隔开(图1B).血淋巴作为为器官提供营养的重要流体,通过心门进入“心脏本体”,再经位于顶端的流出道排出.与脊椎动物心脏不同的是,果蝇的心管不会发生弯曲,始终保持简单的线性结构.果蝇的心肌细胞源于心脏中胚层的心脏前体细胞[6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
The wingless signaling pathway is directly involved in Drosophila heart development
1
1996
... 背血管(dorsal vessel)是果蝇主要的循环器官,相当于果蝇的“心脏”,呈细长管状结构,沿背部中轴线分布(图1A).背血管起源于中胚层背部,主要由成心肌细胞(cardioblast,CB)和围心细胞(pericardial cells,PCs)构成.成心肌细胞可形成心管并分化为收缩性心肌细胞,围心细胞则不规则地分布在背血管两侧,承担血淋巴过滤的功能[6-7].背血管在结构上具有前后极性,前部为“主动脉”,后部为“心脏本体”,二者通过一对特化的成心肌细胞形成的心血管瓣膜隔开(图1B).血淋巴作为为器官提供营养的重要流体,通过心门进入“心脏本体”,再经位于顶端的流出道排出.与脊椎动物心脏不同的是,果蝇的心管不会发生弯曲,始终保持简单的线性结构.果蝇的心肌细胞源于心脏中胚层的心脏前体细胞[6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
Gata factor Pannier is required to establish competence for heart progenitor formation
1
2003
... 背血管(dorsal vessel)是果蝇主要的循环器官,相当于果蝇的“心脏”,呈细长管状结构,沿背部中轴线分布(图1A).背血管起源于中胚层背部,主要由成心肌细胞(cardioblast,CB)和围心细胞(pericardial cells,PCs)构成.成心肌细胞可形成心管并分化为收缩性心肌细胞,围心细胞则不规则地分布在背血管两侧,承担血淋巴过滤的功能[6-7].背血管在结构上具有前后极性,前部为“主动脉”,后部为“心脏本体”,二者通过一对特化的成心肌细胞形成的心血管瓣膜隔开(图1B).血淋巴作为为器官提供营养的重要流体,通过心门进入“心脏本体”,再经位于顶端的流出道排出.与脊椎动物心脏不同的是,果蝇的心管不会发生弯曲,始终保持简单的线性结构.果蝇的心肌细胞源于心脏中胚层的心脏前体细胞[6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
Probing the polygenic basis of cardiomyopathies in Drosophila
1
2012
... 背血管(dorsal vessel)是果蝇主要的循环器官,相当于果蝇的“心脏”,呈细长管状结构,沿背部中轴线分布(图1A).背血管起源于中胚层背部,主要由成心肌细胞(cardioblast,CB)和围心细胞(pericardial cells,PCs)构成.成心肌细胞可形成心管并分化为收缩性心肌细胞,围心细胞则不规则地分布在背血管两侧,承担血淋巴过滤的功能[6-7].背血管在结构上具有前后极性,前部为“主动脉”,后部为“心脏本体”,二者通过一对特化的成心肌细胞形成的心血管瓣膜隔开(图1B).血淋巴作为为器官提供营养的重要流体,通过心门进入“心脏本体”,再经位于顶端的流出道排出.与脊椎动物心脏不同的是,果蝇的心管不会发生弯曲,始终保持简单的线性结构.果蝇的心肌细胞源于心脏中胚层的心脏前体细胞[6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
Akirin is critical for early tinman induction and subsequent formation of the heart in Drosophila melanogaster
2
2021
... 背血管(dorsal vessel)是果蝇主要的循环器官,相当于果蝇的“心脏”,呈细长管状结构,沿背部中轴线分布(图1A).背血管起源于中胚层背部,主要由成心肌细胞(cardioblast,CB)和围心细胞(pericardial cells,PCs)构成.成心肌细胞可形成心管并分化为收缩性心肌细胞,围心细胞则不规则地分布在背血管两侧,承担血淋巴过滤的功能[6-7].背血管在结构上具有前后极性,前部为“主动脉”,后部为“心脏本体”,二者通过一对特化的成心肌细胞形成的心血管瓣膜隔开(图1B).血淋巴作为为器官提供营养的重要流体,通过心门进入“心脏本体”,再经位于顶端的流出道排出.与脊椎动物心脏不同的是,果蝇的心管不会发生弯曲,始终保持简单的线性结构.果蝇的心肌细胞源于心脏中胚层的心脏前体细胞[6].在胚胎早期,中胚层转录因子Twist启动Tinman基因在整个中胚层表达[8-9];随后,Tinman受Dpp(decapentaplegic)和Wg信号通路的调控,先局限于背部中胚层表达;到胚胎第10期时,Tinman被进一步限定在心脏中胚层表达[10-11];到胚胎第11期时,Dpp和Wg还会诱导GATA转录因子Pnr在心脏中胚层表达[12].研究表明,转录辅助因子Akirin突变会引发心脏形态缺陷,导致Tinman转录本及蛋白表达水平降低,进而使Tinman阳性细胞数量减少[13].综上,Dpp、Wg和Akirin共同调控心脏关键基因Tinman在心肌细胞中的区域性表达,从而决定心脏前体细胞的定位与分化进程. ...
... 果蝇Tinman与哺乳动物Nkx2-5均为心脏发育的核心转录因子,二者突变分别导致果蝇背血管缺失和人类先天性心脏病(如房间隔缺损),并分别调控Mef2基因和GATA结合蛋白4(GATA binding protein 4,GATA4)参与心肌细胞的分化[13-14].在Wnt信号通路中,果蝇Wg通过β-联蛋白调控心脏前体细胞的增殖,哺乳动物Wnt则参与心管弯曲的形成;在Hh信号通路中,果蝇Hh与哺乳动物Shh(sonic hedgehog)均通过跨膜蛋白Patched和Smoothened受体复合物调控心腔形态的发生,二者突变均导致心脏流出通道发育异常[15].果蝇和脊椎动物在心脏发育的早期阶段存在显著相似性,且控制早期心脏发生的基因高度保守,这使得果蝇背血管成为研究心脏发育机制以及鉴定复杂且高度异质性的先天性心脏缺陷相关基因的理想模型系统. ...
Examining the cardiac NK-2 genes in early heart development
2
2010
... 果蝇Tinman与哺乳动物Nkx2-5均为心脏发育的核心转录因子,二者突变分别导致果蝇背血管缺失和人类先天性心脏病(如房间隔缺损),并分别调控Mef2基因和GATA结合蛋白4(GATA binding protein 4,GATA4)参与心肌细胞的分化[13-14].在Wnt信号通路中,果蝇Wg通过β-联蛋白调控心脏前体细胞的增殖,哺乳动物Wnt则参与心管弯曲的形成;在Hh信号通路中,果蝇Hh与哺乳动物Shh(sonic hedgehog)均通过跨膜蛋白Patched和Smoothened受体复合物调控心腔形态的发生,二者突变均导致心脏流出通道发育异常[15].果蝇和脊椎动物在心脏发育的早期阶段存在显著相似性,且控制早期心脏发生的基因高度保守,这使得果蝇背血管成为研究心脏发育机制以及鉴定复杂且高度异质性的先天性心脏缺陷相关基因的理想模型系统. ...
... 果蝇模型凭借其遗传操作简单和高通量筛选便捷等优势,已成为构建人类疾病模型和进行药物筛选及研发的关键平台.例如,基于果蝇气管系统与哺乳动物肺脏在FGF信号调控分支发育上的保守性,通过果蝇气管分支缺陷模型筛选出的FGF通路抑制剂已用于人类肺纤维化临床前研究[47];基于果蝇背血管与哺乳动物心脏在心肌细胞分化过程中的高度相似性,利用果蝇背血管发育模型揭示人类先天性心脏病的部分致病基因(如Nkx2-5)及相关信号通路的调控机制(如Dpp/Wg信号通路)[14-15];脂肪体与绛色细胞的代谢调控机制为人类肥胖、脂肪肝等代谢性疾病提供了从基因功能解析到药物筛选的系统研究脉络;马氏管与肾原细胞在滤过-排泄系统方面的保守性,则有助于阐明多囊肾、肾癌等疾病中纤毛功能异常及相关信号通路机制;气管系统分支形态发生中的FGF信号调控,为先天性肺气道畸形等疾病的机制研究提供了跨物种参照.此外,果蝇的神经系统相对简单,由约10万个神经元组成,但这些神经元之间的连接方式及其功能特点与人类大脑具有惊人的相似性,这种特征使果蝇成为研究癫痫等神经系统疾病的理想模型.未来,随着更多保守调控机制的解析,果蝇模型在器官发育异常相关疾病的机制研究与治疗策略开发中,将进一步发挥其“以简驭繁”的独特优势. ...
Wnt/beta-catenin signaling in development and disease
2
2006
... 果蝇Tinman与哺乳动物Nkx2-5均为心脏发育的核心转录因子,二者突变分别导致果蝇背血管缺失和人类先天性心脏病(如房间隔缺损),并分别调控Mef2基因和GATA结合蛋白4(GATA binding protein 4,GATA4)参与心肌细胞的分化[13-14].在Wnt信号通路中,果蝇Wg通过β-联蛋白调控心脏前体细胞的增殖,哺乳动物Wnt则参与心管弯曲的形成;在Hh信号通路中,果蝇Hh与哺乳动物Shh(sonic hedgehog)均通过跨膜蛋白Patched和Smoothened受体复合物调控心腔形态的发生,二者突变均导致心脏流出通道发育异常[15].果蝇和脊椎动物在心脏发育的早期阶段存在显著相似性,且控制早期心脏发生的基因高度保守,这使得果蝇背血管成为研究心脏发育机制以及鉴定复杂且高度异质性的先天性心脏缺陷相关基因的理想模型系统. ...
... 果蝇模型凭借其遗传操作简单和高通量筛选便捷等优势,已成为构建人类疾病模型和进行药物筛选及研发的关键平台.例如,基于果蝇气管系统与哺乳动物肺脏在FGF信号调控分支发育上的保守性,通过果蝇气管分支缺陷模型筛选出的FGF通路抑制剂已用于人类肺纤维化临床前研究[47];基于果蝇背血管与哺乳动物心脏在心肌细胞分化过程中的高度相似性,利用果蝇背血管发育模型揭示人类先天性心脏病的部分致病基因(如Nkx2-5)及相关信号通路的调控机制(如Dpp/Wg信号通路)[14-15];脂肪体与绛色细胞的代谢调控机制为人类肥胖、脂肪肝等代谢性疾病提供了从基因功能解析到药物筛选的系统研究脉络;马氏管与肾原细胞在滤过-排泄系统方面的保守性,则有助于阐明多囊肾、肾癌等疾病中纤毛功能异常及相关信号通路机制;气管系统分支形态发生中的FGF信号调控,为先天性肺气道畸形等疾病的机制研究提供了跨物种参照.此外,果蝇的神经系统相对简单,由约10万个神经元组成,但这些神经元之间的连接方式及其功能特点与人类大脑具有惊人的相似性,这种特征使果蝇成为研究癫痫等神经系统疾病的理想模型.未来,随着更多保守调控机制的解析,果蝇模型在器官发育异常相关疾病的机制研究与治疗策略开发中,将进一步发挥其“以简驭繁”的独特优势. ...
Adipokine and fat body in flies: Connecting organs
1
2021
... 果蝇脂肪体(fat body)和绛色细胞(oenocytes)承担着营养储存、代谢调节、免疫防御等关键的生理功能,与哺乳动物肝脏的功能具有一定的相似性(图1C).脂肪体起源于腹部中胚层(A2-A8体节腹侧),由脂肪体细胞构成,其发育历经胚胎形成、幼虫成熟、蛹期重塑和成虫分化4个阶段,各阶段均受到多种转录因子、激素及信号通路的精准调控[16-17].在胚胎发育早期,中胚层细胞在转录因子Srp(Serpent)[18]的调控下,特化为脂肪体前体细胞(fat body precursor cell,FBP).在胚胎第13∼16期,FBP脱离中胚层,经过迁移和聚集形成分节排列的细胞团,构成脂肪体雏形,此时细胞内尚未形成脂滴,主要为胚胎晚期发育提供基础营养支持.进入幼虫期(L1∼L3)后,脂肪体细胞以体积增大为主[19-20],至L3期末细胞直径可达100 μm以上,与此同时,细胞中开始大量合成并积累脂滴和贮存蛋白(larval serum protein,LSP)1、LSP2等储存蛋白[21].蛹期,在蜕皮激素的主导下,约70%的幼虫脂肪体细胞因自噬和凋亡被降解,释放的营养用于支持成虫盘的发育;其余约30%的脂肪体细胞则重新聚集,体积缩小,脂滴合成减少,转而合成成虫特异性蛋白,并分化为成虫脂肪体前体.成虫期,脂肪体主要分布于腹部背板下方,在能量稳态调控、繁殖支持及免疫防御等方面发挥重要作用. ...
Embryonic fat-cell lineage in Drosophila melanogaster
1
1994
... 果蝇脂肪体(fat body)和绛色细胞(oenocytes)承担着营养储存、代谢调节、免疫防御等关键的生理功能,与哺乳动物肝脏的功能具有一定的相似性(图1C).脂肪体起源于腹部中胚层(A2-A8体节腹侧),由脂肪体细胞构成,其发育历经胚胎形成、幼虫成熟、蛹期重塑和成虫分化4个阶段,各阶段均受到多种转录因子、激素及信号通路的精准调控[16-17].在胚胎发育早期,中胚层细胞在转录因子Srp(Serpent)[18]的调控下,特化为脂肪体前体细胞(fat body precursor cell,FBP).在胚胎第13∼16期,FBP脱离中胚层,经过迁移和聚集形成分节排列的细胞团,构成脂肪体雏形,此时细胞内尚未形成脂滴,主要为胚胎晚期发育提供基础营养支持.进入幼虫期(L1∼L3)后,脂肪体细胞以体积增大为主[19-20],至L3期末细胞直径可达100 μm以上,与此同时,细胞中开始大量合成并积累脂滴和贮存蛋白(larval serum protein,LSP)1、LSP2等储存蛋白[21].蛹期,在蜕皮激素的主导下,约70%的幼虫脂肪体细胞因自噬和凋亡被降解,释放的营养用于支持成虫盘的发育;其余约30%的脂肪体细胞则重新聚集,体积缩小,脂滴合成减少,转而合成成虫特异性蛋白,并分化为成虫脂肪体前体.成虫期,脂肪体主要分布于腹部背板下方,在能量稳态调控、繁殖支持及免疫防御等方面发挥重要作用. ...
Serpent, a GATA-like transcription factor gene, induces fat-cell development in Drosophila melanogaster
1
2001
... 果蝇脂肪体(fat body)和绛色细胞(oenocytes)承担着营养储存、代谢调节、免疫防御等关键的生理功能,与哺乳动物肝脏的功能具有一定的相似性(图1C).脂肪体起源于腹部中胚层(A2-A8体节腹侧),由脂肪体细胞构成,其发育历经胚胎形成、幼虫成熟、蛹期重塑和成虫分化4个阶段,各阶段均受到多种转录因子、激素及信号通路的精准调控[16-17].在胚胎发育早期,中胚层细胞在转录因子Srp(Serpent)[18]的调控下,特化为脂肪体前体细胞(fat body precursor cell,FBP).在胚胎第13∼16期,FBP脱离中胚层,经过迁移和聚集形成分节排列的细胞团,构成脂肪体雏形,此时细胞内尚未形成脂滴,主要为胚胎晚期发育提供基础营养支持.进入幼虫期(L1∼L3)后,脂肪体细胞以体积增大为主[19-20],至L3期末细胞直径可达100 μm以上,与此同时,细胞中开始大量合成并积累脂滴和贮存蛋白(larval serum protein,LSP)1、LSP2等储存蛋白[21].蛹期,在蜕皮激素的主导下,约70%的幼虫脂肪体细胞因自噬和凋亡被降解,释放的营养用于支持成虫盘的发育;其余约30%的脂肪体细胞则重新聚集,体积缩小,脂滴合成减少,转而合成成虫特异性蛋白,并分化为成虫脂肪体前体.成虫期,脂肪体主要分布于腹部背板下方,在能量稳态调控、繁殖支持及免疫防御等方面发挥重要作用. ...
Maturation and degeneration of the fat body in the Drosophila larva and pupa as revealed by morphometric analysis
1
1988
... 果蝇脂肪体(fat body)和绛色细胞(oenocytes)承担着营养储存、代谢调节、免疫防御等关键的生理功能,与哺乳动物肝脏的功能具有一定的相似性(图1C).脂肪体起源于腹部中胚层(A2-A8体节腹侧),由脂肪体细胞构成,其发育历经胚胎形成、幼虫成熟、蛹期重塑和成虫分化4个阶段,各阶段均受到多种转录因子、激素及信号通路的精准调控[16-17].在胚胎发育早期,中胚层细胞在转录因子Srp(Serpent)[18]的调控下,特化为脂肪体前体细胞(fat body precursor cell,FBP).在胚胎第13∼16期,FBP脱离中胚层,经过迁移和聚集形成分节排列的细胞团,构成脂肪体雏形,此时细胞内尚未形成脂滴,主要为胚胎晚期发育提供基础营养支持.进入幼虫期(L1∼L3)后,脂肪体细胞以体积增大为主[19-20],至L3期末细胞直径可达100 μm以上,与此同时,细胞中开始大量合成并积累脂滴和贮存蛋白(larval serum protein,LSP)1、LSP2等储存蛋白[21].蛹期,在蜕皮激素的主导下,约70%的幼虫脂肪体细胞因自噬和凋亡被降解,释放的营养用于支持成虫盘的发育;其余约30%的脂肪体细胞则重新聚集,体积缩小,脂滴合成减少,转而合成成虫特异性蛋白,并分化为成虫脂肪体前体.成虫期,脂肪体主要分布于腹部背板下方,在能量稳态调控、繁殖支持及免疫防御等方面发挥重要作用. ...
Environmental control of the cell cycle in Drosophila: nutrition activates mitotic and endore-plicative cells by distinct mechanisms
1
1998
... 果蝇脂肪体(fat body)和绛色细胞(oenocytes)承担着营养储存、代谢调节、免疫防御等关键的生理功能,与哺乳动物肝脏的功能具有一定的相似性(图1C).脂肪体起源于腹部中胚层(A2-A8体节腹侧),由脂肪体细胞构成,其发育历经胚胎形成、幼虫成熟、蛹期重塑和成虫分化4个阶段,各阶段均受到多种转录因子、激素及信号通路的精准调控[16-17].在胚胎发育早期,中胚层细胞在转录因子Srp(Serpent)[18]的调控下,特化为脂肪体前体细胞(fat body precursor cell,FBP).在胚胎第13∼16期,FBP脱离中胚层,经过迁移和聚集形成分节排列的细胞团,构成脂肪体雏形,此时细胞内尚未形成脂滴,主要为胚胎晚期发育提供基础营养支持.进入幼虫期(L1∼L3)后,脂肪体细胞以体积增大为主[19-20],至L3期末细胞直径可达100 μm以上,与此同时,细胞中开始大量合成并积累脂滴和贮存蛋白(larval serum protein,LSP)1、LSP2等储存蛋白[21].蛹期,在蜕皮激素的主导下,约70%的幼虫脂肪体细胞因自噬和凋亡被降解,释放的营养用于支持成虫盘的发育;其余约30%的脂肪体细胞则重新聚集,体积缩小,脂滴合成减少,转而合成成虫特异性蛋白,并分化为成虫脂肪体前体.成虫期,脂肪体主要分布于腹部背板下方,在能量稳态调控、繁殖支持及免疫防御等方面发挥重要作用. ...
Fat body remodeling and homeostasis control in Drosophila
1
2016
... 果蝇脂肪体(fat body)和绛色细胞(oenocytes)承担着营养储存、代谢调节、免疫防御等关键的生理功能,与哺乳动物肝脏的功能具有一定的相似性(图1C).脂肪体起源于腹部中胚层(A2-A8体节腹侧),由脂肪体细胞构成,其发育历经胚胎形成、幼虫成熟、蛹期重塑和成虫分化4个阶段,各阶段均受到多种转录因子、激素及信号通路的精准调控[16-17].在胚胎发育早期,中胚层细胞在转录因子Srp(Serpent)[18]的调控下,特化为脂肪体前体细胞(fat body precursor cell,FBP).在胚胎第13∼16期,FBP脱离中胚层,经过迁移和聚集形成分节排列的细胞团,构成脂肪体雏形,此时细胞内尚未形成脂滴,主要为胚胎晚期发育提供基础营养支持.进入幼虫期(L1∼L3)后,脂肪体细胞以体积增大为主[19-20],至L3期末细胞直径可达100 μm以上,与此同时,细胞中开始大量合成并积累脂滴和贮存蛋白(larval serum protein,LSP)1、LSP2等储存蛋白[21].蛹期,在蜕皮激素的主导下,约70%的幼虫脂肪体细胞因自噬和凋亡被降解,释放的营养用于支持成虫盘的发育;其余约30%的脂肪体细胞则重新聚集,体积缩小,脂滴合成减少,转而合成成虫特异性蛋白,并分化为成虫脂肪体前体.成虫期,脂肪体主要分布于腹部背板下方,在能量稳态调控、繁殖支持及免疫防御等方面发挥重要作用. ...
Drosophila Spidey/Kar regulates oenocyte growth via PI3-Kinase signaling
1
2016
... 绛色细胞起源于胚胎期体节的腹侧外胚层,是一类特化的分泌细胞,主要功能为合成蜕皮激素前体、角质层脂质及解毒酶,其发育历经胚胎期的起源与分化、幼虫期的成熟与功能建立、蛹期的重塑与成虫期的维持4个阶段[22].在胚胎早期(第10∼12期),腹侧外胚层细胞在sal(spalt major)和en(engrailed)的调控下特化为绛色细胞前体,这些前体细胞于T1∼A7体节形成2∼3个细胞簇,随后经上皮-间质转化脱离基底膜,向体壁内侧迁移并定位于体节侧区.至胚胎第16期,绛色细胞的形态已基本发育完成,但执行其代谢功能的相关酶类尚未开始表达.在幼虫期(L1∼L3龄期),绛色细胞以细胞分裂为主;至L3期末.幼虫的每个体节增至10∼12个细胞,排列成双侧对称的细胞群.幼虫阶段绛色细胞内的粗面内质网与高尔基体显著发达,绛色细胞受保幼激素(juvenile hormone,JH)与雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路的调控,开始表达蜕皮激素合成关键酶(如phantom、disembodied)和脂质合成酶(如fatty acyl-CoA reductase),从而具备合成蜕皮激素前体及表皮蜡质的能力.进入蛹期,绛色细胞在蜕皮激素的主导下发生形态重塑,表现为体积缩小、细胞器更新,部分幼虫来源的绛色细胞凋亡,其余绛色细胞迁移至成虫体壁内侧,分化为成虫绛色细胞,其功能亦随之发生改变,转向合成成虫表皮脂质(如防水蜡质)及解毒酶(如细胞色素P450),以适应成虫期的生存需求[23]. ...
Insect oenocytes: a model system for studying cell-fate specification by Hox genes
1
2001
... 绛色细胞起源于胚胎期体节的腹侧外胚层,是一类特化的分泌细胞,主要功能为合成蜕皮激素前体、角质层脂质及解毒酶,其发育历经胚胎期的起源与分化、幼虫期的成熟与功能建立、蛹期的重塑与成虫期的维持4个阶段[22].在胚胎早期(第10∼12期),腹侧外胚层细胞在sal(spalt major)和en(engrailed)的调控下特化为绛色细胞前体,这些前体细胞于T1∼A7体节形成2∼3个细胞簇,随后经上皮-间质转化脱离基底膜,向体壁内侧迁移并定位于体节侧区.至胚胎第16期,绛色细胞的形态已基本发育完成,但执行其代谢功能的相关酶类尚未开始表达.在幼虫期(L1∼L3龄期),绛色细胞以细胞分裂为主;至L3期末.幼虫的每个体节增至10∼12个细胞,排列成双侧对称的细胞群.幼虫阶段绛色细胞内的粗面内质网与高尔基体显著发达,绛色细胞受保幼激素(juvenile hormone,JH)与雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路的调控,开始表达蜕皮激素合成关键酶(如phantom、disembodied)和脂质合成酶(如fatty acyl-CoA reductase),从而具备合成蜕皮激素前体及表皮蜡质的能力.进入蛹期,绛色细胞在蜕皮激素的主导下发生形态重塑,表现为体积缩小、细胞器更新,部分幼虫来源的绛色细胞凋亡,其余绛色细胞迁移至成虫体壁内侧,分化为成虫绛色细胞,其功能亦随之发生改变,转向合成成虫表皮脂质(如防水蜡质)及解毒酶(如细胞色素P450),以适应成虫期的生存需求[23]. ...
The endoribonuclease Arlr is required to maintain lipid homeostasis by down-regulating lipolytic genes during aging
1
2023
... 果蝇的脂肪体和绛色细胞在代谢功能和调控机制上与哺乳动物代谢器官具有高度保守性,因而成为解析人类代谢疾病(肥胖、糖尿病、脂肪肝)分子机制、筛选致病相关基因及挖掘潜在治疗药物的重要模型,也为理解复杂代谢疾病提供了简化且高效的研究体系.利用果蝇模型,可以筛选与人类代谢疾病相关的药物:例如,特异性敲除脂肪体中脂滴调控基因(如Lsd2)会导致脂滴异常增大,可模拟人类脂质蓄积疾病表型;筛选靶向脂肪体TOR信号通路的抑制剂(如西罗莫司)可改善果蝇的代谢紊乱表型,为人类代谢综合征的治疗提供候选靶点.研究发现,内切核糖核酸酶Arlr(age-related lipid regulator)通过降解脂肪分解相关基因的mRNA维持果蝇脂肪体的脂质稳态[24],进一步印证了果蝇脂肪体在脂质代谢调控机制上与哺乳动物肝脏的保守性,也为解析肝脏代谢疾病中转录水平的调控异常提供了新的分子靶点和研究思路. ...
Drosophila pericardial nephrocyte ultrastructure changes during ageing
1
2018
... 果蝇的“肾脏”结构较为简单,由马氏管(malpighian tubule)和肾原细胞(nephrocyte)组成(图1D).其中马氏管是果蝇主要的排泄及渗透调节器官,它能从血淋巴中清除代谢废物,再通过与后肠(hindgut)的连接将其排出体外,同时调节体内的水盐平衡[25-26].马氏管起源于胚胎期外胚层上皮芽和周围间充质中胚层,发育过程呈现显著的阶段性特征:在胚胎期,马氏管以细胞团的形式增殖并形成四重对称的小管结构,每个小管内均含有尖端细胞,该细胞可通过激活表皮生长因子受体(epidermal growth factor receptor,EGFR)信号促进马氏管的发育[27-30];在幼虫期,马氏管分化为承担主要排泄和渗透调节功能的主细胞与起辅助调节作用的星形细胞,其功能随龄期的增长逐步完善;成虫期,马氏管的形态基本稳定,其下段和输尿管区域的“微小细胞”作为多能干细胞,负责维持细胞更新与功能稳态[31-33].马氏管的发育受Wnt、RET、Janus激酶(Janus kinase,JAK)-信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)等信号通路及Krüppel、Klf15等转录因子的级联调控[34-37],并在滤过结构、生理功能及调控机制上与哺乳动物肾脏具有高度的进化保守性. ...
Using the Drosophila nephrocyte to model podocyte function and disease
1
2017
... 果蝇的“肾脏”结构较为简单,由马氏管(malpighian tubule)和肾原细胞(nephrocyte)组成(图1D).其中马氏管是果蝇主要的排泄及渗透调节器官,它能从血淋巴中清除代谢废物,再通过与后肠(hindgut)的连接将其排出体外,同时调节体内的水盐平衡[25-26].马氏管起源于胚胎期外胚层上皮芽和周围间充质中胚层,发育过程呈现显著的阶段性特征:在胚胎期,马氏管以细胞团的形式增殖并形成四重对称的小管结构,每个小管内均含有尖端细胞,该细胞可通过激活表皮生长因子受体(epidermal growth factor receptor,EGFR)信号促进马氏管的发育[27-30];在幼虫期,马氏管分化为承担主要排泄和渗透调节功能的主细胞与起辅助调节作用的星形细胞,其功能随龄期的增长逐步完善;成虫期,马氏管的形态基本稳定,其下段和输尿管区域的“微小细胞”作为多能干细胞,负责维持细胞更新与功能稳态[31-33].马氏管的发育受Wnt、RET、Janus激酶(Janus kinase,JAK)-信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)等信号通路及Krüppel、Klf15等转录因子的级联调控[34-37],并在滤过结构、生理功能及调控机制上与哺乳动物肾脏具有高度的进化保守性. ...
Drosophila melanogaster as an emerging translational model of human nephrolithiasis
1
2013
... 果蝇的“肾脏”结构较为简单,由马氏管(malpighian tubule)和肾原细胞(nephrocyte)组成(图1D).其中马氏管是果蝇主要的排泄及渗透调节器官,它能从血淋巴中清除代谢废物,再通过与后肠(hindgut)的连接将其排出体外,同时调节体内的水盐平衡[25-26].马氏管起源于胚胎期外胚层上皮芽和周围间充质中胚层,发育过程呈现显著的阶段性特征:在胚胎期,马氏管以细胞团的形式增殖并形成四重对称的小管结构,每个小管内均含有尖端细胞,该细胞可通过激活表皮生长因子受体(epidermal growth factor receptor,EGFR)信号促进马氏管的发育[27-30];在幼虫期,马氏管分化为承担主要排泄和渗透调节功能的主细胞与起辅助调节作用的星形细胞,其功能随龄期的增长逐步完善;成虫期,马氏管的形态基本稳定,其下段和输尿管区域的“微小细胞”作为多能干细胞,负责维持细胞更新与功能稳态[31-33].马氏管的发育受Wnt、RET、Janus激酶(Janus kinase,JAK)-信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)等信号通路及Krüppel、Klf15等转录因子的级联调控[34-37],并在滤过结构、生理功能及调控机制上与哺乳动物肾脏具有高度的进化保守性. ...
Ush regulates hemocyte-specific gene expression, fatty acid metabolism and cell cycle progression and cooperates with dNuRD to orchestrate hematopoiesis
0
2021
The development and functions of oenocytes
0
2014
Lessons learned about adult kidney stem cells from the Malpighian tubules of Drosophila
1
2008
... 果蝇的“肾脏”结构较为简单,由马氏管(malpighian tubule)和肾原细胞(nephrocyte)组成(图1D).其中马氏管是果蝇主要的排泄及渗透调节器官,它能从血淋巴中清除代谢废物,再通过与后肠(hindgut)的连接将其排出体外,同时调节体内的水盐平衡[25-26].马氏管起源于胚胎期外胚层上皮芽和周围间充质中胚层,发育过程呈现显著的阶段性特征:在胚胎期,马氏管以细胞团的形式增殖并形成四重对称的小管结构,每个小管内均含有尖端细胞,该细胞可通过激活表皮生长因子受体(epidermal growth factor receptor,EGFR)信号促进马氏管的发育[27-30];在幼虫期,马氏管分化为承担主要排泄和渗透调节功能的主细胞与起辅助调节作用的星形细胞,其功能随龄期的增长逐步完善;成虫期,马氏管的形态基本稳定,其下段和输尿管区域的“微小细胞”作为多能干细胞,负责维持细胞更新与功能稳态[31-33].马氏管的发育受Wnt、RET、Janus激酶(Janus kinase,JAK)-信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)等信号通路及Krüppel、Klf15等转录因子的级联调控[34-37],并在滤过结构、生理功能及调控机制上与哺乳动物肾脏具有高度的进化保守性. ...
Renal tubule development in Drosophila: a closer look at the cellular level
1
2005
... 果蝇的“肾脏”结构较为简单,由马氏管(malpighian tubule)和肾原细胞(nephrocyte)组成(图1D).其中马氏管是果蝇主要的排泄及渗透调节器官,它能从血淋巴中清除代谢废物,再通过与后肠(hindgut)的连接将其排出体外,同时调节体内的水盐平衡[25-26].马氏管起源于胚胎期外胚层上皮芽和周围间充质中胚层,发育过程呈现显著的阶段性特征:在胚胎期,马氏管以细胞团的形式增殖并形成四重对称的小管结构,每个小管内均含有尖端细胞,该细胞可通过激活表皮生长因子受体(epidermal growth factor receptor,EGFR)信号促进马氏管的发育[27-30];在幼虫期,马氏管分化为承担主要排泄和渗透调节功能的主细胞与起辅助调节作用的星形细胞,其功能随龄期的增长逐步完善;成虫期,马氏管的形态基本稳定,其下段和输尿管区域的“微小细胞”作为多能干细胞,负责维持细胞更新与功能稳态[31-33].马氏管的发育受Wnt、RET、Janus激酶(Janus kinase,JAK)-信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)等信号通路及Krüppel、Klf15等转录因子的级联调控[34-37],并在滤过结构、生理功能及调控机制上与哺乳动物肾脏具有高度的进化保守性. ...
The adult Drosophila Malpighian tubules are maintained by multipotent stem cells
0
2007
Multiple signalling pathways establish cell fate and cell number in Drosophila Malpighian tubules
1
2000
... 果蝇的“肾脏”结构较为简单,由马氏管(malpighian tubule)和肾原细胞(nephrocyte)组成(图1D).其中马氏管是果蝇主要的排泄及渗透调节器官,它能从血淋巴中清除代谢废物,再通过与后肠(hindgut)的连接将其排出体外,同时调节体内的水盐平衡[25-26].马氏管起源于胚胎期外胚层上皮芽和周围间充质中胚层,发育过程呈现显著的阶段性特征:在胚胎期,马氏管以细胞团的形式增殖并形成四重对称的小管结构,每个小管内均含有尖端细胞,该细胞可通过激活表皮生长因子受体(epidermal growth factor receptor,EGFR)信号促进马氏管的发育[27-30];在幼虫期,马氏管分化为承担主要排泄和渗透调节功能的主细胞与起辅助调节作用的星形细胞,其功能随龄期的增长逐步完善;成虫期,马氏管的形态基本稳定,其下段和输尿管区域的“微小细胞”作为多能干细胞,负责维持细胞更新与功能稳态[31-33].马氏管的发育受Wnt、RET、Janus激酶(Janus kinase,JAK)-信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)等信号通路及Krüppel、Klf15等转录因子的级联调控[34-37],并在滤过结构、生理功能及调控机制上与哺乳动物肾脏具有高度的进化保守性. ...
The cellular basis of kidney development
1
2006
... 果蝇的“肾脏”结构较为简单,由马氏管(malpighian tubule)和肾原细胞(nephrocyte)组成(图1D).其中马氏管是果蝇主要的排泄及渗透调节器官,它能从血淋巴中清除代谢废物,再通过与后肠(hindgut)的连接将其排出体外,同时调节体内的水盐平衡[25-26].马氏管起源于胚胎期外胚层上皮芽和周围间充质中胚层,发育过程呈现显著的阶段性特征:在胚胎期,马氏管以细胞团的形式增殖并形成四重对称的小管结构,每个小管内均含有尖端细胞,该细胞可通过激活表皮生长因子受体(epidermal growth factor receptor,EGFR)信号促进马氏管的发育[27-30];在幼虫期,马氏管分化为承担主要排泄和渗透调节功能的主细胞与起辅助调节作用的星形细胞,其功能随龄期的增长逐步完善;成虫期,马氏管的形态基本稳定,其下段和输尿管区域的“微小细胞”作为多能干细胞,负责维持细胞更新与功能稳态[31-33].马氏管的发育受Wnt、RET、Janus激酶(Janus kinase,JAK)-信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)等信号通路及Krüppel、Klf15等转录因子的级联调控[34-37],并在滤过结构、生理功能及调控机制上与哺乳动物肾脏具有高度的进化保守性. ...
Secreted molecules in metanephric induction
0
2000
Regulation of Krüppel expression in the anlage of the Malpighian tubules in the Drosophila embryo
0
1990
Klf15 is critical for the development and differentiation of Drosophila nephrocytes
1
2015
... 果蝇的“肾脏”结构较为简单,由马氏管(malpighian tubule)和肾原细胞(nephrocyte)组成(图1D).其中马氏管是果蝇主要的排泄及渗透调节器官,它能从血淋巴中清除代谢废物,再通过与后肠(hindgut)的连接将其排出体外,同时调节体内的水盐平衡[25-26].马氏管起源于胚胎期外胚层上皮芽和周围间充质中胚层,发育过程呈现显著的阶段性特征:在胚胎期,马氏管以细胞团的形式增殖并形成四重对称的小管结构,每个小管内均含有尖端细胞,该细胞可通过激活表皮生长因子受体(epidermal growth factor receptor,EGFR)信号促进马氏管的发育[27-30];在幼虫期,马氏管分化为承担主要排泄和渗透调节功能的主细胞与起辅助调节作用的星形细胞,其功能随龄期的增长逐步完善;成虫期,马氏管的形态基本稳定,其下段和输尿管区域的“微小细胞”作为多能干细胞,负责维持细胞更新与功能稳态[31-33].马氏管的发育受Wnt、RET、Janus激酶(Janus kinase,JAK)-信号转导及转录激活蛋白(signal transducer and activator of transcription,STAT)等信号通路及Krüppel、Klf15等转录因子的级联调控[34-37],并在滤过结构、生理功能及调控机制上与哺乳动物肾脏具有高度的进化保守性. ...
Cubilin and amnionless mediate protein reabsorption in Drosophila nephrocytes
1
2013
... 果蝇肾原细胞的主要功能之一是过滤血淋巴,包括摄取、内吞和处理血淋巴中的毒素及代谢废物.果蝇的肾原细胞可分为副心肌肾原细胞(pericardial nephrocyte)和花环肾原细胞(garland nephrocyte).花环肾原细胞呈项链状排列在食管周围,位于前胃顶部;副心肌肾原细胞则沿心管分布.在果蝇胚胎阶段,花环肾原细胞是唯一的功能性滤过细胞;在幼虫和成虫阶段,副心肌肾原细胞则成为主要的滤过细胞[38].副心肌肾原细胞在胚胎阶段约为120个,在幼虫和成虫阶段约为40个,它们排列在心脏两侧[39]. ...
Sns and Kirre, the Drosophila orthologs of Nephrin and Neph1, direct adhesion, fusion and formation of a slit diaphragm-like structure in insect nephrocytes
1
2009
... 果蝇肾原细胞的主要功能之一是过滤血淋巴,包括摄取、内吞和处理血淋巴中的毒素及代谢废物.果蝇的肾原细胞可分为副心肌肾原细胞(pericardial nephrocyte)和花环肾原细胞(garland nephrocyte).花环肾原细胞呈项链状排列在食管周围,位于前胃顶部;副心肌肾原细胞则沿心管分布.在果蝇胚胎阶段,花环肾原细胞是唯一的功能性滤过细胞;在幼虫和成虫阶段,副心肌肾原细胞则成为主要的滤过细胞[38].副心肌肾原细胞在胚胎阶段约为120个,在幼虫和成虫阶段约为40个,它们排列在心脏两侧[39]. ...
Bicaudal C mutation causes myc and TOR pathway up-regulation and polycystic kidney disease-like phenotypes in Drosophila
1
2017
... 果蝇BicC基因突变会导致马氏管的管腔扩大和囊肿形成,其表型与人类多囊肾病(polycystic kidney disease,PKD)高度相似.研究发现,BicC基因突变通过上调Myc表达和激活TOR信号通路引发病变,而使用西罗莫司抑制TOR通路可有效改善果蝇马氏管囊肿的表型[40],这为人类PKD的靶向治疗提供了方向.此外,果蝇模型中Tbc1d8b基因功能的缺失会导致肾原细胞损伤,可用于模拟人类类固醇耐药性肾病综合征(steroid-resistant nephrotic syndrome,SRNS);也有研究表明,人类Nup160基因可挽救果蝇Nup160突变引起的肾原细胞功能缺陷[41],证实了该类疾病致病机制的跨物种保守性. ...
TBC1D8B mutations implicate RAB11-dependent vesicular trafficking in the pathogenesis of nephrotic syndrome
1
2019
... 果蝇BicC基因突变会导致马氏管的管腔扩大和囊肿形成,其表型与人类多囊肾病(polycystic kidney disease,PKD)高度相似.研究发现,BicC基因突变通过上调Myc表达和激活TOR信号通路引发病变,而使用西罗莫司抑制TOR通路可有效改善果蝇马氏管囊肿的表型[40],这为人类PKD的靶向治疗提供了方向.此外,果蝇模型中Tbc1d8b基因功能的缺失会导致肾原细胞损伤,可用于模拟人类类固醇耐药性肾病综合征(steroid-resistant nephrotic syndrome,SRNS);也有研究表明,人类Nup160基因可挽救果蝇Nup160突变引起的肾原细胞功能缺陷[41],证实了该类疾病致病机制的跨物种保守性. ...
Development and function of the Drosophila Tracheal system
2
2018
... 果蝇的“肺脏”是昆虫特有的呼吸系统,由上皮小管构成(图1E),通过气孔与外界相通.其发育始于胚胎期第10阶段,历经气管原基特化、分支形态发生和功能成熟3个时期[42],与哺乳动物肺脏的分级分支过程具有进化保守性.在胚胎第10阶段,背部外胚层细胞首先开始表达转录因子Trh(trachealess),启动气管原基的特化.气管原基形成后,原基细胞开始表达受体酪氨酸激酶Btl(breathless),Btl被果蝇中的成纤维细胞生长因子配体Bnl(branchless)激活,随后启动初级气管分支过程.每个分支向特定的靶组织迁移,例如背分支向背部表皮迁移,内脏分支向肠道迁移,神经节分支向腹神经索迁移[43].在气管系统成熟的过程中,管腔通过改变细胞形状和机械反馈机制(如几丁质与肌动蛋白的相互作用)不断优化自身几何结构,最终形成含环纹褶皱的角质层.该结构能够清除管腔内的大分子并充满气体以适配气流;最终微气管末端与靶细胞建立接触,不仅能实现高效的气体交换,还能感知氧水平,以适应外界环境变化[42]. ...
... [42]. ...
The Drosophila FGF-R homolog is expressed in the embryonic tracheal system and appears to be required for directed tracheal cell extension
1
1991
... 果蝇的“肺脏”是昆虫特有的呼吸系统,由上皮小管构成(图1E),通过气孔与外界相通.其发育始于胚胎期第10阶段,历经气管原基特化、分支形态发生和功能成熟3个时期[42],与哺乳动物肺脏的分级分支过程具有进化保守性.在胚胎第10阶段,背部外胚层细胞首先开始表达转录因子Trh(trachealess),启动气管原基的特化.气管原基形成后,原基细胞开始表达受体酪氨酸激酶Btl(breathless),Btl被果蝇中的成纤维细胞生长因子配体Bnl(branchless)激活,随后启动初级气管分支过程.每个分支向特定的靶组织迁移,例如背分支向背部表皮迁移,内脏分支向肠道迁移,神经节分支向腹神经索迁移[43].在气管系统成熟的过程中,管腔通过改变细胞形状和机械反馈机制(如几丁质与肌动蛋白的相互作用)不断优化自身几何结构,最终形成含环纹褶皱的角质层.该结构能够清除管腔内的大分子并充满气体以适配气流;最终微气管末端与靶细胞建立接触,不仅能实现高效的气体交换,还能感知氧水平,以适应外界环境变化[42]. ...
The control of branching morphogenesis
1
2013
... 在果蝇气管系统的发育中,成纤维细胞生长因子(fibroblast growth factor,FGF)信号Bnl/Btl负责驱动气管树状分支的形成,Hh信号负责调控微气管末端细胞的分化,二者功能与哺乳动物中FGF10/FGFR2和Shh信号通路在肺芽分支、肺泡分化中的作用一致[44].果蝇Btl突变体可模拟人类先天性肺气道畸形(congenital pulmonary airway malformation,CPAM),而sprouty作为FGF信号通路的负调控因子,可有效挽救肺气管分支缺陷[45].单细胞测序结果进一步表明,糖基化修饰通过Notch信号调控果蝇气管的干细胞命运决定,这与哺乳动物肺发育中的Notch通路功能具有高度保守性[46]. ...
Sprouty encodes a novel antagonist of FGF signaling that patterns apical branching of the Drosophila airways
1
1998
... 在果蝇气管系统的发育中,成纤维细胞生长因子(fibroblast growth factor,FGF)信号Bnl/Btl负责驱动气管树状分支的形成,Hh信号负责调控微气管末端细胞的分化,二者功能与哺乳动物中FGF10/FGFR2和Shh信号通路在肺芽分支、肺泡分化中的作用一致[44].果蝇Btl突变体可模拟人类先天性肺气道畸形(congenital pulmonary airway malformation,CPAM),而sprouty作为FGF信号通路的负调控因子,可有效挽救肺气管分支缺陷[45].单细胞测序结果进一步表明,糖基化修饰通过Notch信号调控果蝇气管的干细胞命运决定,这与哺乳动物肺发育中的Notch通路功能具有高度保守性[46]. ...
A single-cell atlas of Drosophila trachea reveals glycosylation-mediated Notch signaling in cell fate specification
1
2024
... 在果蝇气管系统的发育中,成纤维细胞生长因子(fibroblast growth factor,FGF)信号Bnl/Btl负责驱动气管树状分支的形成,Hh信号负责调控微气管末端细胞的分化,二者功能与哺乳动物中FGF10/FGFR2和Shh信号通路在肺芽分支、肺泡分化中的作用一致[44].果蝇Btl突变体可模拟人类先天性肺气道畸形(congenital pulmonary airway malformation,CPAM),而sprouty作为FGF信号通路的负调控因子,可有效挽救肺气管分支缺陷[45].单细胞测序结果进一步表明,糖基化修饰通过Notch信号调控果蝇气管的干细胞命运决定,这与哺乳动物肺发育中的Notch通路功能具有高度保守性[46]. ...
FGF9 and FGF18 in idiopathic pulmonary fibrosis promote survival and migration and inhibit myofibroblast differentiation of human lung fibroblasts in vitro
1
2016
... 果蝇模型凭借其遗传操作简单和高通量筛选便捷等优势,已成为构建人类疾病模型和进行药物筛选及研发的关键平台.例如,基于果蝇气管系统与哺乳动物肺脏在FGF信号调控分支发育上的保守性,通过果蝇气管分支缺陷模型筛选出的FGF通路抑制剂已用于人类肺纤维化临床前研究[47];基于果蝇背血管与哺乳动物心脏在心肌细胞分化过程中的高度相似性,利用果蝇背血管发育模型揭示人类先天性心脏病的部分致病基因(如Nkx2-5)及相关信号通路的调控机制(如Dpp/Wg信号通路)[14-15];脂肪体与绛色细胞的代谢调控机制为人类肥胖、脂肪肝等代谢性疾病提供了从基因功能解析到药物筛选的系统研究脉络;马氏管与肾原细胞在滤过-排泄系统方面的保守性,则有助于阐明多囊肾、肾癌等疾病中纤毛功能异常及相关信号通路机制;气管系统分支形态发生中的FGF信号调控,为先天性肺气道畸形等疾病的机制研究提供了跨物种参照.此外,果蝇的神经系统相对简单,由约10万个神经元组成,但这些神经元之间的连接方式及其功能特点与人类大脑具有惊人的相似性,这种特征使果蝇成为研究癫痫等神经系统疾病的理想模型.未来,随着更多保守调控机制的解析,果蝇模型在器官发育异常相关疾病的机制研究与治疗策略开发中,将进一步发挥其“以简驭繁”的独特优势. ...