Book review: insect physiological ecology. mechanisms and patterns
1
2005
... 几乎所有动物都面临着维持糖代谢稳态的挑战.糖代谢稳态是生物体维持内部能量状态稳定的关键过程.黑腹果蝇(Drosophila melanogaster,以下简称果蝇)体型小、繁殖快、基因组相对简单,约60%的基因与人类高度同源,且众多生理机制与人类相似,加之成熟的遗传操作技术使其成为研究糖代谢稳态的理想模式生物.与脊椎动物类似,果蝇的糖代谢稳态也可以通过检测循环糖浓度的变化,即果蝇的血淋巴葡萄糖及海藻糖的浓度来实现[1].糖代谢稳态的调控涉及多种肽类激素的协调作用,肽类激素通过自分泌、旁分泌和内分泌的方式在不同器官间传递[2],影响器官内糖物质的储存与动用,进而调控昆虫的发育和行为等生理进程.其中,类胰高血糖素-脂动激素(adipokinetic hormone,AKH)的表达水平对糖代谢稳态起着关键作用,其可通过心侧体(corpora cardiaca)和胰岛素生成细胞(insulin-producing cells,IPCs)分泌[3-5],它们被视为脊椎动物胰腺α和β细胞的同源组织.AKH和果蝇类胰岛素样肽(Drosophila insulin-like peptides,DILPs)分别具有促进糖物质动用和储存的功能,它们传递至靶标器官如脂肪体等,从而调节血淋巴中葡萄糖等能量物质的表达水平[4].近年来研究显示,果蝇心侧体除了分泌AKH外,还能分泌其他肽激素来调节糖代谢稳态,且心侧体在变态发育、取食、衰老中也发挥重要功能,这些功能进一步凸显出其在动物发育全周期生理过程中的关键地位.对心侧体的研究将有助于科研工作者更加全面地了解动物糖代谢稳态的调控机制. ...
Interorgan communication pathways in physiology: focus on Drosophila
1
2016
... 几乎所有动物都面临着维持糖代谢稳态的挑战.糖代谢稳态是生物体维持内部能量状态稳定的关键过程.黑腹果蝇(Drosophila melanogaster,以下简称果蝇)体型小、繁殖快、基因组相对简单,约60%的基因与人类高度同源,且众多生理机制与人类相似,加之成熟的遗传操作技术使其成为研究糖代谢稳态的理想模式生物.与脊椎动物类似,果蝇的糖代谢稳态也可以通过检测循环糖浓度的变化,即果蝇的血淋巴葡萄糖及海藻糖的浓度来实现[1].糖代谢稳态的调控涉及多种肽类激素的协调作用,肽类激素通过自分泌、旁分泌和内分泌的方式在不同器官间传递[2],影响器官内糖物质的储存与动用,进而调控昆虫的发育和行为等生理进程.其中,类胰高血糖素-脂动激素(adipokinetic hormone,AKH)的表达水平对糖代谢稳态起着关键作用,其可通过心侧体(corpora cardiaca)和胰岛素生成细胞(insulin-producing cells,IPCs)分泌[3-5],它们被视为脊椎动物胰腺α和β细胞的同源组织.AKH和果蝇类胰岛素样肽(Drosophila insulin-like peptides,DILPs)分别具有促进糖物质动用和储存的功能,它们传递至靶标器官如脂肪体等,从而调节血淋巴中葡萄糖等能量物质的表达水平[4].近年来研究显示,果蝇心侧体除了分泌AKH外,还能分泌其他肽激素来调节糖代谢稳态,且心侧体在变态发育、取食、衰老中也发挥重要功能,这些功能进一步凸显出其在动物发育全周期生理过程中的关键地位.对心侧体的研究将有助于科研工作者更加全面地了解动物糖代谢稳态的调控机制. ...
Nutrient-dependent expression of insulin-like peptides from neuroendocrine cells in the CNS contributes to growth regulation in Drosophila
1
2002
... 几乎所有动物都面临着维持糖代谢稳态的挑战.糖代谢稳态是生物体维持内部能量状态稳定的关键过程.黑腹果蝇(Drosophila melanogaster,以下简称果蝇)体型小、繁殖快、基因组相对简单,约60%的基因与人类高度同源,且众多生理机制与人类相似,加之成熟的遗传操作技术使其成为研究糖代谢稳态的理想模式生物.与脊椎动物类似,果蝇的糖代谢稳态也可以通过检测循环糖浓度的变化,即果蝇的血淋巴葡萄糖及海藻糖的浓度来实现[1].糖代谢稳态的调控涉及多种肽类激素的协调作用,肽类激素通过自分泌、旁分泌和内分泌的方式在不同器官间传递[2],影响器官内糖物质的储存与动用,进而调控昆虫的发育和行为等生理进程.其中,类胰高血糖素-脂动激素(adipokinetic hormone,AKH)的表达水平对糖代谢稳态起着关键作用,其可通过心侧体(corpora cardiaca)和胰岛素生成细胞(insulin-producing cells,IPCs)分泌[3-5],它们被视为脊椎动物胰腺α和β细胞的同源组织.AKH和果蝇类胰岛素样肽(Drosophila insulin-like peptides,DILPs)分别具有促进糖物质动用和储存的功能,它们传递至靶标器官如脂肪体等,从而调节血淋巴中葡萄糖等能量物质的表达水平[4].近年来研究显示,果蝇心侧体除了分泌AKH外,还能分泌其他肽激素来调节糖代谢稳态,且心侧体在变态发育、取食、衰老中也发挥重要功能,这些功能进一步凸显出其在动物发育全周期生理过程中的关键地位.对心侧体的研究将有助于科研工作者更加全面地了解动物糖代谢稳态的调控机制. ...
Conserved mechanisms of glucose sensing and regulation by Drosophila corpora cardiaca cells
4
2004
... 几乎所有动物都面临着维持糖代谢稳态的挑战.糖代谢稳态是生物体维持内部能量状态稳定的关键过程.黑腹果蝇(Drosophila melanogaster,以下简称果蝇)体型小、繁殖快、基因组相对简单,约60%的基因与人类高度同源,且众多生理机制与人类相似,加之成熟的遗传操作技术使其成为研究糖代谢稳态的理想模式生物.与脊椎动物类似,果蝇的糖代谢稳态也可以通过检测循环糖浓度的变化,即果蝇的血淋巴葡萄糖及海藻糖的浓度来实现[1].糖代谢稳态的调控涉及多种肽类激素的协调作用,肽类激素通过自分泌、旁分泌和内分泌的方式在不同器官间传递[2],影响器官内糖物质的储存与动用,进而调控昆虫的发育和行为等生理进程.其中,类胰高血糖素-脂动激素(adipokinetic hormone,AKH)的表达水平对糖代谢稳态起着关键作用,其可通过心侧体(corpora cardiaca)和胰岛素生成细胞(insulin-producing cells,IPCs)分泌[3-5],它们被视为脊椎动物胰腺α和β细胞的同源组织.AKH和果蝇类胰岛素样肽(Drosophila insulin-like peptides,DILPs)分别具有促进糖物质动用和储存的功能,它们传递至靶标器官如脂肪体等,从而调节血淋巴中葡萄糖等能量物质的表达水平[4].近年来研究显示,果蝇心侧体除了分泌AKH外,还能分泌其他肽激素来调节糖代谢稳态,且心侧体在变态发育、取食、衰老中也发挥重要功能,这些功能进一步凸显出其在动物发育全周期生理过程中的关键地位.对心侧体的研究将有助于科研工作者更加全面地了解动物糖代谢稳态的调控机制. ...
... 果蝇胰岛素样肽1(Drosophila insulin-like peptide 1,DILP1)和DILP2在果蝇心侧体的功能调控中具有复杂的相互作用.DILP2的缺失会上调DILP1的表达,且这种上调是DILP2突变果蝇中延长寿命和增加AKH表达所必需的.具体来说,DILP2主要在胚胎和成虫阶段表达;在正常发育过程中,DILP1主要在蛹期表达,但在DILP2突变的成虫中,其表达显著增加[5].这表明DILP2对DILP1具有负调控作用,且DILP1在DILP2缺失的情况下发挥作用,影响果蝇的寿命和AKH的表达[48].当营养充足时,DILP2由胰岛素合成细胞分泌,其可抑制AKH的释放,从而维持血糖稳定;而当营养匮乏时,DILP2的分泌减少,AKH释放增加,脂肪分解和糖原分解增加,为果蝇存活提供能量[4,49].研究表明,DILP1和DILP2可能通过不同的信号通路来影响心侧体的功能.例如,DILP1可能通过调节心侧体细胞内胰岛素受体底物(insulin receptor substrate)蛋白的活性来影响AKH分泌,而DILP2则可能通过影响心侧体细胞的增殖和分化来间接调节AKH的合成.DILP1在DILP2缺失的情况下表达增加,其或可通过影响AKH的表达和分泌,调节能量代谢,此外,DILP1的表达与果蝇的寿命延长有关[48,50]. ...
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
... 心侧体在果蝇的多种生理过程中发挥着关键作用,其不仅可以通过分泌肽激素远程调控新陈代谢,心侧体的神经还可以投射至成虫和幼虫的心脏、食道、中枢神经系统、幼虫前胸腺以及成虫嗉囊等组织,直接影响组织功能[4, 22].心侧体轴突投射至心脏,可刺激心脏收缩以促进AKH向靶器官的扩散[73];投射至幼虫中央神经系统的胰岛素合成细胞,可调节DILP3的糖依赖性分泌[74];投射至前胸腺,可调控幼虫发育时间[75];投射至成虫嗉囊,可促进嗉囊排空[22].心侧体通过其分泌的激素和神经连接,在糖代谢、变态发育、取食行为和睡眠调节等方面展现出复杂而精确的调控机制(图3). ...
An evolutionarily conserved function of the Drosophila insulin receptor and insulin-like peptides in growth control
5
2001
... 几乎所有动物都面临着维持糖代谢稳态的挑战.糖代谢稳态是生物体维持内部能量状态稳定的关键过程.黑腹果蝇(Drosophila melanogaster,以下简称果蝇)体型小、繁殖快、基因组相对简单,约60%的基因与人类高度同源,且众多生理机制与人类相似,加之成熟的遗传操作技术使其成为研究糖代谢稳态的理想模式生物.与脊椎动物类似,果蝇的糖代谢稳态也可以通过检测循环糖浓度的变化,即果蝇的血淋巴葡萄糖及海藻糖的浓度来实现[1].糖代谢稳态的调控涉及多种肽类激素的协调作用,肽类激素通过自分泌、旁分泌和内分泌的方式在不同器官间传递[2],影响器官内糖物质的储存与动用,进而调控昆虫的发育和行为等生理进程.其中,类胰高血糖素-脂动激素(adipokinetic hormone,AKH)的表达水平对糖代谢稳态起着关键作用,其可通过心侧体(corpora cardiaca)和胰岛素生成细胞(insulin-producing cells,IPCs)分泌[3-5],它们被视为脊椎动物胰腺α和β细胞的同源组织.AKH和果蝇类胰岛素样肽(Drosophila insulin-like peptides,DILPs)分别具有促进糖物质动用和储存的功能,它们传递至靶标器官如脂肪体等,从而调节血淋巴中葡萄糖等能量物质的表达水平[4].近年来研究显示,果蝇心侧体除了分泌AKH外,还能分泌其他肽激素来调节糖代谢稳态,且心侧体在变态发育、取食、衰老中也发挥重要功能,这些功能进一步凸显出其在动物发育全周期生理过程中的关键地位.对心侧体的研究将有助于科研工作者更加全面地了解动物糖代谢稳态的调控机制. ...
... 果蝇胰岛素样肽1(Drosophila insulin-like peptide 1,DILP1)和DILP2在果蝇心侧体的功能调控中具有复杂的相互作用.DILP2的缺失会上调DILP1的表达,且这种上调是DILP2突变果蝇中延长寿命和增加AKH表达所必需的.具体来说,DILP2主要在胚胎和成虫阶段表达;在正常发育过程中,DILP1主要在蛹期表达,但在DILP2突变的成虫中,其表达显著增加[5].这表明DILP2对DILP1具有负调控作用,且DILP1在DILP2缺失的情况下发挥作用,影响果蝇的寿命和AKH的表达[48].当营养充足时,DILP2由胰岛素合成细胞分泌,其可抑制AKH的释放,从而维持血糖稳定;而当营养匮乏时,DILP2的分泌减少,AKH释放增加,脂肪分解和糖原分解增加,为果蝇存活提供能量[4,49].研究表明,DILP1和DILP2可能通过不同的信号通路来影响心侧体的功能.例如,DILP1可能通过调节心侧体细胞内胰岛素受体底物(insulin receptor substrate)蛋白的活性来影响AKH分泌,而DILP2则可能通过影响心侧体细胞的增殖和分化来间接调节AKH的合成.DILP1在DILP2缺失的情况下表达增加,其或可通过影响AKH的表达和分泌,调节能量代谢,此外,DILP1的表达与果蝇的寿命延长有关[48,50]. ...
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
... [5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
... [5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
The continuum of Drosophila embryonic development at single-cell resolution
1
2022
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Aging Fly Cell Atlas identifies exhaustive aging features at cellular resolution
1
2023
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
The connectome of an insect brain
1
2023
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Coordinated control of neuronal differentiation and wiring by sustained transcription factors
1
2022
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Axonal self-sorting without target guidance in Drosophila visual map formation
1
2024
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Effects of hunger on neuronal histone modifications slow aging in Drosophila
1
2023
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Presynaptic Ube3a E3 ligase promotes synapse elimination through down-regulation of BMP signaling
1
2023
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Ecology-relevant bacteria drive the evolution of host antimicrobial peptides in Drosophila
1
2023
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
A conserved bacterial genetic basis for commensal-host specificity
1
2024
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
PI4P-mediated solid-like Merlin condensates orchestrate Hippo pathway regulation
1
2024
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Hippo signaling instructs ectopic but not normal organ growth
1
2022
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Widespread regulatory specificities between transcriptional co-repressors and enhancers in Drosophila
1
2023
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Pervasive sublethal effects of agrochemicals on insects at environmentally relevant concentrations
1
2024
... 近年来,果蝇作为经典模式生物,在细胞发育、神经回路、衰老机制、代谢调控、微生物互作以及环境应答等方面发挥着关键作用.在图谱层面,研究者利用单细胞技术和多组学方法,重构了果蝇从胚胎发育到衰老过程中的转录组和神经连接图谱.Calderon等[6]研究发现果蝇胚胎发育的细胞类型特异性.Lu等[7]研究发现果蝇衰老细胞图谱的动态变化.Winding等[8]研究重建了果蝇大脑的神经元连接网络,揭示了神经回路的复杂性和功能.在神经机制方面,研究者们探索了神经发育、突触连接和行为调控的整合机制.例如,关于神经元分化和连接的研究揭示了转录因子在神经元命运决定和突触形成中的双重作用[9].Agi等[10]的研究发现,轴突之间的局部接触规则在视觉神经元投射中起主导作用.在表观遗传与代谢网络层面,研究者们探讨了代谢状态通过表观遗传机制影响寿命和衰老的过程.Weaver等[11]关于“饥饿信号经组蛋白乙酰化调控抗衰老转录程式”的研究发现,饥饿或支链氨基酸(branched-chain amino acid)剥夺降低特定脑区组蛋白乙酰化,可激活抗衰老转录.同年,Furusawa等[12]关于“泛素连接酶Ube3a介导突触消除”的研究揭示了Ube3a调控突触的可塑性.二者共同说明了代谢记忆可通过神经功能来影响衰老.宿主-微生物互作研究显示,果蝇与共生体的共演化由分子匹配来驱动.Hanson等[13]关于“生态细菌驱动抗菌肽进化”的研究表明,抗菌肽定向突变匹配肠杆菌表面特征.Gutiérrez-García等[14]利用果蝇和植物乳植杆菌模型,发现了一种保守的细菌遗传机制,揭示了特定宿主黏附蛋白的关键作用.细胞信号研究突破线性模型,强调空间、相变与生理背景.得克萨斯大学西南医学中心潘多加院士团队发现肿瘤抑制因子Merlin固态凝聚体通过与磷脂酰肌醇-4-磷酸(phosphatidylinositol 4-phosphate)结合相互作用,激活下游hippo信号,从而维持组织稳态平衡[15].Gandara等[16]关于“hippo通路特异性抑制异位生长”的研究发现,hippo通路对正常发育器官保持低活性以支持其生长,而对异位或再生样组织则激活下游效应器Yorkie来抑制其生长.这些研究为理解细胞内信号通路的复杂调控机制提供了新的视角.在转录调控与表观层面,研究者们系统性地分析了经典共抑制因子的结合谱,发现它们具有特定组织类型与增强子结构的偏好性.Jacobs等[17]的研究揭示了共抑制转录因子可通过结合不同的DNA元件来调控发育节点基因,支持共抑制转录因子“选择性抑制机制”并推翻“广泛背景型抑制”旧说.在生态适应与环境毒理学层面,研究者们拓宽了果蝇在毒理学研究中的边界,将果蝇用于真实生态以扰动响应建模.例如,2023年的“自然浓度下农药扰动果蝇磷酸化网络”[18]采用高通量行为与磷酸组学技术,系统地评估了大剂量农药在“环境实际浓度+热胁迫”条件下对果蝇神经系统和代谢稳态的影响.研究发现,超过50%的化合物具有亚致死神经毒性,且其毒性随着温度升高而显著增强.这一研究为帮助研究者们更好地理解环境因素对生物体的影响提供了新的视角. ...
Drosophila: A laboratory handbook
1
1990
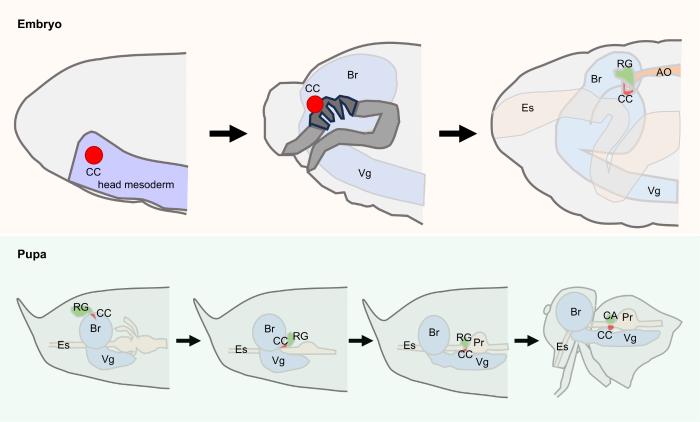
... 作为全变态昆虫,果蝇在25 ℃且营养丰富的条件下,其胚胎期发育时间需约24 h,孵化后的幼虫在经历3个龄期后进入蛹期.化蛹后,幼虫的身体结构发生剧烈重塑,最终的成虫会在化蛹后的第5天羽化而出[19].整个发育进程,心侧体经历了胚胎期分化、幼虫期生长、蛹期重塑和成虫期成熟4个过程. ...
Specification of Drosophila corpora cardiaca neuroendocrine cells from mesoderm is regulated by Notch signaling
3
2011
... 果蝇心侧体是一种与脊椎动物胰腺α细胞同源的神经内分泌腺,始于果蝇头部中胚层(head mesoderm)[20].随着胚胎期发育的推进,心侧体祖细胞(progenitors)经历一系列形态变化,在延长的原肠胚阶段(extended germ band stage),心侧体的祖细胞形成每簇包含6~8个细胞的一对细胞簇,位于原脑(protocerebrum)内表面与前肠之间.当毗邻原脑时,心侧体的祖细胞直接与神经前体细胞(neural precursors)接触,而这些神经前体细胞将发育成脑部的中间神经节(pars intercerebralis),其神经元在后期可支配心侧体[21].在原肠胚回缩期间(germ band retraction),心侧体的祖细胞数量增加并向后迁移,穿过脑部的腹侧神经束并附着于咽侧体(corpus allatum)和前胸腺(prothoracic gland)的原始基团上[22].在背闭合(dorsal closure)过程中,心侧体咽侧体和前胸腺围绕前主动脉移动,最终形成环腺(ring gland)[23](图1). ...
... 在幼虫阶段,心侧体作为环腺的一部分,位于幼虫脑的两个半球之间,与咽侧体和前胸腺共同构成环腺[24].环腺位于大脑前中枢神经系统背侧,肠道和心脏穿“环”而过[25].此时的心侧体由两簇细胞组成,每簇约7个细胞,共约14个细胞[22].进入蛹期后,心侧体细胞逐渐迁移至脑叶和前肠背侧.期间,心侧体发生了迁移与重塑,前胸腺从环腺分离后降解,咽侧体和心侧体虽被保留但逐渐分离,咽侧体附着在靠近头部的食管上,心侧体迁移到嗉囊(crop)和中肠交界处上方的位置[21,23].在成虫期,心侧体两簇细胞逐渐融合,且环绕心脏分布,形成双叶结构,两叶之间彼此密切结合,看起来像一整个组织块[20](图1). ...
... Notch信号通路在控制心侧体祖细胞的数量方面扮演着核心角色.在胚胎发育第11阶段之前,Notch信号活跃,可限制心侧体祖细胞的数量.然而,若Notch信号被破坏,例如在基因delta、Notch或E(spl)突变体中,心侧体细胞会发生扩增[20].此外,dpp(decapentaplegic)基因及其拮抗因子sog(short gastrulation)基因,以及hh(hedgehog)基因等也参与调控心侧体的形态发生[33-35].sog基因在心侧体祖细胞起源的中腹区域(midventral domain)表达,在sog基因突变体中,心侧体完全缺失.dpp基因和hh基因分别在头部中胚层(head mesoderm)和前肠(foregut)中表达,这两种组织与心侧体相邻,它们的缺失会导致心侧体细胞增殖和迁移缺陷[32]. ...
Specification of the endocrine primordia controlling insect moulting and metamorphosis by the JAK/STAT signalling pathway
2
2022
... 果蝇心侧体是一种与脊椎动物胰腺α细胞同源的神经内分泌腺,始于果蝇头部中胚层(head mesoderm)[20].随着胚胎期发育的推进,心侧体祖细胞(progenitors)经历一系列形态变化,在延长的原肠胚阶段(extended germ band stage),心侧体的祖细胞形成每簇包含6~8个细胞的一对细胞簇,位于原脑(protocerebrum)内表面与前肠之间.当毗邻原脑时,心侧体的祖细胞直接与神经前体细胞(neural precursors)接触,而这些神经前体细胞将发育成脑部的中间神经节(pars intercerebralis),其神经元在后期可支配心侧体[21].在原肠胚回缩期间(germ band retraction),心侧体的祖细胞数量增加并向后迁移,穿过脑部的腹侧神经束并附着于咽侧体(corpus allatum)和前胸腺(prothoracic gland)的原始基团上[22].在背闭合(dorsal closure)过程中,心侧体咽侧体和前胸腺围绕前主动脉移动,最终形成环腺(ring gland)[23](图1). ...
... 在幼虫阶段,心侧体作为环腺的一部分,位于幼虫脑的两个半球之间,与咽侧体和前胸腺共同构成环腺[24].环腺位于大脑前中枢神经系统背侧,肠道和心脏穿“环”而过[25].此时的心侧体由两簇细胞组成,每簇约7个细胞,共约14个细胞[22].进入蛹期后,心侧体细胞逐渐迁移至脑叶和前肠背侧.期间,心侧体发生了迁移与重塑,前胸腺从环腺分离后降解,咽侧体和心侧体虽被保留但逐渐分离,咽侧体附着在靠近头部的食管上,心侧体迁移到嗉囊(crop)和中肠交界处上方的位置[21,23].在成虫期,心侧体两簇细胞逐渐融合,且环绕心脏分布,形成双叶结构,两叶之间彼此密切结合,看起来像一整个组织块[20](图1). ...
Hemolymph sugar homeostasis and starvation-induced hyperactivity affected by genetic manipulations of the adipokinetic hormone-encoding gene in Drosophila melanogaster
5
2004
... 果蝇心侧体是一种与脊椎动物胰腺α细胞同源的神经内分泌腺,始于果蝇头部中胚层(head mesoderm)[20].随着胚胎期发育的推进,心侧体祖细胞(progenitors)经历一系列形态变化,在延长的原肠胚阶段(extended germ band stage),心侧体的祖细胞形成每簇包含6~8个细胞的一对细胞簇,位于原脑(protocerebrum)内表面与前肠之间.当毗邻原脑时,心侧体的祖细胞直接与神经前体细胞(neural precursors)接触,而这些神经前体细胞将发育成脑部的中间神经节(pars intercerebralis),其神经元在后期可支配心侧体[21].在原肠胚回缩期间(germ band retraction),心侧体的祖细胞数量增加并向后迁移,穿过脑部的腹侧神经束并附着于咽侧体(corpus allatum)和前胸腺(prothoracic gland)的原始基团上[22].在背闭合(dorsal closure)过程中,心侧体咽侧体和前胸腺围绕前主动脉移动,最终形成环腺(ring gland)[23](图1). ...
... 在幼虫阶段,心侧体作为环腺的一部分,位于幼虫脑的两个半球之间,与咽侧体和前胸腺共同构成环腺[24].环腺位于大脑前中枢神经系统背侧,肠道和心脏穿“环”而过[25].此时的心侧体由两簇细胞组成,每簇约7个细胞,共约14个细胞[22].进入蛹期后,心侧体细胞逐渐迁移至脑叶和前肠背侧.期间,心侧体发生了迁移与重塑,前胸腺从环腺分离后降解,咽侧体和心侧体虽被保留但逐渐分离,咽侧体附着在靠近头部的食管上,心侧体迁移到嗉囊(crop)和中肠交界处上方的位置[21,23].在成虫期,心侧体两簇细胞逐渐融合,且环绕心脏分布,形成双叶结构,两叶之间彼此密切结合,看起来像一整个组织块[20](图1). ...
... 心侧体在果蝇的多种生理过程中发挥着关键作用,其不仅可以通过分泌肽激素远程调控新陈代谢,心侧体的神经还可以投射至成虫和幼虫的心脏、食道、中枢神经系统、幼虫前胸腺以及成虫嗉囊等组织,直接影响组织功能[4, 22].心侧体轴突投射至心脏,可刺激心脏收缩以促进AKH向靶器官的扩散[73];投射至幼虫中央神经系统的胰岛素合成细胞,可调节DILP3的糖依赖性分泌[74];投射至前胸腺,可调控幼虫发育时间[75];投射至成虫嗉囊,可促进嗉囊排空[22].心侧体通过其分泌的激素和神经连接,在糖代谢、变态发育、取食行为和睡眠调节等方面展现出复杂而精确的调控机制(图3). ...
... [22].心侧体通过其分泌的激素和神经连接,在糖代谢、变态发育、取食行为和睡眠调节等方面展现出复杂而精确的调控机制(图3). ...
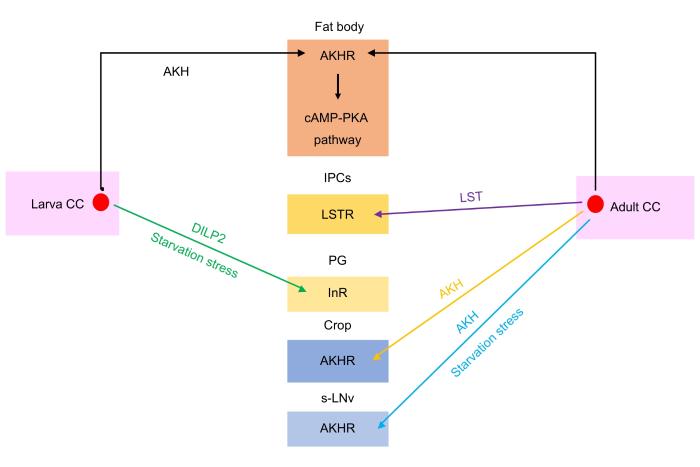
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
Metamorphosis of the corpus allatum and degeneration of the prothoracic glands during the larval-pupal-adult transformation of Drosophila melanogaster: a cytophysiological analysis of the ring gland
2
1991
... 果蝇心侧体是一种与脊椎动物胰腺α细胞同源的神经内分泌腺,始于果蝇头部中胚层(head mesoderm)[20].随着胚胎期发育的推进,心侧体祖细胞(progenitors)经历一系列形态变化,在延长的原肠胚阶段(extended germ band stage),心侧体的祖细胞形成每簇包含6~8个细胞的一对细胞簇,位于原脑(protocerebrum)内表面与前肠之间.当毗邻原脑时,心侧体的祖细胞直接与神经前体细胞(neural precursors)接触,而这些神经前体细胞将发育成脑部的中间神经节(pars intercerebralis),其神经元在后期可支配心侧体[21].在原肠胚回缩期间(germ band retraction),心侧体的祖细胞数量增加并向后迁移,穿过脑部的腹侧神经束并附着于咽侧体(corpus allatum)和前胸腺(prothoracic gland)的原始基团上[22].在背闭合(dorsal closure)过程中,心侧体咽侧体和前胸腺围绕前主动脉移动,最终形成环腺(ring gland)[23](图1). ...
... 在幼虫阶段,心侧体作为环腺的一部分,位于幼虫脑的两个半球之间,与咽侧体和前胸腺共同构成环腺[24].环腺位于大脑前中枢神经系统背侧,肠道和心脏穿“环”而过[25].此时的心侧体由两簇细胞组成,每簇约7个细胞,共约14个细胞[22].进入蛹期后,心侧体细胞逐渐迁移至脑叶和前肠背侧.期间,心侧体发生了迁移与重塑,前胸腺从环腺分离后降解,咽侧体和心侧体虽被保留但逐渐分离,咽侧体附着在靠近头部的食管上,心侧体迁移到嗉囊(crop)和中肠交界处上方的位置[21,23].在成虫期,心侧体两簇细胞逐渐融合,且环绕心脏分布,形成双叶结构,两叶之间彼此密切结合,看起来像一整个组织块[20](图1). ...
The postembryonic development of Drosophila
1
1950
... 在幼虫阶段,心侧体作为环腺的一部分,位于幼虫脑的两个半球之间,与咽侧体和前胸腺共同构成环腺[24].环腺位于大脑前中枢神经系统背侧,肠道和心脏穿“环”而过[25].此时的心侧体由两簇细胞组成,每簇约7个细胞,共约14个细胞[22].进入蛹期后,心侧体细胞逐渐迁移至脑叶和前肠背侧.期间,心侧体发生了迁移与重塑,前胸腺从环腺分离后降解,咽侧体和心侧体虽被保留但逐渐分离,咽侧体附着在靠近头部的食管上,心侧体迁移到嗉囊(crop)和中肠交界处上方的位置[21,23].在成虫期,心侧体两簇细胞逐渐融合,且环绕心脏分布,形成双叶结构,两叶之间彼此密切结合,看起来像一整个组织块[20](图1). ...
Ablation of insulin-producing neurons in flies: growth and diabetic phenotypes
1
2002
... 在幼虫阶段,心侧体作为环腺的一部分,位于幼虫脑的两个半球之间,与咽侧体和前胸腺共同构成环腺[24].环腺位于大脑前中枢神经系统背侧,肠道和心脏穿“环”而过[25].此时的心侧体由两簇细胞组成,每簇约7个细胞,共约14个细胞[22].进入蛹期后,心侧体细胞逐渐迁移至脑叶和前肠背侧.期间,心侧体发生了迁移与重塑,前胸腺从环腺分离后降解,咽侧体和心侧体虽被保留但逐渐分离,咽侧体附着在靠近头部的食管上,心侧体迁移到嗉囊(crop)和中肠交界处上方的位置[21,23].在成虫期,心侧体两簇细胞逐渐融合,且环绕心脏分布,形成双叶结构,两叶之间彼此密切结合,看起来像一整个组织块[20](图1). ...
The Drosophila sine oculis locus encodes a homeodomain-containing protein required for the development of the entire visual system
1
1994
... 心侧体分化在胚胎发育阶段受特定基因和信号通路的严格调控,并依赖多个基因和信号通路的协同作用,且发育历程具有高度时空特异性,其结构和功能会随发育阶段的推进而发生显著变化.在胚胎发育早期,心侧体祖细胞从头部中胚层的前腹褶唇区域(anterior lip of the ventral furrow)中分离出来,这一过程受到诸如so(sine oculis)、gt(giant)、twi(twist)、sna(snail)和tin(tinman)等关键基因的调控.这些基因在囊胚层阶段(blastoderm stage)表达,可决定心侧体的早期命运,即它们的突变会导致心侧体的缺失[26-31].随着发育进入原肠胚阶段(germ band stage),心侧体祖细胞开始表达同源框基因gl(glass),gl基因对于心侧体的正常分化和成熟发挥着不可或缺的作用,其在胚胎发育的第10阶段开始表达,若gl基因突变,心侧体将无法正常形成[32]. ...
The giant gene of Drosophila encodes a b-ZIP DNA-binding protein that regulates the expression of other segmentation gap genes
0
1992
A novel spatial transcription pattern associated with the segmentation gene, giant, of Drosophila
0
1989
The snail gene required for mesoderm formation in Drosophila is expressed dynamically in derivatives of all three germ layers
0
1991
The Drosophila developmental gene snail encodes a protein with nucleic acid binding fingers
0
1987
The gene tinman is required for specification of the heart and visceral muscles in Drosophila
1
1993
... 心侧体分化在胚胎发育阶段受特定基因和信号通路的严格调控,并依赖多个基因和信号通路的协同作用,且发育历程具有高度时空特异性,其结构和功能会随发育阶段的推进而发生显著变化.在胚胎发育早期,心侧体祖细胞从头部中胚层的前腹褶唇区域(anterior lip of the ventral furrow)中分离出来,这一过程受到诸如so(sine oculis)、gt(giant)、twi(twist)、sna(snail)和tin(tinman)等关键基因的调控.这些基因在囊胚层阶段(blastoderm stage)表达,可决定心侧体的早期命运,即它们的突变会导致心侧体的缺失[26-31].随着发育进入原肠胚阶段(germ band stage),心侧体祖细胞开始表达同源框基因gl(glass),gl基因对于心侧体的正常分化和成熟发挥着不可或缺的作用,其在胚胎发育的第10阶段开始表达,若gl基因突变,心侧体将无法正常形成[32]. ...
Embryonic development of the Drosophila corpus cardiacum, a neuroendocrine gland with similarity to the vertebrate pituitary, is controlled by sine oculis and glass
2
2004
... 心侧体分化在胚胎发育阶段受特定基因和信号通路的严格调控,并依赖多个基因和信号通路的协同作用,且发育历程具有高度时空特异性,其结构和功能会随发育阶段的推进而发生显著变化.在胚胎发育早期,心侧体祖细胞从头部中胚层的前腹褶唇区域(anterior lip of the ventral furrow)中分离出来,这一过程受到诸如so(sine oculis)、gt(giant)、twi(twist)、sna(snail)和tin(tinman)等关键基因的调控.这些基因在囊胚层阶段(blastoderm stage)表达,可决定心侧体的早期命运,即它们的突变会导致心侧体的缺失[26-31].随着发育进入原肠胚阶段(germ band stage),心侧体祖细胞开始表达同源框基因gl(glass),gl基因对于心侧体的正常分化和成熟发挥着不可或缺的作用,其在胚胎发育的第10阶段开始表达,若gl基因突变,心侧体将无法正常形成[32]. ...
... Notch信号通路在控制心侧体祖细胞的数量方面扮演着核心角色.在胚胎发育第11阶段之前,Notch信号活跃,可限制心侧体祖细胞的数量.然而,若Notch信号被破坏,例如在基因delta、Notch或E(spl)突变体中,心侧体细胞会发生扩增[20].此外,dpp(decapentaplegic)基因及其拮抗因子sog(short gastrulation)基因,以及hh(hedgehog)基因等也参与调控心侧体的形态发生[33-35].sog基因在心侧体祖细胞起源的中腹区域(midventral domain)表达,在sog基因突变体中,心侧体完全缺失.dpp基因和hh基因分别在头部中胚层(head mesoderm)和前肠(foregut)中表达,这两种组织与心侧体相邻,它们的缺失会导致心侧体细胞增殖和迁移缺陷[32]. ...
An activity gradient of decapentaplegic is necessary for the specification of dorsal pattern elements in the Drosophila embryo
1
1993
... Notch信号通路在控制心侧体祖细胞的数量方面扮演着核心角色.在胚胎发育第11阶段之前,Notch信号活跃,可限制心侧体祖细胞的数量.然而,若Notch信号被破坏,例如在基因delta、Notch或E(spl)突变体中,心侧体细胞会发生扩增[20].此外,dpp(decapentaplegic)基因及其拮抗因子sog(short gastrulation)基因,以及hh(hedgehog)基因等也参与调控心侧体的形态发生[33-35].sog基因在心侧体祖细胞起源的中腹区域(midventral domain)表达,在sog基因突变体中,心侧体完全缺失.dpp基因和hh基因分别在头部中胚层(head mesoderm)和前肠(foregut)中表达,这两种组织与心侧体相邻,它们的缺失会导致心侧体细胞增殖和迁移缺陷[32]. ...
A conserved system for dorsal-ventral patterning in insects and vertebrates involving sog and chordin
0
1995
Control of epithelial morphogenesis by cell signaling and integrin molecules in the Drosophila foregut
1
1995
... Notch信号通路在控制心侧体祖细胞的数量方面扮演着核心角色.在胚胎发育第11阶段之前,Notch信号活跃,可限制心侧体祖细胞的数量.然而,若Notch信号被破坏,例如在基因delta、Notch或E(spl)突变体中,心侧体细胞会发生扩增[20].此外,dpp(decapentaplegic)基因及其拮抗因子sog(short gastrulation)基因,以及hh(hedgehog)基因等也参与调控心侧体的形态发生[33-35].sog基因在心侧体祖细胞起源的中腹区域(midventral domain)表达,在sog基因突变体中,心侧体完全缺失.dpp基因和hh基因分别在头部中胚层(head mesoderm)和前肠(foregut)中表达,这两种组织与心侧体相邻,它们的缺失会导致心侧体细胞增殖和迁移缺陷[32]. ...
Heartless, a Drosophila FGF receptor homolog, is essential for cell migration and establishment of several mesodermal lineages
1
1996
... htl(heartless)基因作为果蝇成纤维细胞生长因子受体同源物,其突变对心侧体的早期发育没有直接影响,但会造成主动脉(aorta)缺失,从而使环腺在后期的形成过程中高度异常[36].tll(tailless)基因突变同样会导致心侧体出现缺陷,这提示原脑(protocerebrum)与心侧体祖细胞之间可能存在其他尚未明确的信号交互[37].这些调控因子在不同发育阶段的精确协调,确保了心侧体祖细胞的正常形成、迁移、增殖和分化,从而维持了果蝇胚胎期心侧体发育的正常进程. ...
The Drosophila gene tailless is expressed at the embryonic termini and is a member of the steroid receptor superfamily
1
1990
... htl(heartless)基因作为果蝇成纤维细胞生长因子受体同源物,其突变对心侧体的早期发育没有直接影响,但会造成主动脉(aorta)缺失,从而使环腺在后期的形成过程中高度异常[36].tll(tailless)基因突变同样会导致心侧体出现缺陷,这提示原脑(protocerebrum)与心侧体祖细胞之间可能存在其他尚未明确的信号交互[37].这些调控因子在不同发育阶段的精确协调,确保了心侧体祖细胞的正常形成、迁移、增殖和分化,从而维持了果蝇胚胎期心侧体发育的正常进程. ...
Energy homeostasis control in Drosophila adipokinetic hormone mutants
3
2015
... 心侧体通过自分泌反馈回路来维持AKH水平的稳态.研究表明,AKH与AKH受体(adipokinetic hormone receptor,AKHR)相互作用,通过调节AKH基因的转录活性来实现这一目的.此外,AKH的分泌水平与心侧体细胞内的环磷酸腺苷(cyclic adenosine monophosphate,cAMP)和钙离子浓度密切相关,这些信号分子在反馈回路中发挥关键作用[38]. ...
... 营养状况是影响心侧体功能的重要因素.在营养丰富的条件下,高血糖水平会抑制心侧体细胞的电信号活力,从而减少AKH的分泌;而在饥饿状态下,低血糖水平会增加心侧体细胞的电信号活力,促进AKH的释放,以动员储存的能源物质.这种调节机制可能涉及心侧体细胞表面的葡萄糖感受器,如葡糖激酶(glucokinase)和ATP敏感性钾通道(ATP-sensitive potassium channels)蛋白,它们能够感知血糖变化并调节细胞的兴奋性[38].此外,味觉水感应离子通道蛋白PPK28的缺失也会改变果蝇的代谢稳态,其通过增强神经元的AKH信号来促进内部脂质和水分储存,并延长健康寿命[39]. ...
... 最近的研究表明,埃及伊蚊卵巢内存在AKHR基因的表达[60],暗示AKH信号在生殖中可能有新的作用.另有研究显示,心侧体因表达瞬时受体电位 A1 通道蛋白(transient receptor potential A1)而对紫外线敏感[103],表明心侧体在应激反应中发挥关键作用,且AKH信号可调节抗氧化应激[104].在营养丰富的环境中,AKH基因和AKHR基因突变对突变体的发育(如孵化率、存活率、从产卵到羽化的时间)或适应性(如体型、繁殖力)无影响[38],表明AKH主要在极端条件(如饥饿)下发挥作用.饥饿胁迫会极大地促进脂肪体中脂类的动用,使生物体在缺乏食物的情况下可调动储备的能量[105].在短时间(4 h)禁食条件下,AKH通过一系列复杂的信号转导通路(包括肝激酶B1、盐诱导激酶3和组蛋白去乙酰化酶4)使FOXO去乙酰化,进而调控TAG脂酶Brummer基因的转录[106].在饥饿状态下,AKHR基因突变的果蝇雄虫交配率显著降低,对雄性特异性信息素的感应能力也减弱,同时,AKHR基因缺失的雌虫表皮中信息素的合成受到抑制.由此推测,在饥饿胁迫下,AKH/AKHR通路通过调控脂类调动影响雄虫的求偶行为和雌虫的生殖力[95, 98]. ...
Water sensor ppk28 modulates Drosophila lifespan and physiology through AKH signaling
1
2014
... 营养状况是影响心侧体功能的重要因素.在营养丰富的条件下,高血糖水平会抑制心侧体细胞的电信号活力,从而减少AKH的分泌;而在饥饿状态下,低血糖水平会增加心侧体细胞的电信号活力,促进AKH的释放,以动员储存的能源物质.这种调节机制可能涉及心侧体细胞表面的葡萄糖感受器,如葡糖激酶(glucokinase)和ATP敏感性钾通道(ATP-sensitive potassium channels)蛋白,它们能够感知血糖变化并调节细胞的兴奋性[38].此外,味觉水感应离子通道蛋白PPK28的缺失也会改变果蝇的代谢稳态,其通过增强神经元的AKH信号来促进内部脂质和水分储存,并延长健康寿命[39]. ...
The lateral posterior clock neurons of Drosophila melanogaster express three neuropeptides and have multiple connections within the circadian clock network and beyond
1
2022
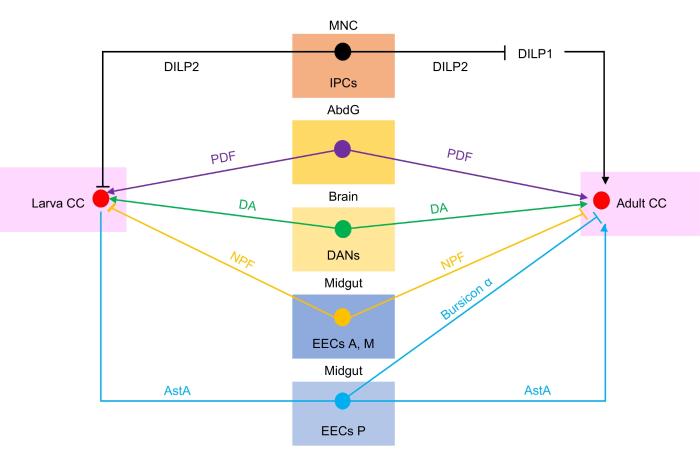
... 在果蝇的营养调控网络中,肠道通过多种信号机制对心侧体进行精细调控.其中抑咽侧体神经肽A(allatostatin-A,AstA)是关键的调节因子之一.AstA由肠内分泌细胞(enteroendocrine cells)产生后通过其受体Dar-2在心侧体和胰岛素合成细胞中发挥作用,对AKH产生正向调节作用,同时对胰岛素样肽的合成产生负向调节作用[40].研究表明,当AstA神经元的活性增加时,果蝇对蛋白质丰富食物的偏好性增强,对糖的偏好性减弱,表明肠道通过AstA信号在不同营养物质之间进行权衡,进而影响果蝇的代谢和进食行为[41].此外,肠内分泌细胞在感知营养物质后分泌的bursicon α通过其受体DLgr2向心侧体发送信号,从而抑制AKH的产生和全身信号传导,这种机制在营养充足时可限制能量的过度消耗,以维持能量稳态[42].肠内分泌细胞响应饮食中的糖并分泌神经肽F(neuro-peptide F,NPF),NPF与NPF受体(neuropeptide F receptor,NPFR)结合可激活下游信号通路,在心侧体中抑制AKH的合成和分泌,同时增强胰岛素样肽的分泌,从而调节糖脂代谢[43-44]. ...
The neuropeptide allatostatin a regulates metabolism and feeding decisions in Drosophila
2
2015
... 在果蝇的营养调控网络中,肠道通过多种信号机制对心侧体进行精细调控.其中抑咽侧体神经肽A(allatostatin-A,AstA)是关键的调节因子之一.AstA由肠内分泌细胞(enteroendocrine cells)产生后通过其受体Dar-2在心侧体和胰岛素合成细胞中发挥作用,对AKH产生正向调节作用,同时对胰岛素样肽的合成产生负向调节作用[40].研究表明,当AstA神经元的活性增加时,果蝇对蛋白质丰富食物的偏好性增强,对糖的偏好性减弱,表明肠道通过AstA信号在不同营养物质之间进行权衡,进而影响果蝇的代谢和进食行为[41].此外,肠内分泌细胞在感知营养物质后分泌的bursicon α通过其受体DLgr2向心侧体发送信号,从而抑制AKH的产生和全身信号传导,这种机制在营养充足时可限制能量的过度消耗,以维持能量稳态[42].肠内分泌细胞响应饮食中的糖并分泌神经肽F(neuro-peptide F,NPF),NPF与NPF受体(neuropeptide F receptor,NPFR)结合可激活下游信号通路,在心侧体中抑制AKH的合成和分泌,同时增强胰岛素样肽的分泌,从而调节糖脂代谢[43-44]. ...
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
A neuronal relay mediates a nutrient responsive gut/fat body axis regulating energy homeostasis in adult Drosophila
1
2019
... 在果蝇的营养调控网络中,肠道通过多种信号机制对心侧体进行精细调控.其中抑咽侧体神经肽A(allatostatin-A,AstA)是关键的调节因子之一.AstA由肠内分泌细胞(enteroendocrine cells)产生后通过其受体Dar-2在心侧体和胰岛素合成细胞中发挥作用,对AKH产生正向调节作用,同时对胰岛素样肽的合成产生负向调节作用[40].研究表明,当AstA神经元的活性增加时,果蝇对蛋白质丰富食物的偏好性增强,对糖的偏好性减弱,表明肠道通过AstA信号在不同营养物质之间进行权衡,进而影响果蝇的代谢和进食行为[41].此外,肠内分泌细胞在感知营养物质后分泌的bursicon α通过其受体DLgr2向心侧体发送信号,从而抑制AKH的产生和全身信号传导,这种机制在营养充足时可限制能量的过度消耗,以维持能量稳态[42].肠内分泌细胞响应饮食中的糖并分泌神经肽F(neuro-peptide F,NPF),NPF与NPF受体(neuropeptide F receptor,NPFR)结合可激活下游信号通路,在心侧体中抑制AKH的合成和分泌,同时增强胰岛素样肽的分泌,从而调节糖脂代谢[43-44]. ...
The sugar-responsive enteroendocrine neuropeptide F regulates lipid metabolism through glucagon-like and insulin-like hormones in Drosophila melanogaster
1
2021
... 在果蝇的营养调控网络中,肠道通过多种信号机制对心侧体进行精细调控.其中抑咽侧体神经肽A(allatostatin-A,AstA)是关键的调节因子之一.AstA由肠内分泌细胞(enteroendocrine cells)产生后通过其受体Dar-2在心侧体和胰岛素合成细胞中发挥作用,对AKH产生正向调节作用,同时对胰岛素样肽的合成产生负向调节作用[40].研究表明,当AstA神经元的活性增加时,果蝇对蛋白质丰富食物的偏好性增强,对糖的偏好性减弱,表明肠道通过AstA信号在不同营养物质之间进行权衡,进而影响果蝇的代谢和进食行为[41].此外,肠内分泌细胞在感知营养物质后分泌的bursicon α通过其受体DLgr2向心侧体发送信号,从而抑制AKH的产生和全身信号传导,这种机制在营养充足时可限制能量的过度消耗,以维持能量稳态[42].肠内分泌细胞响应饮食中的糖并分泌神经肽F(neuro-peptide F,NPF),NPF与NPF受体(neuropeptide F receptor,NPFR)结合可激活下游信号通路,在心侧体中抑制AKH的合成和分泌,同时增强胰岛素样肽的分泌,从而调节糖脂代谢[43-44]. ...
Hormonal axes in Drosophila: regulation of hormone release and multiplicity of actions
1
2020
... 在果蝇的营养调控网络中,肠道通过多种信号机制对心侧体进行精细调控.其中抑咽侧体神经肽A(allatostatin-A,AstA)是关键的调节因子之一.AstA由肠内分泌细胞(enteroendocrine cells)产生后通过其受体Dar-2在心侧体和胰岛素合成细胞中发挥作用,对AKH产生正向调节作用,同时对胰岛素样肽的合成产生负向调节作用[40].研究表明,当AstA神经元的活性增加时,果蝇对蛋白质丰富食物的偏好性增强,对糖的偏好性减弱,表明肠道通过AstA信号在不同营养物质之间进行权衡,进而影响果蝇的代谢和进食行为[41].此外,肠内分泌细胞在感知营养物质后分泌的bursicon α通过其受体DLgr2向心侧体发送信号,从而抑制AKH的产生和全身信号传导,这种机制在营养充足时可限制能量的过度消耗,以维持能量稳态[42].肠内分泌细胞响应饮食中的糖并分泌神经肽F(neuro-peptide F,NPF),NPF与NPF受体(neuropeptide F receptor,NPFR)结合可激活下游信号通路,在心侧体中抑制AKH的合成和分泌,同时增强胰岛素样肽的分泌,从而调节糖脂代谢[43-44]. ...
Modulation of metabolic hormone signaling via a circadian hormone and biogenic amine in Drosophila melanogaster
3
2022
... 在果蝇中,脑产生的神经递质多巴胺(dopamine,DA)和肽激素如色素分散因子(pigment-dispersing factor,PDF)可通过复杂的机制参与对心侧体细胞的调控,进而影响AKH的释放.研究表明,脑产生的DA在低血糖条件下可通过增加心侧体中细胞钙信号来促进AKH释放,其作用依赖于DA受体的激活.然而,蜕皮激素能够完全阻断细胞钙信号的增加,表明二者在心侧体中以拮抗的方式共同调节AKH的产生[45].此外,腹部神经节产生的PDF通过其色素分散因子受体(pigment-dispersing factor receptor)在心侧体中可增加cAMP水平,从而促进AKH的释放,这种调节作用可能与昼夜节律无关,而是通过非生物钟相关的机制来影响代谢过程[46].这些发现揭示了DA和PDF在代谢调控中的重要作用,表明它们通过与蜕皮激素相互作用,共同调节果蝇的代谢状态和行为响应. ...
... 进一步研究发现,如前所述的PDF和DA在心侧体中的作用可对果蝇的饥饿应激反应和运动行为产生显著影响.实验表明,敲低PDF可延长果蝇在饥饿条件下的生存时间,而过表达PDF则会缩短其寿命,这表明PDF通过调节AKH的释放来影响能量代谢[47].同样,DA受体在心侧体中的敲低会显著降低果蝇在饥饿条件下的生存能力,并引起运动活性的显著变化[45].这些结果表明,PDF和DA的信号通路通过调节AKH的分泌,为果蝇在饥饿等代谢应激条件下提供一种灵活的生理调节机制,以维持能量平衡并适应环境变化. ...
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
A novel diuretic hormone receptor in Drosophila: evidence for conservation of CGRP signaling
1
2005
... 在果蝇中,脑产生的神经递质多巴胺(dopamine,DA)和肽激素如色素分散因子(pigment-dispersing factor,PDF)可通过复杂的机制参与对心侧体细胞的调控,进而影响AKH的释放.研究表明,脑产生的DA在低血糖条件下可通过增加心侧体中细胞钙信号来促进AKH释放,其作用依赖于DA受体的激活.然而,蜕皮激素能够完全阻断细胞钙信号的增加,表明二者在心侧体中以拮抗的方式共同调节AKH的产生[45].此外,腹部神经节产生的PDF通过其色素分散因子受体(pigment-dispersing factor receptor)在心侧体中可增加cAMP水平,从而促进AKH的释放,这种调节作用可能与昼夜节律无关,而是通过非生物钟相关的机制来影响代谢过程[46].这些发现揭示了DA和PDF在代谢调控中的重要作用,表明它们通过与蜕皮激素相互作用,共同调节果蝇的代谢状态和行为响应. ...
Identification of Drosophila neuropeptide receptors by G protein-coupled receptors-β-arrestin2 interactions
1
2003
... 进一步研究发现,如前所述的PDF和DA在心侧体中的作用可对果蝇的饥饿应激反应和运动行为产生显著影响.实验表明,敲低PDF可延长果蝇在饥饿条件下的生存时间,而过表达PDF则会缩短其寿命,这表明PDF通过调节AKH的释放来影响能量代谢[47].同样,DA受体在心侧体中的敲低会显著降低果蝇在饥饿条件下的生存能力,并引起运动活性的显著变化[45].这些结果表明,PDF和DA的信号通路通过调节AKH的分泌,为果蝇在饥饿等代谢应激条件下提供一种灵活的生理调节机制,以维持能量平衡并适应环境变化. ...
Drosophila insulin-like peptide dilp1 increases lifespan and glucagon-like Akh expression epistatic to dilp2
3
2019
... 果蝇胰岛素样肽1(Drosophila insulin-like peptide 1,DILP1)和DILP2在果蝇心侧体的功能调控中具有复杂的相互作用.DILP2的缺失会上调DILP1的表达,且这种上调是DILP2突变果蝇中延长寿命和增加AKH表达所必需的.具体来说,DILP2主要在胚胎和成虫阶段表达;在正常发育过程中,DILP1主要在蛹期表达,但在DILP2突变的成虫中,其表达显著增加[5].这表明DILP2对DILP1具有负调控作用,且DILP1在DILP2缺失的情况下发挥作用,影响果蝇的寿命和AKH的表达[48].当营养充足时,DILP2由胰岛素合成细胞分泌,其可抑制AKH的释放,从而维持血糖稳定;而当营养匮乏时,DILP2的分泌减少,AKH释放增加,脂肪分解和糖原分解增加,为果蝇存活提供能量[4,49].研究表明,DILP1和DILP2可能通过不同的信号通路来影响心侧体的功能.例如,DILP1可能通过调节心侧体细胞内胰岛素受体底物(insulin receptor substrate)蛋白的活性来影响AKH分泌,而DILP2则可能通过影响心侧体细胞的增殖和分化来间接调节AKH的合成.DILP1在DILP2缺失的情况下表达增加,其或可通过影响AKH的表达和分泌,调节能量代谢,此外,DILP1的表达与果蝇的寿命延长有关[48,50]. ...
... [48,50]. ...
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
Regulation of insulin and adipokinetic hormone/glucagon production in flies
1
2020
... 果蝇胰岛素样肽1(Drosophila insulin-like peptide 1,DILP1)和DILP2在果蝇心侧体的功能调控中具有复杂的相互作用.DILP2的缺失会上调DILP1的表达,且这种上调是DILP2突变果蝇中延长寿命和增加AKH表达所必需的.具体来说,DILP2主要在胚胎和成虫阶段表达;在正常发育过程中,DILP1主要在蛹期表达,但在DILP2突变的成虫中,其表达显著增加[5].这表明DILP2对DILP1具有负调控作用,且DILP1在DILP2缺失的情况下发挥作用,影响果蝇的寿命和AKH的表达[48].当营养充足时,DILP2由胰岛素合成细胞分泌,其可抑制AKH的释放,从而维持血糖稳定;而当营养匮乏时,DILP2的分泌减少,AKH释放增加,脂肪分解和糖原分解增加,为果蝇存活提供能量[4,49].研究表明,DILP1和DILP2可能通过不同的信号通路来影响心侧体的功能.例如,DILP1可能通过调节心侧体细胞内胰岛素受体底物(insulin receptor substrate)蛋白的活性来影响AKH分泌,而DILP2则可能通过影响心侧体细胞的增殖和分化来间接调节AKH的合成.DILP1在DILP2缺失的情况下表达增加,其或可通过影响AKH的表达和分泌,调节能量代谢,此外,DILP1的表达与果蝇的寿命延长有关[48,50]. ...
Functional implications of Drosophila insulin -like peptides in metabolism, aging, and dietary restriction
1
2013
... 果蝇胰岛素样肽1(Drosophila insulin-like peptide 1,DILP1)和DILP2在果蝇心侧体的功能调控中具有复杂的相互作用.DILP2的缺失会上调DILP1的表达,且这种上调是DILP2突变果蝇中延长寿命和增加AKH表达所必需的.具体来说,DILP2主要在胚胎和成虫阶段表达;在正常发育过程中,DILP1主要在蛹期表达,但在DILP2突变的成虫中,其表达显著增加[5].这表明DILP2对DILP1具有负调控作用,且DILP1在DILP2缺失的情况下发挥作用,影响果蝇的寿命和AKH的表达[48].当营养充足时,DILP2由胰岛素合成细胞分泌,其可抑制AKH的释放,从而维持血糖稳定;而当营养匮乏时,DILP2的分泌减少,AKH释放增加,脂肪分解和糖原分解增加,为果蝇存活提供能量[4,49].研究表明,DILP1和DILP2可能通过不同的信号通路来影响心侧体的功能.例如,DILP1可能通过调节心侧体细胞内胰岛素受体底物(insulin receptor substrate)蛋白的活性来影响AKH分泌,而DILP2则可能通过影响心侧体细胞的增殖和分化来间接调节AKH的合成.DILP1在DILP2缺失的情况下表达增加,其或可通过影响AKH的表达和分泌,调节能量代谢,此外,DILP1的表达与果蝇的寿命延长有关[48,50]. ...
Flight fuel and neuropeptidergic control of fuel mobilisation in the twig wilter, Holopterna alata (Hemiptera, Coreidae)
1
2006
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
Occurrence of a hyperglyc?mic factor in the corpus cardiacum of an insect
1
1961
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
The proprotein convertase encoded by amontillado (amon) is required in Drosophila corpora cardiaca endocrine cells producing the glucose regulatory hormone AKH
1
2010
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
Hormonal regulation of energy metabolism in insects as a driving force for performance
1
2009
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
The role of peptide hormones in insect lipid metabolism
1
2020
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
Neuropeptides and neuropeptide receptors in the Drosophila melanogaster genome
1
2001
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
Identification of G protein-coupled receptors for Drosophila PRXamide peptides, CCAP, corazonin, and AKH supports a theory of ligand-receptor coevolution
2
2002
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
... [57-61]. ...
Molecular identification of the insect adipokinetic hormone receptors
1
2002
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
Analysis of peptide ligand specificity of different insect adipokinetic hormone receptors
0
2018
Functional characterization and quantitative expression analysis of two GnRH-related peptide receptors in the mosquito, Aedes aegypti
1
2018
... 最近的研究表明,埃及伊蚊卵巢内存在AKHR基因的表达[60],暗示AKH信号在生殖中可能有新的作用.另有研究显示,心侧体因表达瞬时受体电位 A1 通道蛋白(transient receptor potential A1)而对紫外线敏感[103],表明心侧体在应激反应中发挥关键作用,且AKH信号可调节抗氧化应激[104].在营养丰富的环境中,AKH基因和AKHR基因突变对突变体的发育(如孵化率、存活率、从产卵到羽化的时间)或适应性(如体型、繁殖力)无影响[38],表明AKH主要在极端条件(如饥饿)下发挥作用.饥饿胁迫会极大地促进脂肪体中脂类的动用,使生物体在缺乏食物的情况下可调动储备的能量[105].在短时间(4 h)禁食条件下,AKH通过一系列复杂的信号转导通路(包括肝激酶B1、盐诱导激酶3和组蛋白去乙酰化酶4)使FOXO去乙酰化,进而调控TAG脂酶Brummer基因的转录[106].在饥饿状态下,AKHR基因突变的果蝇雄虫交配率显著降低,对雄性特异性信息素的感应能力也减弱,同时,AKHR基因缺失的雌虫表皮中信息素的合成受到抑制.由此推测,在饥饿胁迫下,AKH/AKHR通路通过调控脂类调动影响雄虫的求偶行为和雌虫的生殖力[95, 98]. ...
Adipokinetic hormone signalling system in the Chagas disease vector, Rhodnius prolixus
1
2015
... AKH最早发现于美洲大蠊(Periplaneta americana)和飞蝗(Locusta migratoria)[51-52]中,属于AKH/RPCH(red pigment-concentrating hormone)多肽家族,迄今为止,在昆虫中已经鉴定出80多种.AKH是一种神经多肽,由心侧体合成[4],它源自一个包含信号肽和两个潜在肽段的前体,具有封闭的焦谷氨酰(pyroglutamyl,pGlu)N末端和酰胺化的C末端.在前体蛋白转化酶(amontillado)的作用下,AKH被加工成包含8~11个氨基酸的成熟肽,并激活生物活性[53].这种成熟肽能够促进昆虫脂肪体中的脂滴和糖原分解,并促进海藻糖生成.在高耗能的生命活动中,AKH通过调动脂肪体内的营养储备,为耗能组织提供能量物质,以维持生命过程的正常运行[54-55].AKH通过结合膜受体AKHR来激活胞内信号.AKHR属于A类视紫红质G蛋白偶联受体家族[56],最初通过果蝇受体分子cDNA的异源表达系统筛选发现[57-58].AKHR首次被鉴定于果蝇和家蚕(Bombyx mori)体内,目前已在多种昆虫中报道[57-61]. ...
Suppression of insulin production and secretion by a decretin hormone
2
2015
... Lst是一种由心侧体细胞分泌的肽激素,可响应成年果蝇食物限制,成熟肽由15个氨基酸组成.Lst的表达主要受糖类物质的调控,饥饿状态可引起其表达的上调.它通过胰岛素合成细胞上的G蛋白偶联受体CG9918来抑制胰岛素分泌.Lst基因的缺乏会导致高胰岛素血症、低血糖和肥胖等表型.正常情况下,心侧体负责合成并分泌Lst,而Lst基因突变会导致虫体发育的延迟,从而缩短成虫寿命.成虫中Lst基因的缺失会引发血淋巴中胰岛素含量的增加,同时虫体甘油三酯(triacylglycerol,TAG)的含量也上升,最终导致突变体肥胖[62]. ...
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
A new secreted insect protein belonging to the immuno globulin superfamily binds insulin and related peptides and inhibits their activities
1
2000
... ImpL2属于免疫球蛋白超家族,与胰岛素样生长因子结合蛋白-7(insulin-like growth factor-binding protein 7,IGFBP-7)有部分序列同源性,包含V型免疫球蛋白结构域和纤维连接蛋白Ⅲ型结构域[63-65].它在果蝇的大脑、环腺、肠道和脂肪体等部位的特定细胞中表达,尤其在环腺的心侧体、前中肠的约20个肠内分泌细胞以及脑半球和食管下神经节的不同神经元中[66].ImpL2是果蝇的生长抑制因子,能调节蜕皮激素的产生,协调生长发育与营养状态之间的关系[66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
Inhibition of insulin receptor activation by insulin-like growth factor binding proteins
0
1997
IMP-L2: an essential secreted immunoglobulin family member implicated in neural and ectodermal development in Drosophila
1
1993
... ImpL2属于免疫球蛋白超家族,与胰岛素样生长因子结合蛋白-7(insulin-like growth factor-binding protein 7,IGFBP-7)有部分序列同源性,包含V型免疫球蛋白结构域和纤维连接蛋白Ⅲ型结构域[63-65].它在果蝇的大脑、环腺、肠道和脂肪体等部位的特定细胞中表达,尤其在环腺的心侧体、前中肠的约20个肠内分泌细胞以及脑半球和食管下神经节的不同神经元中[66].ImpL2是果蝇的生长抑制因子,能调节蜕皮激素的产生,协调生长发育与营养状态之间的关系[66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
Imp-L2, a putative homolog of vertebrate IGF-binding protein 7, counteracts insulin signaling in Drosophila and is essential for starvation resistance
4
2008
... ImpL2属于免疫球蛋白超家族,与胰岛素样生长因子结合蛋白-7(insulin-like growth factor-binding protein 7,IGFBP-7)有部分序列同源性,包含V型免疫球蛋白结构域和纤维连接蛋白Ⅲ型结构域[63-65].它在果蝇的大脑、环腺、肠道和脂肪体等部位的特定细胞中表达,尤其在环腺的心侧体、前中肠的约20个肠内分泌细胞以及脑半球和食管下神经节的不同神经元中[66].ImpL2是果蝇的生长抑制因子,能调节蜕皮激素的产生,协调生长发育与营养状态之间的关系[66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
... [66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
... [66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
... [66, 70-72]. ...
Lifespan extension by increased expression of the Drosophila homologue of the IGFBP7 tumour suppressor
1
2011
... ImpL2属于免疫球蛋白超家族,与胰岛素样生长因子结合蛋白-7(insulin-like growth factor-binding protein 7,IGFBP-7)有部分序列同源性,包含V型免疫球蛋白结构域和纤维连接蛋白Ⅲ型结构域[63-65].它在果蝇的大脑、环腺、肠道和脂肪体等部位的特定细胞中表达,尤其在环腺的心侧体、前中肠的约20个肠内分泌细胞以及脑半球和食管下神经节的不同神经元中[66].ImpL2是果蝇的生长抑制因子,能调节蜕皮激素的产生,协调生长发育与营养状态之间的关系[66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
The TOR pathway couples nutrition and developmental timing in Drosophila
1
2008
... ImpL2属于免疫球蛋白超家族,与胰岛素样生长因子结合蛋白-7(insulin-like growth factor-binding protein 7,IGFBP-7)有部分序列同源性,包含V型免疫球蛋白结构域和纤维连接蛋白Ⅲ型结构域[63-65].它在果蝇的大脑、环腺、肠道和脂肪体等部位的特定细胞中表达,尤其在环腺的心侧体、前中肠的约20个肠内分泌细胞以及脑半球和食管下神经节的不同神经元中[66].ImpL2是果蝇的生长抑制因子,能调节蜕皮激素的产生,协调生长发育与营养状态之间的关系[66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
Antagonistic actions of ecdysone and insulins determine final size in Drosophila
1
2005
... ImpL2属于免疫球蛋白超家族,与胰岛素样生长因子结合蛋白-7(insulin-like growth factor-binding protein 7,IGFBP-7)有部分序列同源性,包含V型免疫球蛋白结构域和纤维连接蛋白Ⅲ型结构域[63-65].它在果蝇的大脑、环腺、肠道和脂肪体等部位的特定细胞中表达,尤其在环腺的心侧体、前中肠的约20个肠内分泌细胞以及脑半球和食管下神经节的不同神经元中[66].ImpL2是果蝇的生长抑制因子,能调节蜕皮激素的产生,协调生长发育与营养状态之间的关系[66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
Local requirement of the Drosophila insulin binding protein imp-L2 in coordinating developmental progression with nutritional conditions
1
2013
... ImpL2属于免疫球蛋白超家族,与胰岛素样生长因子结合蛋白-7(insulin-like growth factor-binding protein 7,IGFBP-7)有部分序列同源性,包含V型免疫球蛋白结构域和纤维连接蛋白Ⅲ型结构域[63-65].它在果蝇的大脑、环腺、肠道和脂肪体等部位的特定细胞中表达,尤其在环腺的心侧体、前中肠的约20个肠内分泌细胞以及脑半球和食管下神经节的不同神经元中[66].ImpL2是果蝇的生长抑制因子,能调节蜕皮激素的产生,协调生长发育与营养状态之间的关系[66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
Ras activity in the Drosophila prothoracic gland regulates body size and developmental rate via ecdysone release
0
2005
The role of the prothoracic gland in determining critical weight for metamorphosis in Drosophila melanogaster
2
2005
... ImpL2属于免疫球蛋白超家族,与胰岛素样生长因子结合蛋白-7(insulin-like growth factor-binding protein 7,IGFBP-7)有部分序列同源性,包含V型免疫球蛋白结构域和纤维连接蛋白Ⅲ型结构域[63-65].它在果蝇的大脑、环腺、肠道和脂肪体等部位的特定细胞中表达,尤其在环腺的心侧体、前中肠的约20个肠内分泌细胞以及脑半球和食管下神经节的不同神经元中[66].ImpL2是果蝇的生长抑制因子,能调节蜕皮激素的产生,协调生长发育与营养状态之间的关系[66-67].它通过与DILP直接结合的方式来抑制果蝇DILP的活性,并且可以调节前胸腺中的胰岛素信号活性,进而调节幼虫的发育时间以适应营养条件[66].此外,ImpL2参与调控胰岛素信号通路和雷帕霉素靶蛋白(target of rapamycin,TOR)信号通路,二者共同响应营养条件,调节发育时间,胰岛素通路在将营养信息与生长发育过程相结合方面发挥着关键作用[68-69].ImpL2过表达会导致化蛹的延迟,突变则会加速发育,在饥饿条件下,ImpL2对发育时间的影响更为显著[66, 70-72]. ...
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
Identification and expression of the Drosophila adipokinetic hormone gene
1
1995
... 心侧体在果蝇的多种生理过程中发挥着关键作用,其不仅可以通过分泌肽激素远程调控新陈代谢,心侧体的神经还可以投射至成虫和幼虫的心脏、食道、中枢神经系统、幼虫前胸腺以及成虫嗉囊等组织,直接影响组织功能[4, 22].心侧体轴突投射至心脏,可刺激心脏收缩以促进AKH向靶器官的扩散[73];投射至幼虫中央神经系统的胰岛素合成细胞,可调节DILP3的糖依赖性分泌[74];投射至前胸腺,可调控幼虫发育时间[75];投射至成虫嗉囊,可促进嗉囊排空[22].心侧体通过其分泌的激素和神经连接,在糖代谢、变态发育、取食行为和睡眠调节等方面展现出复杂而精确的调控机制(图3). ...
Dietary sugar promotes systemic TOR activation in Drosophila through AKH-dependent selective secretion of Dilp3
1
2015
... 心侧体在果蝇的多种生理过程中发挥着关键作用,其不仅可以通过分泌肽激素远程调控新陈代谢,心侧体的神经还可以投射至成虫和幼虫的心脏、食道、中枢神经系统、幼虫前胸腺以及成虫嗉囊等组织,直接影响组织功能[4, 22].心侧体轴突投射至心脏,可刺激心脏收缩以促进AKH向靶器官的扩散[73];投射至幼虫中央神经系统的胰岛素合成细胞,可调节DILP3的糖依赖性分泌[74];投射至前胸腺,可调控幼虫发育时间[75];投射至成虫嗉囊,可促进嗉囊排空[22].心侧体通过其分泌的激素和神经连接,在糖代谢、变态发育、取食行为和睡眠调节等方面展现出复杂而精确的调控机制(图3). ...
Ecdysone control of developmental transitions: lessons from Drosophila research
2
2013
... 心侧体在果蝇的多种生理过程中发挥着关键作用,其不仅可以通过分泌肽激素远程调控新陈代谢,心侧体的神经还可以投射至成虫和幼虫的心脏、食道、中枢神经系统、幼虫前胸腺以及成虫嗉囊等组织,直接影响组织功能[4, 22].心侧体轴突投射至心脏,可刺激心脏收缩以促进AKH向靶器官的扩散[73];投射至幼虫中央神经系统的胰岛素合成细胞,可调节DILP3的糖依赖性分泌[74];投射至前胸腺,可调控幼虫发育时间[75];投射至成虫嗉囊,可促进嗉囊排空[22].心侧体通过其分泌的激素和神经连接,在糖代谢、变态发育、取食行为和睡眠调节等方面展现出复杂而精确的调控机制(图3). ...
... 在果蝇变态发育中,心侧体发挥着关键作用,这与促前胸腺激素(prothoracicotropic hormone,PTTH)和ImpL2密切相关.在幼虫时期,PTTH在昆虫脑部神经分泌细胞合成后,被转移到心侧体中储存,并在特定发育阶段被释放到血淋巴中,刺激前胸腺合成蜕皮激素,从而启动变态发生[89].另一种观点认为,心侧体可将轴突投射至前胸腺,作为蜕皮激素前体蜕皮酮合成器官,可直接释放PTTH,从而影响蜕皮激素调控的变态发育[75].当PTTH缺失时,果蝇发育过程中核因子κB(nuclear factor κB)的信号减弱,成虫体内炎症标志物显著下降,组织损伤和功能衰退的情况降低[90].心侧体可在细胞表面富集ImpL2,用于帮助幼虫维持饥饿情况下前胸腺中胰岛素信号的水平.心侧体前期将DILP2通过ImpL2束缚在心侧体上,当幼虫渡过临界体重后,即便面临饥饿等环境压力,心侧体也能释放DILP2至前胸腺,维持前胸腺营养信号活力、保障蜕皮酮的正常合成,从而帮助幼虫变态发育的顺利推进[91-92]. ...
Discovering signaling mechanisms governing metabolism and metabolic diseases with Drosophila
1
2021
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
Dual lipolytic control of body fat storage and mobilization in Drosophila
1
2007
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
The use of decapitated insects to study lipid mobilization in adult Manduca sexta: effects of adipokinetic hormone and trehalose on fat body lipase activity
0
1996
Activation of fat body glycogen phosphorylase in Locusta migratoria by corpus cardiacum extract and synthetic adipokinetic hormone
0
1981
Endocrine control of TAG lipase in the fat body of the migratory locust, Locusta migratoria
0
2006
Locust adipokinetic hormones mobilize diacylglycerols selectively
1
2010
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
The role of Ins(1, 4, 5)P(3) in signal transduction of the metabolic neuropeptide Mem-CC in the cetoniid beetle, Pachnoda sinuata
0
2002
Mode of action of neuropeptides from the adipokinetic hormone family
1
2003
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
Adipokinetic hormone is dependent on extracellular Ca2+ for its stimulatory action on the glycogenolytic pathway in locust fat body in vitro
1
1991
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
New insights into adipokinetic hormone signaling
1
1998
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
Regulation of starvation-induced hyperactivity by insulin and glucagon signaling in adult Drosophila
3
2016
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
... [86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
Role of adipokinetic hormone during starvation in Drosophila
1
2018
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
High-fat diet enhances starvation-induced hyperactivity via sensitizing hunger-sensing neurons in Drosophila
1
2020
... AKH具有类胰高血糖素的功能,能够动员储存的能量储备,通过与G蛋白偶联受体结合发挥作用.在循环能量水平较低时,AKH被分泌并与脂肪体中的特异性受体AKHR结合.激活AKHR可通过增加糖原磷酸化酶活性和脂酶活性使糖原水解产生海藻糖,并促使TAG分解转化为甘油二酯(diacylglycerol,DAG)或脯氨酸[76],从而为机体提供葡萄糖等能量物质,以维持血糖水平[48].在果蝇等昆虫中,AKHR表达细胞簇主要分布于幼虫和成虫的脂肪体,AKH作用于脂肪体细胞,海藻糖作为分解产物被释放到血淋巴,为机体糖代谢提供物质基础,以维持血糖稳定[77-81].AKH与AKHR结合后,通过两种通路发挥作用:(1)cAMP-PKA通路:活化糖原磷酸化酶,使糖原水解产生葡萄糖-1-磷酸,最终转化为海藻糖[72-84].(2)cAMP-PKA通路激活TAG脂酶:该酶在Ca2+介导下定位到脂滴,将TAG分解生成DAG.在以脯氨酸为主要供能物质的甲虫中,AKH还可促进TAG分解产生的游离脂肪酸合成脯氨酸[83, 85].海藻糖和脯氨酸作为分解产物被释放到血淋巴,DAG则由载脂蛋白携带进入血淋巴,进而被运输到靶标组织进行氧化供能或再次储存.在食物限制情况下,心侧体还会分泌Lst作为降糖素,通过作用于胰岛素合成细胞上的Lst受体减少胰岛素分泌,从而调节胰岛素信号,进一步影响糖代谢[62].饥饿状态下的果蝇在临近死亡前会表现出亢奋的觅食活动,但当AKH基因缺失或负责表达AKHR基因的神经元失活时,这种觅食行为会受到抑制[22, 86],AKH基因过表达则会加剧饥饿引起的死亡率[87].富含脂类的食物会增强饥饿导致的亢奋活动,这与AKH对糖代谢的调控密切相关.高脂食物中的脂类被载脂蛋白运输到表达AKHR的章鱼胺分泌神经元后,通过抑制AMPK-TOR通路抑制神经元的自噬作用,使AKHR蛋白得以累积,最终介导高脂食物以增强饥饿状态下的亢奋行为,表明AKH在糖代谢与行为调控之间存在复杂联系,二者共同应对饥饿胁迫[88]. ...
The insect neuropeptide PTTH activates receptor tyrosine kinase torso to initiate metamorphosis
1
2009
... 在果蝇变态发育中,心侧体发挥着关键作用,这与促前胸腺激素(prothoracicotropic hormone,PTTH)和ImpL2密切相关.在幼虫时期,PTTH在昆虫脑部神经分泌细胞合成后,被转移到心侧体中储存,并在特定发育阶段被释放到血淋巴中,刺激前胸腺合成蜕皮激素,从而启动变态发生[89].另一种观点认为,心侧体可将轴突投射至前胸腺,作为蜕皮激素前体蜕皮酮合成器官,可直接释放PTTH,从而影响蜕皮激素调控的变态发育[75].当PTTH缺失时,果蝇发育过程中核因子κB(nuclear factor κB)的信号减弱,成虫体内炎症标志物显著下降,组织损伤和功能衰退的情况降低[90].心侧体可在细胞表面富集ImpL2,用于帮助幼虫维持饥饿情况下前胸腺中胰岛素信号的水平.心侧体前期将DILP2通过ImpL2束缚在心侧体上,当幼虫渡过临界体重后,即便面临饥饿等环境压力,心侧体也能释放DILP2至前胸腺,维持前胸腺营养信号活力、保障蜕皮酮的正常合成,从而帮助幼虫变态发育的顺利推进[91-92]. ...
NF-κB-mediated developmental delay extends lifespan in Drosophila
1
2025
... 在果蝇变态发育中,心侧体发挥着关键作用,这与促前胸腺激素(prothoracicotropic hormone,PTTH)和ImpL2密切相关.在幼虫时期,PTTH在昆虫脑部神经分泌细胞合成后,被转移到心侧体中储存,并在特定发育阶段被释放到血淋巴中,刺激前胸腺合成蜕皮激素,从而启动变态发生[89].另一种观点认为,心侧体可将轴突投射至前胸腺,作为蜕皮激素前体蜕皮酮合成器官,可直接释放PTTH,从而影响蜕皮激素调控的变态发育[75].当PTTH缺失时,果蝇发育过程中核因子κB(nuclear factor κB)的信号减弱,成虫体内炎症标志物显著下降,组织损伤和功能衰退的情况降低[90].心侧体可在细胞表面富集ImpL2,用于帮助幼虫维持饥饿情况下前胸腺中胰岛素信号的水平.心侧体前期将DILP2通过ImpL2束缚在心侧体上,当幼虫渡过临界体重后,即便面临饥饿等环境压力,心侧体也能释放DILP2至前胸腺,维持前胸腺营养信号活力、保障蜕皮酮的正常合成,从而帮助幼虫变态发育的顺利推进[91-92]. ...
Coupled sensing of hunger and thirst signals balances sugar and water consumption
2
2016
... 在果蝇变态发育中,心侧体发挥着关键作用,这与促前胸腺激素(prothoracicotropic hormone,PTTH)和ImpL2密切相关.在幼虫时期,PTTH在昆虫脑部神经分泌细胞合成后,被转移到心侧体中储存,并在特定发育阶段被释放到血淋巴中,刺激前胸腺合成蜕皮激素,从而启动变态发生[89].另一种观点认为,心侧体可将轴突投射至前胸腺,作为蜕皮激素前体蜕皮酮合成器官,可直接释放PTTH,从而影响蜕皮激素调控的变态发育[75].当PTTH缺失时,果蝇发育过程中核因子κB(nuclear factor κB)的信号减弱,成虫体内炎症标志物显著下降,组织损伤和功能衰退的情况降低[90].心侧体可在细胞表面富集ImpL2,用于帮助幼虫维持饥饿情况下前胸腺中胰岛素信号的水平.心侧体前期将DILP2通过ImpL2束缚在心侧体上,当幼虫渡过临界体重后,即便面临饥饿等环境压力,心侧体也能释放DILP2至前胸腺,维持前胸腺营养信号活力、保障蜕皮酮的正常合成,从而帮助幼虫变态发育的顺利推进[91-92]. ...
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
A local insulin reservoir in Drosophila alpha cell homologs ensures developmental progression under nutrient shortage
1
2022
... 在果蝇变态发育中,心侧体发挥着关键作用,这与促前胸腺激素(prothoracicotropic hormone,PTTH)和ImpL2密切相关.在幼虫时期,PTTH在昆虫脑部神经分泌细胞合成后,被转移到心侧体中储存,并在特定发育阶段被释放到血淋巴中,刺激前胸腺合成蜕皮激素,从而启动变态发生[89].另一种观点认为,心侧体可将轴突投射至前胸腺,作为蜕皮激素前体蜕皮酮合成器官,可直接释放PTTH,从而影响蜕皮激素调控的变态发育[75].当PTTH缺失时,果蝇发育过程中核因子κB(nuclear factor κB)的信号减弱,成虫体内炎症标志物显著下降,组织损伤和功能衰退的情况降低[90].心侧体可在细胞表面富集ImpL2,用于帮助幼虫维持饥饿情况下前胸腺中胰岛素信号的水平.心侧体前期将DILP2通过ImpL2束缚在心侧体上,当幼虫渡过临界体重后,即便面临饥饿等环境压力,心侧体也能释放DILP2至前胸腺,维持前胸腺营养信号活力、保障蜕皮酮的正常合成,从而帮助幼虫变态发育的顺利推进[91-92]. ...
Role of Phote-HrTH (Phormia terraenovae hypertrehalosemic hormone) in modulating the supercontractile muscles of the crop of adult Phormia regina Meigen
1
2014
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
A glucagon-like endocrine pathway in Drosophila modulates both lipid and carbohydrate homeostasis
1
2008
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
The adipokinetic hormone receptor modulates sexual behavior, pheromone perception and pheromone production in a sex-specific and starvation-dependent manner in Drosophila melanogaster
2
2016
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
... 最近的研究表明,埃及伊蚊卵巢内存在AKHR基因的表达[60],暗示AKH信号在生殖中可能有新的作用.另有研究显示,心侧体因表达瞬时受体电位 A1 通道蛋白(transient receptor potential A1)而对紫外线敏感[103],表明心侧体在应激反应中发挥关键作用,且AKH信号可调节抗氧化应激[104].在营养丰富的环境中,AKH基因和AKHR基因突变对突变体的发育(如孵化率、存活率、从产卵到羽化的时间)或适应性(如体型、繁殖力)无影响[38],表明AKH主要在极端条件(如饥饿)下发挥作用.饥饿胁迫会极大地促进脂肪体中脂类的动用,使生物体在缺乏食物的情况下可调动储备的能量[105].在短时间(4 h)禁食条件下,AKH通过一系列复杂的信号转导通路(包括肝激酶B1、盐诱导激酶3和组蛋白去乙酰化酶4)使FOXO去乙酰化,进而调控TAG脂酶Brummer基因的转录[106].在饥饿状态下,AKHR基因突变的果蝇雄虫交配率显著降低,对雄性特异性信息素的感应能力也减弱,同时,AKHR基因缺失的雌虫表皮中信息素的合成受到抑制.由此推测,在饥饿胁迫下,AKH/AKHR通路通过调控脂类调动影响雄虫的求偶行为和雌虫的生殖力[95, 98]. ...
Starvation promotes concerted modulation of appetitive olfactory behavior via parallel neuromodulatory circuits
1
2015
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
AKH-producing neuroendocrine cell ablation decreases trehalose and induces behavioral changes in Drosophila
1
2005
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
Adipokinetic hormone receptor gene identification and its role in triacylglycerol mobilization and sexual behavior in the oriental fruit fly (Bactrocera dorsalis)
1
2017
... 最近的研究表明,埃及伊蚊卵巢内存在AKHR基因的表达[60],暗示AKH信号在生殖中可能有新的作用.另有研究显示,心侧体因表达瞬时受体电位 A1 通道蛋白(transient receptor potential A1)而对紫外线敏感[103],表明心侧体在应激反应中发挥关键作用,且AKH信号可调节抗氧化应激[104].在营养丰富的环境中,AKH基因和AKHR基因突变对突变体的发育(如孵化率、存活率、从产卵到羽化的时间)或适应性(如体型、繁殖力)无影响[38],表明AKH主要在极端条件(如饥饿)下发挥作用.饥饿胁迫会极大地促进脂肪体中脂类的动用,使生物体在缺乏食物的情况下可调动储备的能量[105].在短时间(4 h)禁食条件下,AKH通过一系列复杂的信号转导通路(包括肝激酶B1、盐诱导激酶3和组蛋白去乙酰化酶4)使FOXO去乙酰化,进而调控TAG脂酶Brummer基因的转录[106].在饥饿状态下,AKHR基因突变的果蝇雄虫交配率显著降低,对雄性特异性信息素的感应能力也减弱,同时,AKHR基因缺失的雌虫表皮中信息素的合成受到抑制.由此推测,在饥饿胁迫下,AKH/AKHR通路通过调控脂类调动影响雄虫的求偶行为和雌虫的生殖力[95, 98]. ...
Adipokinetic hormone receptor mediates lipid mobilization to regulate starvation resistance in the brown planthopper, Nilaparvata lugens
0
2018
Role of adipokinetic hormone and adenosine in the anti-stress response in Drosophila melanogaster
1
2016
... 果蝇成虫心侧体的神经元轴突延伸到嗉囊,推测其可调节果蝇的嗉囊排空[5].嗉囊是碳水化合物储存的重要器官,对肌肉和脂肪体糖原的储存较少,所以调节嗉囊排空对于果蝇早期应对饥饿至关重要.在伏蝇(Phormia regina)中,这些神经元沿着嗉囊管道向下延伸,并投射到包裹嗉囊的收缩肌上,AKH被输送到这些肌肉并刺激肌肉收缩和嗉囊排空[93].饥饿状态下,AKH调节果蝇对饥饿的行为响应,其信号可调节食物搜索行为[86].饥饿状态下果蝇出现的亢奋觅食活动与AKH密切相关,AKH通过促进能量调动以维持机体活跃状态,促使昆虫积极寻找食物,从而补充糖类等营养物质[5, 45].消融心侧体细胞会减少果蝇对饥饿的过度活动和摄食反应,增加对饥饿的耐受性[5, 41].AKHR在食道下区的章鱼胺能神经元中表达[86],表明其对运动行为有影响.同区域中的四个AKHR神经元对调节进食和饮水行为起关键作用[91].研究发现,食道下神经节内的部分AKH受体表达神经元与味觉相关[94],且可支配触角叶,进而改变对信息素的偏好[95].此外,触角中AKHR的表达会随饥饿程度发生变化[96].当AKHR基因在褐飞虱中被沉默或在果蝇体内缺失时,这些昆虫的寿命会显著延长[97-100].这些结果说明AKH在调控取食行为方面发挥关键作用,通过影响果蝇对饥饿的感知和反应,调节食物摄取,以适应环境食物变化. ...
AKH-FOXO pathway regulates starvation-induced sleep loss through remodeling of the small ventral lateral neuron dorsal projections
2
2020
... 饥饿会阻碍果蝇的睡眠,其机制在于饥饿会导致含PDF的小侧腹神经元背向连接延展[101].当AKH基因或AKHR基因缺失时,饥饿诱发的这一反应及随后的睡眠丧失会被阻断.叉头框蛋白O(forkhead box protein O,FOXO)在调控神经元突触可塑性方面发挥重要作用,饥饿会增强FOXO的信号转导,但在AKH基因缺失的果蝇中,FOXO基因的表达下降.由此可知,AKH基因可通过调控FOXO基因的表达,抑制饥饿导致的小型腹侧外侧神经元(small ventral lateral neurons,s-LNv)背向连接延展和睡眠障碍,以实现对睡眠的调控,从而使果蝇在饥饿状态下维持适当的生理机能平衡,避免影响觅食与生存活动[101-102]. ...
... [101-102]. ...
Minibrain/Dyrk1a regulates food intake through the Sir2-FOXO-sNPF/NPY pathway in Drosophila and mammals
1
2012
... 饥饿会阻碍果蝇的睡眠,其机制在于饥饿会导致含PDF的小侧腹神经元背向连接延展[101].当AKH基因或AKHR基因缺失时,饥饿诱发的这一反应及随后的睡眠丧失会被阻断.叉头框蛋白O(forkhead box protein O,FOXO)在调控神经元突触可塑性方面发挥重要作用,饥饿会增强FOXO的信号转导,但在AKH基因缺失的果蝇中,FOXO基因的表达下降.由此可知,AKH基因可通过调控FOXO基因的表达,抑制饥饿导致的小型腹侧外侧神经元(small ventral lateral neurons,s-LNv)背向连接延展和睡眠障碍,以实现对睡眠的调控,从而使果蝇在饥饿状态下维持适当的生理机能平衡,避免影响觅食与生存活动[101-102]. ...
Drosophila TRPA1 isoforms detect UV light via photochemical production of H2O2
1
2015
... 最近的研究表明,埃及伊蚊卵巢内存在AKHR基因的表达[60],暗示AKH信号在生殖中可能有新的作用.另有研究显示,心侧体因表达瞬时受体电位 A1 通道蛋白(transient receptor potential A1)而对紫外线敏感[103],表明心侧体在应激反应中发挥关键作用,且AKH信号可调节抗氧化应激[104].在营养丰富的环境中,AKH基因和AKHR基因突变对突变体的发育(如孵化率、存活率、从产卵到羽化的时间)或适应性(如体型、繁殖力)无影响[38],表明AKH主要在极端条件(如饥饿)下发挥作用.饥饿胁迫会极大地促进脂肪体中脂类的动用,使生物体在缺乏食物的情况下可调动储备的能量[105].在短时间(4 h)禁食条件下,AKH通过一系列复杂的信号转导通路(包括肝激酶B1、盐诱导激酶3和组蛋白去乙酰化酶4)使FOXO去乙酰化,进而调控TAG脂酶Brummer基因的转录[106].在饥饿状态下,AKHR基因突变的果蝇雄虫交配率显著降低,对雄性特异性信息素的感应能力也减弱,同时,AKHR基因缺失的雌虫表皮中信息素的合成受到抑制.由此推测,在饥饿胁迫下,AKH/AKHR通路通过调控脂类调动影响雄虫的求偶行为和雌虫的生殖力[95, 98]. ...
Independent, reciprocal neuromodulatory control of sweet and bitter taste sensitivity during starvation in Drosophila
1
2014
... 最近的研究表明,埃及伊蚊卵巢内存在AKHR基因的表达[60],暗示AKH信号在生殖中可能有新的作用.另有研究显示,心侧体因表达瞬时受体电位 A1 通道蛋白(transient receptor potential A1)而对紫外线敏感[103],表明心侧体在应激反应中发挥关键作用,且AKH信号可调节抗氧化应激[104].在营养丰富的环境中,AKH基因和AKHR基因突变对突变体的发育(如孵化率、存活率、从产卵到羽化的时间)或适应性(如体型、繁殖力)无影响[38],表明AKH主要在极端条件(如饥饿)下发挥作用.饥饿胁迫会极大地促进脂肪体中脂类的动用,使生物体在缺乏食物的情况下可调动储备的能量[105].在短时间(4 h)禁食条件下,AKH通过一系列复杂的信号转导通路(包括肝激酶B1、盐诱导激酶3和组蛋白去乙酰化酶4)使FOXO去乙酰化,进而调控TAG脂酶Brummer基因的转录[106].在饥饿状态下,AKHR基因突变的果蝇雄虫交配率显著降低,对雄性特异性信息素的感应能力也减弱,同时,AKHR基因缺失的雌虫表皮中信息素的合成受到抑制.由此推测,在饥饿胁迫下,AKH/AKHR通路通过调控脂类调动影响雄虫的求偶行为和雌虫的生殖力[95, 98]. ...
Insect fat body: energy, metabolism, and regulation
1
2010
... 最近的研究表明,埃及伊蚊卵巢内存在AKHR基因的表达[60],暗示AKH信号在生殖中可能有新的作用.另有研究显示,心侧体因表达瞬时受体电位 A1 通道蛋白(transient receptor potential A1)而对紫外线敏感[103],表明心侧体在应激反应中发挥关键作用,且AKH信号可调节抗氧化应激[104].在营养丰富的环境中,AKH基因和AKHR基因突变对突变体的发育(如孵化率、存活率、从产卵到羽化的时间)或适应性(如体型、繁殖力)无影响[38],表明AKH主要在极端条件(如饥饿)下发挥作用.饥饿胁迫会极大地促进脂肪体中脂类的动用,使生物体在缺乏食物的情况下可调动储备的能量[105].在短时间(4 h)禁食条件下,AKH通过一系列复杂的信号转导通路(包括肝激酶B1、盐诱导激酶3和组蛋白去乙酰化酶4)使FOXO去乙酰化,进而调控TAG脂酶Brummer基因的转录[106].在饥饿状态下,AKHR基因突变的果蝇雄虫交配率显著降低,对雄性特异性信息素的感应能力也减弱,同时,AKHR基因缺失的雌虫表皮中信息素的合成受到抑制.由此推测,在饥饿胁迫下,AKH/AKHR通路通过调控脂类调动影响雄虫的求偶行为和雌虫的生殖力[95, 98]. ...
Feeding and fasting signals converge on the LKB1-SIK3 pathway to regulate lipid metabolism in Drosophila
1
2015
... 最近的研究表明,埃及伊蚊卵巢内存在AKHR基因的表达[60],暗示AKH信号在生殖中可能有新的作用.另有研究显示,心侧体因表达瞬时受体电位 A1 通道蛋白(transient receptor potential A1)而对紫外线敏感[103],表明心侧体在应激反应中发挥关键作用,且AKH信号可调节抗氧化应激[104].在营养丰富的环境中,AKH基因和AKHR基因突变对突变体的发育(如孵化率、存活率、从产卵到羽化的时间)或适应性(如体型、繁殖力)无影响[38],表明AKH主要在极端条件(如饥饿)下发挥作用.饥饿胁迫会极大地促进脂肪体中脂类的动用,使生物体在缺乏食物的情况下可调动储备的能量[105].在短时间(4 h)禁食条件下,AKH通过一系列复杂的信号转导通路(包括肝激酶B1、盐诱导激酶3和组蛋白去乙酰化酶4)使FOXO去乙酰化,进而调控TAG脂酶Brummer基因的转录[106].在饥饿状态下,AKHR基因突变的果蝇雄虫交配率显著降低,对雄性特异性信息素的感应能力也减弱,同时,AKHR基因缺失的雌虫表皮中信息素的合成受到抑制.由此推测,在饥饿胁迫下,AKH/AKHR通路通过调控脂类调动影响雄虫的求偶行为和雌虫的生殖力[95, 98]. ...