肾移植是当前器官移植领域基础研究的核心焦点之一,构建可靠的肾移植模型,对于提升临床医生的手术技巧、改进肾移植器官的灌注方式以及完善术后护理方案具有重要意义[1-2]。与啮齿类等小型实验动物相比,猪在解剖结构、生理功能及营养代谢特征方面与人类更加相似,是研究人类疾病较为理想的实验动物模型[3]。其中,猪肾脏的大小和解剖结构与人类高度相似,适合用于肾移植手术模型的构建研究。此外,相较于其他动物,伴侣动物(如猫、犬)寿命相对较长,其慢性肾病(chronic kidney disease,CKD)的患病率会随年龄的增长而显著上升[4-5],且易进展为肾功能衰竭。近年来,伴侣动物器官移植技术发展迅速,其在临床中的应用也不断扩展。因此,开展猪的同种异体肾移植手术研究,既能为临床医生开展人的肾移植手术技能训练提供动物模型,也能为兽医领域开展伴侣动物的肾移植手术积累经验。
版纳微型猪近交系选育自西双版纳傣族自治州境内的滇南小耳猪,全身毛色黑且被毛细密适中,头部长、耳朵短小、躯体和四肢矮小,尾巴较长。版纳微型猪近交系不仅体型矮小、性成熟较早,而且具有耐粗饲、抗逆性强、对炎热潮湿环境的适应性强等优良特性,是培育生物医学用实验动物的理想资源。版纳微型猪近交系各亚系平均连续性纯合片段(run of homozygosity,ROH)为5.35 Mbp,且长ROH片段(>10 Mbp)占29.7%,是目前已报道的近交程度较高的小型猪,平均基因组近交系数(fraction of the genome in runs of homozygosity,FROH)高达47.57%[6],已成为独立于滇南小耳猪的遗传资源[7]。
猪肾脏在大小和解剖结构方面与人类肾脏高度相似,且版纳微型猪近交系个体之间的差异较小,这使其成为构建肾移植模型的理想实验动物。因此,本研究选用版纳微型猪近交系为实验动物,建立同种异体肾移植技术,通过检测术后受体猪的血常规、肝功能、肾功能及病理组织学情况,对肾移植结果进行评估,以期为同种异体肾移植手术模型的构建及其术后护理积累经验,从而推动肾移植技术持续进步与完善。
1 材料与方法
1.1 实验动物
8头普通级的成年版纳微型猪近交系均由云南农业大学云南省小型猪基因编辑与异种器官移植重点实验室提供[SCXK(滇)K2020-0003];其中,供体猪D(♂,F4代,9月龄,35.5 kg)与受体猪R(♂,F4代,9月龄,36.0 kg)是全同胞兄弟,供/受体猪DR1(♀,F5代,9月龄,32.0 kg)和DR2(♂,F5代,9月龄,37.0 kg)是全同胞姐弟,供体猪D3(♂,F3代,12月龄,44.0 kg)和受体猪DR3(♂,F3代,12月龄,45.0 kg)为全同胞兄弟。另采集与供体猪、受体猪不同家系远亲同族的2头猪C1、C2的外周血作为配型实验中的质控。动物均饲养于普通环境,术前24 h禁食,自由饮水。动物实验在云南农业大学云南省小型猪基因编辑与异种器官移植重点实验室开展[SYXK(滇)K2020-0005],实验方案已通过云南农业大学生命科学伦理委员会审批(批号202105009)。
1.2 主要仪器和试剂
兽用自动血液细胞分析仪(型号BC-5000 Vet)购自深圳迈瑞动物医疗有限公司,流式细胞仪(型号A00-1-1102)购自美国Beckman Coulter Biotechnology公司,离心机(型号SC-3614)购自安徽中科中佳科学仪器有限公司,呼吸麻醉机(型号AX-400)和多参数兽用监护仪(型号C80-V)购自深圳科曼医疗设备有限公司,聚凝胺介质试剂盒(批号A211201)购自珠海贝索生物技术有限公司,猪外周血淋巴细胞分离试剂盒(批号20240913)购自天津市灏洋生物制品科技有限责任公司,兔补体血清(批号1003325314)购自美国Sigma公司,碘化丙啶(propidium iodide,PI,批号CR2307077)购自武汉塞维尔生物科技有限公司,注射用盐酸替来他明/盐酸唑拉西泮(舒泰™50,批号2024.04)购自法国Virbac公司,异氟烷(批号20230901)购自河北金达福药业有限公司,UW液(批号CHD090924)购自美国Preservation Solutions公司,甲泼尼龙琥珀酸钠注射液(批号20049721)购自美国Pfizer公司,呋塞米注射液(批号D42307224)购自湖北津药药业股份有限公司,肝素钠注射液(批号2410103)购自上海上药第一生化药业有限公司,青霉素钠(批号153240705)购自内蒙古联邦动保药品有限公司。
1.3 实验设计
本研究共进行4例同种异体肾移植手术,其中1例为健康猪(R)接受单肾移植,2例为猪(DR1和DR2)单肾切除后肾移植,另1例为猪(DR3)双肾切除后肾移植。三组手术对应的受体猪和供体猪编号见表1,具体如下:(1)猪D为供体,猪R为受体,猪R的双肾保留,在猪R右髂窝处移植猪D的左侧肾脏;(2)猪DR1为供体,猪DR2为受体,交换移植左肾,右肾保留;猪DR2为供体,猪DR1为受体,交换移植左肾,右肾保留;(3)猪D3为供体,猪DR3为受体,猪DR3摘除双肾,移植猪D3的左肾。术后对移植肾进行肾功能检测,以肾功能丧失作为人道终点,用5 mg/kg的舒泰肌内注射诱导麻醉后,用1.5%异氟烷与氧气混合气体维持麻醉,在深度麻醉状态下,耳缘静脉推注10%氯化钾溶液(0.3~0.5 mL/kg)行安乐死。
表1 肾移植手术的实验动物分组
Table 1
组别 Group | 受体猪编号 Recipient pig number | 供体猪编号 Donor pig number |
|---|---|---|
健康猪接受单肾移植 Single kidney transplantation in a healthy pig | R | D |
单肾切除后肾移植 Kidney transplantation after unilateral nephrectomy | DR1 | DR2 |
| DR2 | DR1 | |
双肾切除后肾移植 Kidney transplantation after bilateral nephrectomy | DR3 | D3 |
1.4 供体猪与受体猪交叉配血实验
使用聚凝胺介质试剂盒,按照试剂盒说明书进行交叉配血实验。实验猪经前腔静脉采血6 mL,分别置于不含抗凝剂的采血管(3 mL)和含有肝素钠的抗凝血管(3 mL)中,4 ℃静置2 h后,2 000×g离心5 min,分离血清和红细胞,使用生理盐水分别将血清和红细胞稀释至10%和5%的浓度,然后采用凝聚胺法进行血型交叉配血实验。血型鉴定主侧实验:受体猪血清+供体猪红细胞悬液。血型鉴定次侧实验:受体猪红细胞悬液+供体猪血清。1.5 mL 离心管中加血清50 μL,红细胞悬液25 μL,低离子介质0.6 mL,混匀,室温静置1 min;加聚凝胺溶液50 μL,混匀后室温下静置15 s;1 000×g离心18 s;弃上清液,管底保留约50 μL液体。轻摇试管,观察是否形成凝块,如未形成凝块,说明交叉配血实验结果为阴性,则重复实验;如形成凝块,于离心管中加入50 μL重悬液,轻轻混合,于肉眼或显微镜下观察实验结果。如果凝块可在1 min内分散,则交叉配血实验结果为阴性,供体猪和受体猪血型相配;如形成不同程度的凝块,则交叉配血实验结果为阳性,供体猪和受体猪血型不匹配。交叉配血实验结果必须在3 min内判读,每个组重复3次。
1.5 供体猪与受体猪细胞毒性配型实验
补体依赖的细胞毒性(complement-dependent cytotoxicity,CDC)实验参照参考文献[8]的实验流程开展。首先采集供体猪的外周血,使用猪外周血单核细胞分离液试剂盒分离获得猪外周血单个核细胞(peripheral blood mononuclear cell,PBMC)。每组反应分别设置阴性对照组(供体猪PBMC+PBS+兔补体血清)及实验组(供体猪PBMC+受体猪血清+兔补体血清),每种配型组合分别做3个复孔。受体血清2 000×g离心10 min,取200 μL上清,56 ℃ 30 min灭活补体。首先将PBMC的细胞浓度调整至103个/μL,37 ℃避光封闭30 min,500×g离心6 min后弃上清,用PBS溶液重悬细胞至104个/μL。取供体猪的PBMC悬液10 μL置于1.5 mL EP管中,加入PBS溶液(阴性对照组)或受体猪血清(实验组)100 μL,于37 ℃避光孵育2 h,孵育完成后加入1 mL预冷的PBS溶液终止实验,500×g离心6 min,弃上清。加入1 mL PBS溶液洗涤细胞,500×g离心6 min,弃上清,冰上保存。向反应体系中加入使用蒸馏水稀释好的兔补体血清(1∶50)75 μL,37 ℃恒温箱避光孵育30 min,最后加入20 μL的PI染料标记死亡细胞,室温避光孵育2 min后,采用流式细胞仪分析计算死亡细胞(PI阳性细胞)比例,并计算细胞死亡率。计算公式:细胞死亡率=1⁃(1⁃实验组阳性细胞率)/(1-阴性对照组阳性细胞率)。
1.6 肾脏移植
1.6.1 术前麻醉和术中监测
供体猪、受体猪经过肌内注射5 mg/kg舒泰诱导麻醉后,行气管插管,用1.5%浓度的异氟烷气体维持麻醉,呈仰卧位固定于手术台。通过前腔静脉采集各组猪的静脉血,术中持续生理盐水滴注,使用多参数兽用监护仪对供体猪和受体猪的多项生理指标(包括心电图、血氧饱和度、血压和体温)进行实时监测和记录。
1.6.2 供体猪肾脏的获取
沿腹中线做纵向切口,游离左肾及输尿管,远端结扎输尿管,游离左肾动脉至腹主动脉,游离肾静脉至下腔静脉。给予100 IU/kg体重的肝素钠静脉推注致供体猪全身血循环肝素化后,使用无损伤阻断钳阻断近心端腹主动脉和远心端腹主动脉,剪断肾动脉,使用无损伤阻断钳阻断肾静脉并结扎,摘取左侧肾脏。摘出的肾脏使用UW灌注液进行灌注,直至肾脏颜色变为苍白色、肾静脉流出液转清为止。
1.6.3 术式Ⅰ组肾移植
打开受体猪腹腔,充分游离髂外动脉和髂外静脉,使用无损伤阻断钳阻断它们后,将供体肾分别端-侧吻合于腹主动脉、髂外静脉,吻合动脉前快速静推注射甲泼尼龙10 mg/kg。于循环开放前静推注射呋塞米10 mg,开放输尿管上的血管夹后,可观察到供体肾的颜色逐渐变红,开放循环2 min后有尿液排出,端-端吻合供体猪和受体猪的输尿管,关闭腹腔,缝合手术切口。猪R和DR3的肾移植采用术式Ⅰ方案进行。
1.6.4 术式Ⅱ组肾移植
打开受体猪腹腔,游离腹主动脉和下腔静脉3~4 cm,将供体肾与受体猪的腹主动脉进行端-侧吻合,血管夹阻断左肾动脉后,开放腹主动脉。将供体肾的静脉与受体猪的下腔静脉吻合,静推注射甲泼尼龙10 mg/kg,呋塞米10 mg。缝合结束后开放血流,端-端吻合输尿管与膀胱,关闭腹腔,缝合手术切口。猪DR1和DR2肾移植采用术式Ⅱ方案进行。
1.6.5 移植猪术后护理和检测
术后1周内,密切观察受体猪的精神状态,及时清理伤口,保持伤口处干燥清洁,肌内注射青霉素钠(20 000 IU/kg)防止伤口感染。术后定期采集猪R、猪DR1、猪DR2和猪DR3外周血 5 mL进行血常规、肝功能和肾功能检测。
1.7 移植肾的病理组织学检测
受体猪DR1和DR3分别于肾移植术后第17天和第30天死亡。摘取受体猪的移植肾与自体肾,于4%多聚甲醛溶液中固定后,经石蜡包埋,用石蜡切片机切取4 μm厚的切片。石蜡切片经过二甲苯脱蜡和梯度乙醇水化处理后,将切片放入苏木精溶液中染色10 min,拿出切片用流水冲洗2 min;用移液枪吸取1%盐酸乙醇分化液滴加到切片上分化1 s,然后迅速用流水冲洗2 min;用移液枪吸取返蓝液滴加到切片上,10 s后用流水冲洗2 min,把冲洗后的切片放到伊红染液中染色5 min,然后拿出切片用流水冲洗去除多余的伊红染料。染色完成后,用中性树胶封片,在显微镜下观察染色结果并采集图片。
1.8 数据统计分析
采用Flowjo_v10.8.1软件对流式细胞仪检测数据进行处理分析,所有研究数据使用GraphPad Prism 8.0和Adobe Photoshop 2020软件进行作图。
2 结果
2.1 供体猪和受体猪的血型相配
图1
图1
供体猪和受体猪的交叉配血实验结果
Figure 1
Cross-matching test results between donor and recipient pigs
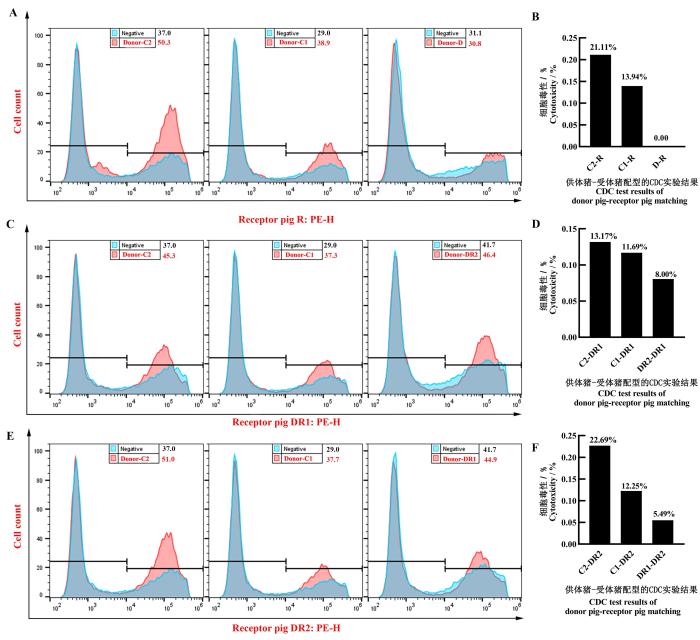
2.2 供体猪和受体猪配型的CDC实验结果
将供体猪C2、C1、D的PBMC分别与受体猪R的血清进行CDC配型实验,结果显示,C2-R、C1-R和D-R组合的PI阳性细胞率分别为50.3%、38.9%、30.8%,对应组合的细胞死亡率分别为21.11%、13.94%和接近0(图2A~B)。将供体猪C2、C1、DR2的PBMC与受体猪DR1的血清进行CDC配型实验,结果显示,C2-DR1、C1-DR1和DR2-DR1组合的PI细胞阳性率分别为45.3%、37.3%、46.4%,对应组合的细胞死亡率分别为13.17%、11.69%和8.0%(图2C~D)。将供体猪C2、C1、DR1的PBMC与受体猪DR2的血清进行CDC配型实验,结果显示,C2-DR2、C1-DR2和DR1-DR2组合的PI阳性细胞率分别为51.0%、37.7%、44.9%,对应组合的细胞死亡率分别为22.69%、12.25%和5.49%(图2E~F)。
图 2
图 2
供体猪和受体猪配型的CDC实验结果
Figure 2
Results of the CDC assay between donor and recipient pigs
2.3 同种异体肾移植后受体猪的存活情况
同种异体肾移植手术中(表2),在开放受体猪R、DR1、DR2和DR3输尿管上的血管夹后,均观察到供体肾的颜色变红,且分别于开放循环2、5、3、4 min后有尿液排出。术后第17天,对猪DR1进行超声检测,结果显示移植肾的功能丧失,实验到达人道终点,安乐死后摘取肾脏,行组织病理学检测;猪DR3于术后第30天死亡,解剖后摘取肾脏,行组织病理学检测;猪R和DR2在监测周期内(0~30 d)一直存活。
表2 同种异体猪肾移植手术情况
Table 2
供体猪或受体猪编号 Donor/recipient number | 供体肾重量/g Donor kidney weight/g | 热缺血时间 Warm ischemia time | 冷缺血时间 Cold ischemia time | 开放循环后开始排尿时间 Time to initiate urination after opening the loop |
|---|---|---|---|---|
| R | 118.9 | 1 min 5 s | 4 h 35 min | 2 min |
| DR1 | 87.3 | 2 min 5 s | 1 h 15 min | 5 min |
| DR2 | 115.7 | 5 min | 6 h 23 min | 3 min |
| DR3 | 100.5 | 4 min | 8 h 18 min | 4 min |
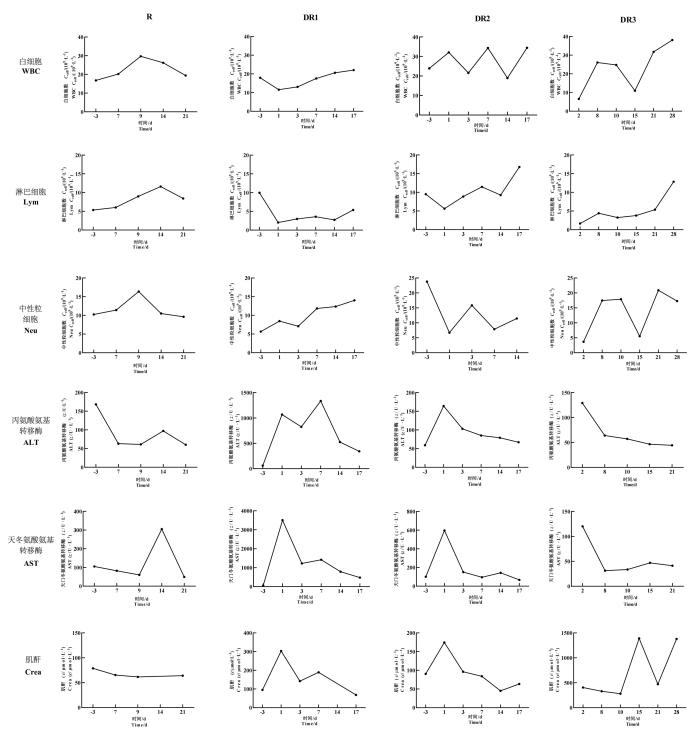
2.4 同种异体肾移植后供体猪和受体猪的血常规、肝功能和肾功能变化
血常规报告(图3)显示,在术前3 d至术后9 d,猪R的白细胞(white blood cell,WBC)、淋巴细胞(lymphocyte,Lym)和中性粒细胞(neutrophil,Neu)计数都有升高的趋势,之后14~21 d逐渐减低至术前水平;在术前3 d至术后17 d,猪DR1的WBC和Neu计数逐渐升高,Lym计数逐渐降低,猪DR2的WBC和Lym计数升高,Neu计数降低;术后0~28 d,猪DR3的WBC、Lym和Neu计数总体呈上升的趋势。肝功能和肾功能检测结果显示,猪DR1术后1 d时丙氨酸氨基转移酶(alanine aminotransferase,ALT)的水平升高(>1 000 U/L),术后7 d ALT的水平达到高峰(1 300 U/L);术后1 d天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)的水平达到高峰(>3 000 U/L);术后17 d,ALT和AST的含量仍处于较高水平(ALT,500 U/L;AST,700 U/L)。猪R、DR2和DR3的ALT和AST的含量均于17 d左右恢复到正常水平(图3)。猪R血清中的肌酐(creatinine,Crea)含量较为稳定,术后未有上升;猪DR1、DR2的血清Crea含量在术后1 d时有一过性的升高,之后逐渐恢复到正常水平(<100 μmol/L);猪DR3的Crea水平在术后2~10 d均低于500 μmol/L,术后11~28 d最高达到1 500 μmol/L。
图3
图3
肾移植前后供体猪和受体猪的血常规和肝功能、肾功能检测
Figure 3
Routine blood, liver, and kidney function test results of donor and recipient pigs before and after kidney transplantation
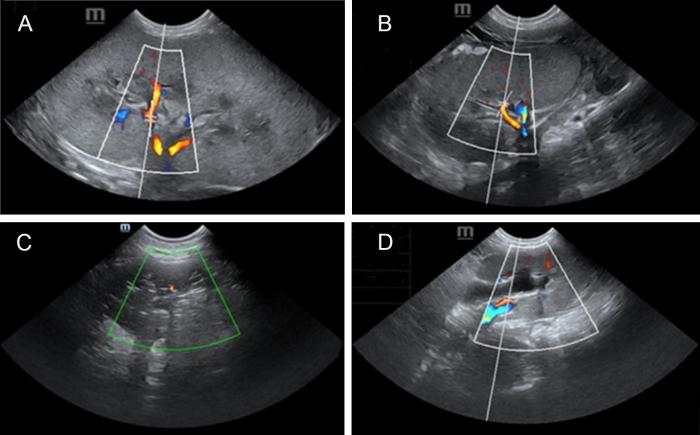
2.5 同种异体肾移植后供体猪和受体猪的肾脏血流变化
图4
图4
供体猪和受体猪的肾脏血流监测
Figure 4
Renal blood flow monitoring of donor and recipient pigs
2.6 同种异体肾移植后供体猪和受体猪的肾脏组织病理学变化
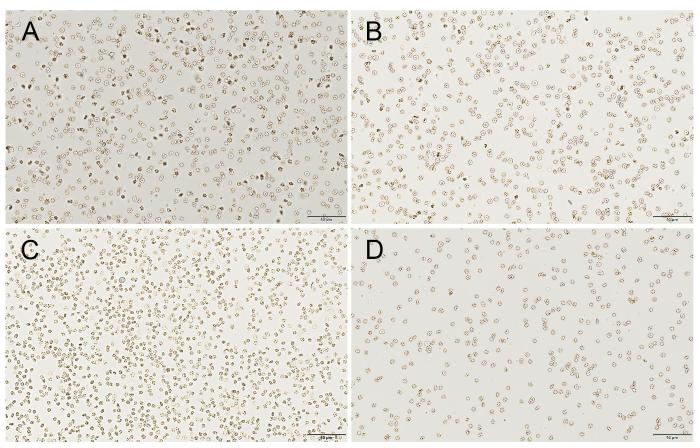
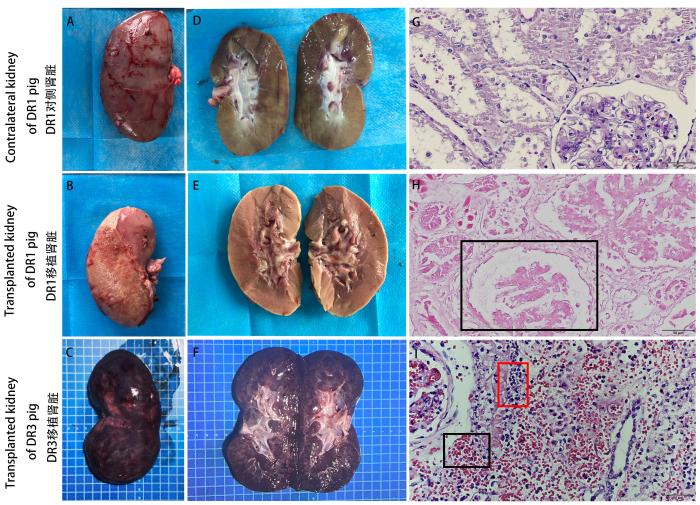
受体猪DR1在肾移植术后第17天行安乐死。剖取肾脏,观察大体病变,发现对侧健康肾脏未发生组织粘连,颜色为鲜红色,经生理盐水灌注后作为正常对照(图5A、D);移植肾已与周围组织粘连,不易分离,肾脏颜色呈土黄色(图5B、E)。猪DR3于术后30 d死亡,解剖发现猪DR3的移植肾脏未发生粘连,但该移植肾脏肿胀,呈深紫色(图5C、F)。HE染色结果显示,猪DR1的对侧健康肾脏肾小球和肾小管结构完整清晰,细胞核、细胞质清晰分明,着色均匀一致,肾小管中仅有少量红细胞,未见组织损伤(图5G),猪DR1的移植肾脏中肾小管形态轮廓不清晰,细胞核未见着色,表明其细胞核溶解(图5H);猪DR3移植肾脏的肾小球、肾小管中可见大量红细胞和淋巴细胞浸润(图5I)。
图5
图5
移植肾脏大体观察和HE染色
Figure 5
Gross observation and HE staining of transplanted kidney
3 讨论
本研究的CDC实验结果显示,版纳微型猪近交系个体间(D-R、DR1-DR2、DR2-DR1组合)的细胞死亡率均明显低于远亲同族猪C1、C2与近交系个体(C1-R、C2-R、C1-DR1、C2-DR1、C1-DR2、C2-DR2)配型时的细胞死亡率。另外,本研究开展的4例版纳微型猪近交系的同种异体肾移植手术均未发生超急性免疫排斥反应,猪DR3在双肾切除并植入左肾后存活30 d。这些结果在一定程度上证明了版纳微型猪近交系个体间的差异较小。我们前期开展的版纳微型猪近交系染色体水平基因组组装结果显示,各亚系长ROH片段(>10 Mb)占29.7%,平均FROH高达47.57%,是目前已知的近交程度较高的小型猪[6]。本文的研究结果与前期开展的版纳微型猪近交系的遗传分析结果一致,进一步印证了版纳微型猪近交系个体间差异较小的特性。
肾功能的恢复情况与血流动力学的稳定性是肾移植术后24~72 h的即刻评估重点,其中,术后受体猪血清中的Crea水平应在术后3 d内至少下降50%,同时还要通过多普勒超声评估移植肾的血流动力学稳定性,观察静脉血流是否通畅,排除肾动脉狭窄、血栓形成等血管并发症,确保移植肾血供正常[11-13]。临床上,肾移植手术的恢复期一般只需几天,但是当供体肾热缺血时间过长、保存不当或者血管吻合时间过长时,则会发生急性肾小管坏死(acute tubular necrosis,ATN),主要表现为少尿或无尿[14]。Crea是评估肾功能的核心指标之一,其浓度变化可反映肾小球滤过功能的损伤程度,当肾小球滤过功能下降(如肾小球损伤)时,Crea排泄减少,血清中Crea水平升高。本研究中,猪DR1、DR2和DR3术后第3天的Crea水平均有所下降。其中,猪DR2的Crea水平先降至100 μmol/L,后恢复到正常水平;猪DR3术后2~10 d的Crea水平低于500 μmol/L,提示移植肾脏在此期间仍有部分功能,11~28 d时Crea水平最高达到了1 500 μmol/L,表明此肾脏功能逐渐丧失。该变化趋势与临床上ATN患者术后表现极为相似,ATN患者术后2~3 d尿素和Crea水平异常,移植肾的功能迟迟不能恢复。
肾移植的超急性免疫排斥反应是肾移植后发生速度最快的一种免疫排斥反应,通常在移植后数分钟至24 h内出现[15]。猪DR1在术后17 d出现肾小管上皮细胞核溶解现象,而猪DR3在术后30 d仍存在严重的淋巴细胞浸润,这种组织学变化差异可能有不同的原因,早期的肾损伤(猪DR1)可能与缺血再灌注损伤有关(AST>3 000 U/L提示严重肝损伤继发的代谢紊乱[16]),后期淋巴细胞严重浸润、出血(猪DR3)可能源自强烈的细胞免疫应答[17]。可能的原因包括:(1)血管吻合术操作的精准度直接影响移植肾血供,局部组织坏死引发免疫反应,最终促使排斥反应发生;(2)供体肾获取时的热缺血时间过长或冷缺血期低温保存不当时会导致细胞能量代谢障碍,再灌注阶段活性氧暴发会引发细胞凋亡,这些病理反应均会加重炎症反应,增加排斥风险[18];(3)免疫抑制剂的及时、足量使用是预防和治疗免疫排斥反应的关键——通过抑制受体免疫系统活性,可有效减少受体对移植肾的免疫攻击[19];(4)术后感染是移植肾功能丧失的常见原因,若存在尿路重建或细菌感染未得到及时控制的问题,会进一步加剧移植肾的损伤[20]。
当前研究仍存在一定局限,后续研究将从以下方面优化:(1)规范手术操作流程,提高血管吻合等关键步骤的精准度;(2)改进供体肾脏的摘取与保存方法,缩短热缺血时间并优化低温保存条件;(3)加强术后监测与感染控制,以降低受体猪免疫排斥反应的发生率,从而延长移植肾存活时间;(4)全面评估该移植技术体系的效果与稳定性,并深入探究肾移植后受体动物长期的生理变化以及潜在并发症。
本研究以版纳微型猪近交系为实验动物,实施了4例猪-猪的同种异体肾移植手术,术后借助血常规、肝功能、肾功能以及彩色多普勒检查,对受体猪的生理指标和移植肾脏的功能展开监测。本研究构建的猪-猪同种异体肾移植技术体系,对于临床医生提升手术技巧、改进肾移植器官的灌注方式以及完善术后护理方案提供了借鉴,为医学实验动物肾移植教学奠定基础,同时对人类同种异体肾移植以及宠物器官移植也具有重要意义。
引用本文
张滢, 彭自伟, 杨畅, 等. 版纳微型猪近交系同种异体肾移植技术体系的建立[J]. 实验动物与比较医学, 2025, 45(5): 623-633. DOI: 10.12300/j.issn.1674-5817.2025.033.
ZHANG Y, PENG Z W, YANG C, et al. Establishment of allogeneic kidney transplantation technical system in banna miniature pig inbred strain[J]. Lab Anim Comp Med, 2025, 45(5): 623-633. DOI:10.12300/j.issn.1674-5817.2025.033.
作者贡献声明
张滢负责肾移植猪模型的护理、收集、整理实验数据、结果重复性验证及初稿撰写;
彭自伟负责肾移植猪模型B超检测、给药;
杨畅负责术前的交叉配血、CDC实验以及术中麻醉;
王晶负责肾移植猪模型术后的饲养管理和论文修订;作者贡献声明:
赵红芳参与肾移植手术和病理学检测;
陈根负责肾移手术操作,制定手术方案;
赵红业负责监督、领导实验研究的执行以及提供实验指导,并对初稿做审阅、评论或修订;
魏红江负责策划总体研究目标、获取基金资助、管理研究项目的执行,以及稿件审阅和修订。
医学伦理声明Medical Ethics Statement
本研究涉及的动物实验均已通过云南农业大学生命科学伦理委员会批准(编号202105009)。各实验过程均遵照中国实验动物相关法律法规条例进行。
Medical Ethics Statement
All animal experiments involved in this study have been approved by the Life Science Ethics Committee of Yunnan Agricultural University (No.202105009). All experimental procedures were conducted in compliance with China's relevant laws, regulations, and provisions on laboratory animals.
利益冲突声明
所有作者均声明本文不存在利益冲突。
参考文献
高压氧对大鼠肾移植后缺血再灌注肾组织中Th17细胞和单核巨噬细胞标志物表达的影响
[J].
Effect of hyperbaric oxygenation on expression of Th17 cell and monocyte macrophage markers of rat in renal tissue after renal transplantation ischemia reperfusion
[J].
小鼠移植肾再次移植动物模型的建立
[J].
Technique for mouse kidney graft re-transplantation
[J].
Importance of the pig as a human biomedical model
[J].
Prevalence and classification of chronic kidney disease in cats randomly selected from four age groups and in cats recruited for degenerative joint disease studies
[J].
Acute kidney injury in cats and dogs: a proportional meta-analysis of case series studies
[J].
A chromosome-scale reference genome of the Banna miniature inbred pig
[J].
Genomic consequences of intensive inbreeding in miniature inbred pigs
[J].
Flow cytometric detection of complement-activating HLA antibodies
[J].
The probability of receiving a kidney transplantation in end-stage kidney disease patients who are treated with haemodia-filtration or haemodialysis: a pooled individual participant data from four randomised controlled trials
[J].
Renal transplantation: pretransplant workup, surgical techniques, and surgical anatomy
[J].
彩色多普勒超声对移植肾动脉狭窄的临床应用价值
[J].
Clinical application value of color doppler ultrasound in transplanted renal artery stenosis
[J].
中国肾脏移植围手术期处理临床诊疗指南
[J].
Clinical guidelines for perioperative management of kidney transplantation in China
[J].
慢性移植肾功能不全诊疗技术规范(2019版)
[J].
Technical specification for diagnosis and treatment of chronic renal allograft dysfunction (2019 edition)
[J].
A comparative study on the efficacy of a retrograde perfusion technique and an antegrade perfusion technique for donor kidney recovery in transplantation in pigs
[J].
Developments in kidney xenotransplantation
[J].
CO2气腹对小猪原位肾移植缺血再灌注损伤影响的实验研究
[D].
Experimental research of ischemic reperfusion Injury with CO2 influence in small pig situ renal transplan-tation model
[D].
肾移植免疫学研究进展
[J].
Advances in immunology of renal transplantation research
[J].
Oxygenated versus standard cold perfusion preservation in kidney transplan-tation (COMPARE): a randomised, double-blind, paired, phase 3 trial
[J].
异种移植免疫学、生理学与生物安全挑战
[J].
Immunological, physiological, and biosafety challenges in xenotransplantation
[J].
Methicillin-resistant Staphylococcus aureus: molecular characterization, evolution, and epidemiology
[J].