1 资料与方法
1.1 文献检索
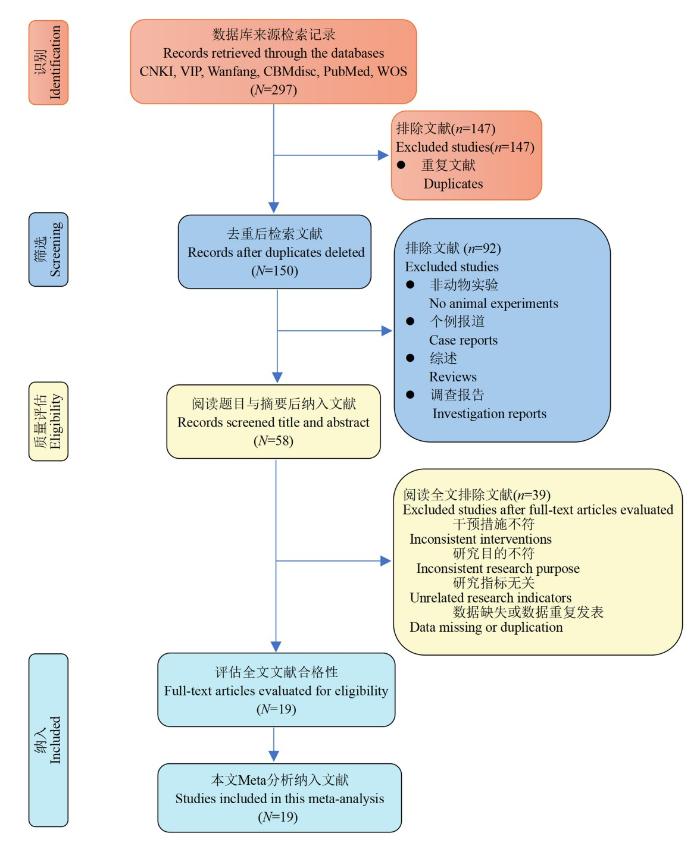
本文献检索流程遵循系统综述和荟萃分析优先报告条目(Preferred Reporting Items for Systematic reviews and Meta-Analyses,PRISMA),检索中国知网(China National Knowledge Infrastructure,CNKI)、维普中文科技期刊数据库(VIP Database for Chinese Technical Periodicals,VIP)、万方数据知识服务平台(Wanfang Data Knowledge Service Platform)、中国生物医学文献数据库(China Biomedical Literature Database, CBMdisc)、PubMed 以及 Web of Science(WOS)数据库中从建库起始至2025年3月关于黄芪(纯黄芪制剂)或其成分治疗AP的动物实验文献。黄芪或其成分的主要检索词为“黄芪、黄芪注射液、黄芪多糖、黄芪甲苷、黄芪总皂苷、毛蕊异黄酮;Astragalus plant、Huang Qi、astragalus injection、astragaloside、astragalus saponin、astragalus flavonoids”,AP的主要检索词为“急性胰腺炎、胰腺炎、acute pancreatitis、pancreatitis”。本文采用主题词与自由词相结合的检索策略,不设置文献语言及地域限制。以PubMed数据库为例,本文通过分别以“Astragalus plant”[Mesh]、“Huang Qi”[Supplementary Concept][Mesh]、“pancreatitis”[Mesh]为主题词,并以上述黄芪或其成分和AP的检索词为自由词,使用主题词与自由词相结合的检索策略进行检索。
1.2 纳入与排除标准
纳入文献应同时符合以下三项标准:(1)研究内容为黄芪或其成分(如黄芪多糖、黄芪甲苷、黄芪总皂苷、毛蕊异黄酮等)对AP的疗效或机制研究,同时包含足够数量、可供分析的任意观察指标,观察指标包括但不限于血清中检测到的AP病理过程中可能涉及的各类酶、细胞因子等;(2)基于动物实验开展研究,同时根据疾病诊断或模型评估标准明确其已成功构建AP模型;(3)实验对象分为实验组与对照组,实验组干预措施为仅使用纯黄芪制剂或黄芪成分治疗,对照组不干预或仅给予安慰剂。
文献排除标准:(1)报告为重复发表的实验数据;(2)未注明实验动物福利伦理审批号的动物实验报告;(3)实验结果数据不完整、无法溯源或无法确定其数据的真实性。
1.3 数据提取
提取纳入文献的主要信息,包括第一作者、发表年份、实验动物模型(物种、品种、品系和数量)、实验动物造模方法、干预方案、采样时间、评估指标及其检测数值。所有实验数据均来自文献,若原文中未列明具体数值,则通过查阅补充材料或测量统计图后换算获得。当研究涉及多个采样时间时,优先提取不同研究者使用最多的时间点,尽可能降低由于采样时间差异造成的偏倚。部分动物实验涉及到多个剂量时,为初步评估黄芪或其成分是否存在剂量-效应关系,提取高、低剂量组数据进行分析。
1.4 质量评估
研究文献由两位研究者收集,采用SYRCLE偏倚风险工具[10]对纳入文献的动物实验报告进行质量评估,通过协商、沟通确保数据准确。当对评估结果存在分歧时,由本文通信作者组织讨论,协商决定纳入文献最终评估结果。
1.5 统计学方法
本文使用软件RevMan 5.4.1进行统计分析。文献的异质性评估遵循Cochrane手册[11],采用Cochrane's Q检验和I2 统计量进行评价。当I2 值≤50%且P≥0.1时,认为各研究报告间存在低异质性;当I2 值>50%或P<0.1时,则认为研究报告间存在高异质性。对于低异质性研究,使用固定效应模型进行分析;对于高异质性研究,则使用随机效应模型进行分析。当研究指标的数值较大,影响数据可视化分析时,同时对黄芪或其成分组、对照组数据进行等比例缩小。各研究间测量指标的单位不统一或异质性较高时,采用标准化均数差(standardized mean difference,SMD)作为Meta分析的合并效应量;当单位统一且异质性较低时,则使用均数差(mean difference,MD)作为效应量。
2 结果
2.1 文献检索及纳入结果
图 1
2.2 文献质量评估结果
表1 纳入文献的基本特征
Table 1
第一作者 (发表年份) First author (publication date) | 动物 数量# Animal number# | 造模方法 Modeling method | 干预措施 Intervene measure | 采样时间 Sampling time | SYRCLE评分 Score of SYRCLE | 研究指标 Research indicator | |
|---|---|---|---|---|---|---|---|
黄芪或其成分组 Astragali radix or its ingredients group | 对照组 Control group | ||||||
孙海燕 (2006)[12] SUN H Y (2006) | 10/10 | SD大鼠,雌性,14∼15周龄,体重(200±20) g;胆胰管开口处逆行注入脱氧胆酸钠0.25%,0.5 mL/kg | 造模前皮下注射黄芪总皂苷80 mg/kg 2次,间隔1 h,末次给药30 min后造模 | 相同方法注 射生理盐 水10 mL/kg | 造模后 6 h和12 h | 4 | ①② |
傅强 (2006)[13] FU Q (2006) | 20/20 | 昆明小鼠,雌性,体重(25±3) g; 腹腔注射雨蛙素50 g/kg,间隔1 h,连续6次,末次注射后,腹腔注射脂多糖10 mg/kg | 末次造模注射后经尾静脉注射黄芪注射液0.5 mL/只 | 末次造模注射后经尾静脉注射等体积生理盐水 | 给药2、6、12、24 h后 | 3 | ① |
郭文学 (2008)[14] GUO W X (2008) | 8/8 | SD大鼠,雄性,体重(250±30) g;经胰胆管逆行注射5%牛磺胆酸钠0.11 mL/100 g,速度为0.24 mL/min | 术后即刻注射黄芪注射液 3 mL/100 g,并以2 mL/ 100(g·h-1)维持 | 相同方法注射等体积生理盐水 | 给药2、6、12 h后 | 3 | ①②⑦⑧ |
朱渊红 (2009)[15] ZHU Y H (2009) | 24/24 | SD大鼠,雌雄各半,体重(250±20) g;经胰胆管逆行注射3.5%牛磺胆酸钠(1 mL/kg) | 造模前24、12 h及造模后注射0.4 mL/100 g黄芪注射液 | 无 | 造模后6、9、12 h | 3 | ① |
朱渊红 (2012)[16] ZHU Y H (2012) | 8/8 | SD大鼠,雌雄各半,体重(250±20) g;胰胆管穿刺3.5%磺胆酸钠(1 mL/kg)注射 | 造模前24、12 h及造模后分别尾静脉注射黄芪注射液0.2 mL/100 g及0.4 mL/100 g | 无 | 造模后6 h | 3 | ⑦⑧ |
邱雷 (2014)[17] QIU L (2014) | 21/21 | SD大鼠,雄性,体重180∼200 g;胰胆管穿刺注射4%磺胆酸钠(1 mL/kg) | 造模前12 h和2 h腹腔注射黄芪甲苷40 mg/kg | 无 | 造模后24 h | 3 | ①②③④⑤ |
王少言 (2014)[18] WANG S Y (2014) | 15/15 | SD大鼠,雄性,12∼16周龄,体重250∼300 g;胰胆管穿刺注射5%磺胆酸钠(1 mL/kg) | 造模前12 h注射黄芪注射液0.2 mL/100 g | 等体积生理盐水 | 造模后6 h | 3 | ⑦⑧⑨ |
邱雷 (2015)[19] QIU L (2015) | 18/18 | SD大鼠,雄性,体重(250±30) g;4%磺胆酸钠(0.1 mL/100 g)逆行胆胰管注射;腹腔注射20% L-精氨酸(3 mg/kg)2次,间隔 1 h | 造模前2 h给予50 mg/kg溶于DMSO的黄芪甲苷 | 等体积DMSO | 造模后12、24、48 h | 3 | ①②③④⑤ |
王秉均 (2016)[20] WANG B J (2016) | 8/8 | SD大鼠,雌雄各半,体重180∼220 g;胰胆管穿刺注射5%磺胆酸钠(1 mL/kg) | 造模后立即单次灌胃给药黄芪多糖800 mg/kg | 等体积生理盐水 | 造模后 12 h | 4 | ①③⑦ |
郑洋 (2016)[21] ZHENG Y (2016) | 10/10 | SD大鼠,雌雄各半,体重(180 ± 20) g;胰胆管穿刺注射5%磺胆酸钠 | 造模后注射2 mL/kg黄芪注射液,6 h/次,共4次 | 等体积生理盐水 | 造模后 24 h | 3 | ③④⑥⑦⑧ |
郑蓓蓓 (2017)[22] ZHENG B B (2017) | 15/15 | SD大鼠,雄性,体重220~250 g;胰胆管穿刺注射5%磺胆酸钠 | 造模后腹腔注射300 mg/kg黄芪多糖 | 等体积生理盐水 | 造模后 24 h | 3 | ③④ |
MA R (2018) [23] | 20/20 | BALB/c小鼠,雄性,8∼10周龄,体重(20±2) g;腹腔内注射雨蛙肽(50 μg/kg),1次/h,连续8 h | 雨蛙肽给药前1 h腹腔注射25 mg/kg、50 mg/kg毛蕊异黄酮 | 等体积生理盐水 | 注射雨蛙肽后16 h | 3 | ①②③④ ⑥⑦⑧ |
吴爱详(2019)[24] WU A X (2019) | 20/20 | 昆明小鼠,6∼8周龄,体重(20.02 ± 2.65) g;腹腔注射20% L-精氨酸3 mg/kg,首次注射1 h后再注射1次 | 灌胃给药200 mg/kg黄芪甲苷,2 次/d,连续干预7 d | 等体积生理盐水 | 给药结束后 | 3 | ①②④ |
ZHU C J (2021)[25] | 6/6 | C57BL/6 N小鼠,雄性,8∼10周龄,体重18∼22 g;小鼠每小时腹腔注射4 g/kg L-精氨酸,持续2 h | 在第1次注射L-精氨酸前1 h,腹腔注射毛蕊异黄酮 25 mg/kg或50 mg/kg | 等体积生理盐水 | 造模后 | 3 | ①②④ |
金玲玲(2021)[26] JIN L L (2021) | 20/20 | SD大鼠,雌雄不限,6周龄,体重220∼250 g;胰胆管注射3.5%牛磺胆酸钠 | 造模后腹腔注射20 mg/kg、40 mg/kg黄芪总皂苷,给药体积为10 mL/kg | 等体积生理盐水 | 给药24 h | 3 | ① |
王欣 (2022)[27] WANG X (2022) | 20/20 | C57BL/6小鼠,6~8周龄,体重为18 ~ 22 g;腹腔注射pH=7,20% L-精氨酸2.5 mg/kg,以此间隔1 h注射2次 | 造模后黄芪总皂100 mg/kg灌胃1次/d,连续7 d | 无 | 末次给药后24 h | 3 | ①⑦⑧⑨ |
洪春霞(2023)[28] HONG C X (2023) | 8/8 | SD大鼠,体重为220~250 g;造模前禁食12 h,不禁水,麻醉经胰胆管穿刺后,3.5%牛黄胆酸按1 mL/kg在微量泵恒压下匀速注射 | 造模前12 h、24 h、造模后即刻、造模后12 h及24 h分别给予(0.10、0.15、0.20) mL/(100 g·d-1)黄芪注射液经尾静脉注射 | 无 | 末次给药后6 h | 3 | ①③ |
李振国(2024)[29] LI Z G (2024) | 20/20 | SD大鼠,雄性,体重200~220 g,胆管穿刺注射5%磺胆酸钠(1 mL/kg) | 造模后每天给予黄芪多糖400 mg/kg,持续灌胃2周 | 等体积生理盐水 | 造模后2周 | 3 | ③④⑤ |
HOU X T (2024) [30] | 6/6 | 昆明小鼠,7周龄,体重(35.0±2.5) g;胆胰管开口经十二指肠壁逆行注射脱氧胆酸钠(2.5%,0.5 mL/kg) | 小鼠后肢皮下注射黄芪总皂苷(20、40、80 mg/kg)两次,每隔1 h给药 | 10 mL/kg生理盐水 | 造模后6、12、24 h | 3 | ①⑦⑧ |
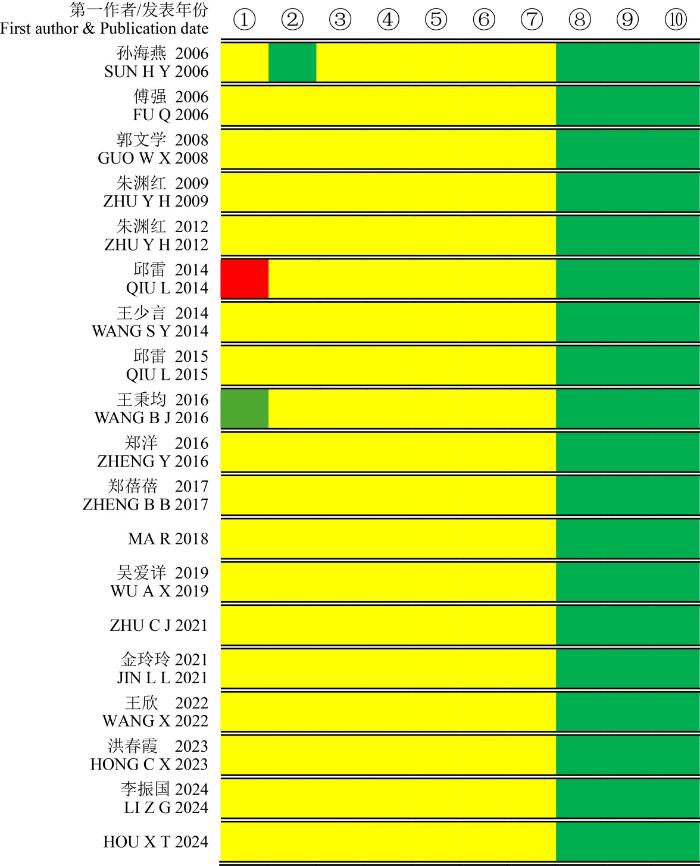
图2
图2
纳入文献的SYRCLE评分偏倚风险图
Figure 2
Risk of bias graph of SYRCLE ratings for the included studies
2.3 动物实验中黄芪注射液或黄芪成分影响临床疗效指标的Meta分析结果
2.3.1 血清淀粉酶(serum amylase,AMY)
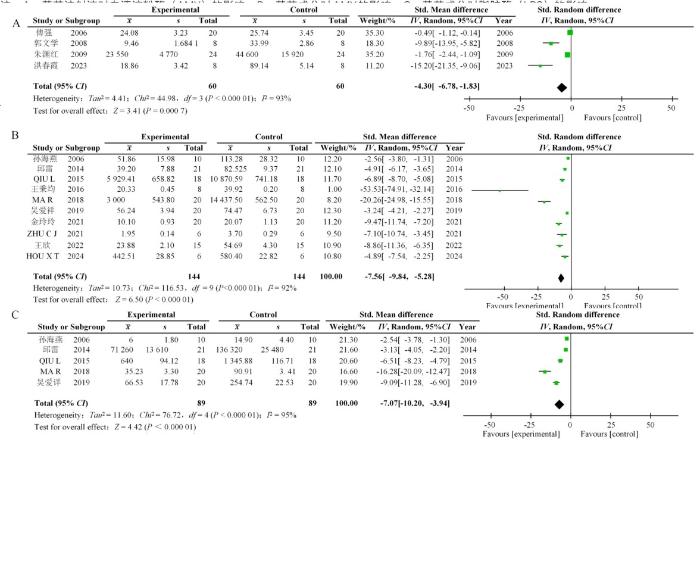
共有4篇文献报告了黄芪注射液对动物血清中AMY水平的影响。异质性分析结果表明,各研究间存在高度异质性(I2 =93%,P<0.000 01)。Meta分析结果显示,在昆明小鼠和SD大鼠动物实验中,黄芪注射液能降低AMY水平[SMD=-4.30,95%置信区间(confidence interval,CI)(-6.78,-1.83)],结果具有统计学意义(图3A)。
2.3.2 脂肪酶
共有5篇文献探讨了黄芪成分对脂肪酶(lipase,LPS)的影响,包括黄芪甲苷与毛蕊异黄酮。异质性分析结果显示,文献间存在高异质性(I2 =95%,P<0.000 01);Meta分析结果表明,在SD大鼠、BALB/c小鼠、昆明小鼠动物实验中,黄芪成分可以显著降低LPS水平[SMD=-7.07,95%CI(-10.20,-3.94)](图3C)。
2.3.3 炎症介质
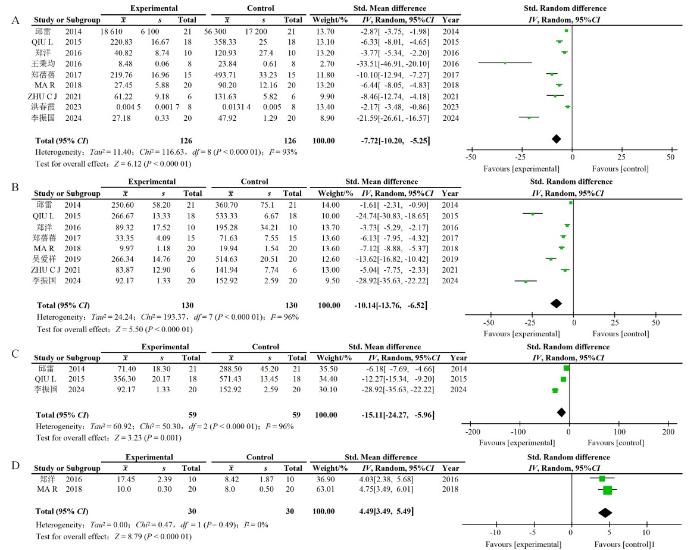
提取文献数据并进行Meta分析,共有9篇文献显示黄芪注射液或黄芪成分能显著降低肿瘤坏死因子(tumor necrosis factor,TNF)-α的水平[SMD=-7.72,95%CI(-10.20,-5.25)](图4A);共有8篇文献显示黄芪注射液或黄芪成分能抑制白细胞介素(interleukin,IL)-6的产生[SMD=-10.14,95%CI(-13.76,-6.52)](图4B);共有3篇文献表明黄芪成分能降低IL-1β水平[SMD=-15.11,95%CI(-24.27,-5.96)](图4C);共有2篇文献显示黄芪注射液及黄芪成分能抑制IL-10的下调[SMD=4.49,95%CI(3.49,5.49)](图4D)。在AP疾病发展过程中,黄芪注射液及黄芪成分可降低TNF-α、IL-6、IL-1β的水平,同时升高IL-10的水平。但受限于现有文献数量,仅分别有2篇文献涵盖IL-1β和IL-10指标,因此分析结果存在一定的局限性。
图4
图4
黄芪或其成分治疗急性胰腺炎后有关实验动物炎症因子的Meta分析森林图
Figure 4
Forest plot of the meta-analysis on inflammatory mediators in experimental animals with acute pancreatitis after treatment with Astragali Radix or its ingredients
2.3.4 氧化因子
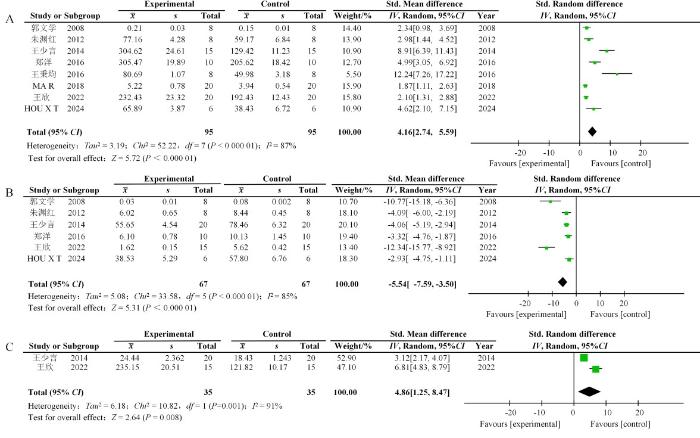
共有8篇文献报道了黄芪注射液或黄芪成分在AP疾病进展中对氧化/抗氧化平衡相关氧化因子的影响。其中8篇文献均涉及超氧化物歧化酶(superoxide dismutase,SOD)指标,Meta分析结果显示,黄芪注射液或黄芪成分能抑制SOD的下调[SMD=4.16,95%CI(2.74,5.59)](图5A);有6篇文献报道了黄芪注射液或黄芪成分对丙二醛(malondialdehyde,MDA)的作用,Meta结果表明它们能降低MDA的水平[SMD=-5.54,95%CI(-7.59,-3.50)](图5B);有2篇文献显示黄芪注射液和黄芪总皂苷能抑制谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)的下调[SMD=4.86,95%CI(1.25,8.47)](图5C)。
图5
图5
黄芪注射液或黄芪成分治疗急性胰腺炎后有关实验动物氧化/抗氧化平衡过程的Meta分析森林图
Figure 5
Forest plot of the meta-analysis on oxidative and antioxidant equilibrium in experimental animals with acute pancreatitis after treatment with Astragali Radix injection or Astragali Radix ingredients
2.4 动物实验中黄芪注射液或黄芪成分用药剂量与临床疗效相关性的Meta分析结果
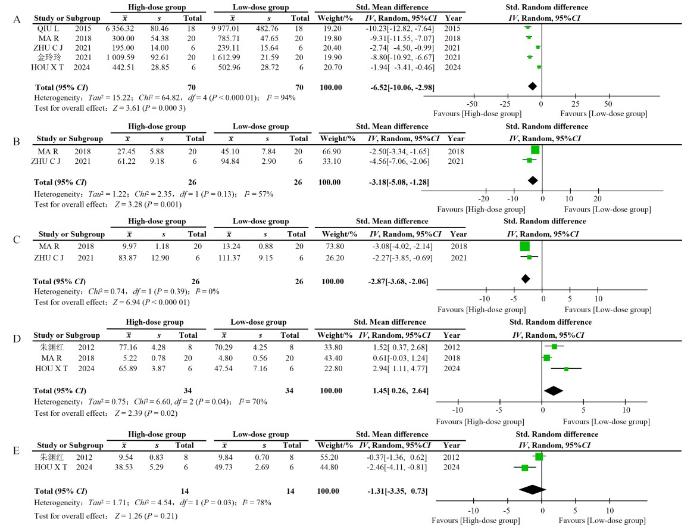
共有6篇文献研究设置了高、低剂量组,干预药物包括黄芪注射液、黄芪总皂苷、毛蕊异黄酮,涵盖AMY、TNF-α、IL-6、SOD、MDA 5项指标。黄芪注射液及黄芪成分的给药剂量与AP实验动物指标之间的Meta分析结果表明,高剂量组比低剂量组更能降低AMY的水平[SMD=-6.52,95%CI(-10.06,-2.98)](图6A);在炎症介质中,黄芪注射液及黄芪成分的给药剂量与TNF-α[SMD=-3.18,95%CI(-5.08,-1.28)](图6B)和IL-6[SMD=-2.87,95%CI(-3.68,-2.06)](图6C)水平的降低呈现出剂量相关性;在氧化因子方面,高剂量组更能促进SOD水平的升高[SMD=1.45,95%CI(0.26,2.64)](图6D)。高剂量组与低剂量组的MDA水平无显著差异[SMD=-1.31,95%CI(-3.35,0.73](图6E)。以上结果均具有统计学意义。由于仅有6篇文献中设置了浓度梯度,且仅包括5项指标,因此分析结果存在一定的局限性。
图6
图6
不同剂量的黄芪注射液或黄芪成分治疗急性胰腺炎后有关实验动物临床病理指标的Meta分析森林图
Figure 6
Forest plot of a meta-analysis on clinicopathological indicators in experimental animals after treatment of acute pancreatitis with different doses of Astragali Radix injection or Astragali Radix ingredients
2.5 敏感性分析与发表偏倚风险结果
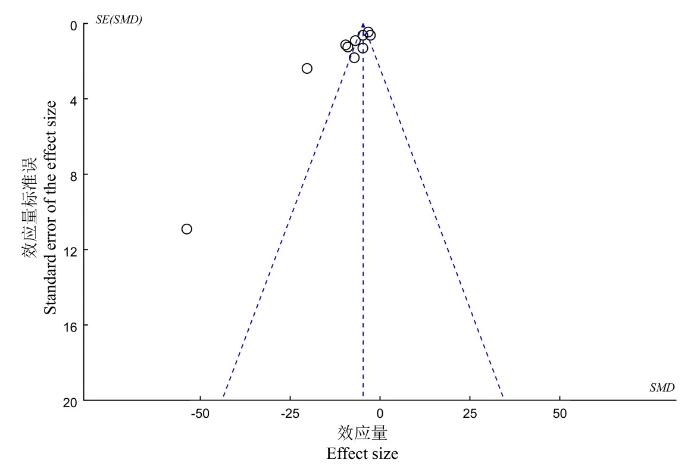
在RevMan 5.4.1软件上对文献使用留一法进行敏感性分析,未发现有能显著影响异质性指标的研究。结合文献数量及文献语言类型综合考虑,基于黄芪成分(黄芪多糖、黄芪甲苷、黄芪总皂苷、毛蕊异黄酮)影响AMY的相关文献制作漏斗图并进行Egger's test检验。漏斗图结果显示散点非两端对称,Egger's test检验结果为P<0.05,提示纳入文献存在一定的发表偏倚风险(图7)。
图7
图7
黄芪成分影响血清淀粉酶的漏斗图
Figure 7
Funnel plot of effects of Astragali Radix ingredients on AMY
3 讨论
炎症介质驱动的炎症反应在AP的发生发展中具有关键作用,可导致组织损伤和器官功能障碍[39]。AP中被激活的胰酶可促进多种炎症因子(如TNF-α、IL-6、IL-1β等)的生成,这些炎症因子通过触发“炎症级联反应”,导致患者出现全身炎症反应综合征与多器官功能障碍综合征[40]。既往研究表明,降低大鼠血清中TNF-α、IL-6和IL-1β的水平能有效缓解AP[41-42]。同时,IL-10可以通过抑制促炎细胞因子的产生与巨噬细胞和中性粒细胞的活化,从而减少炎症因子的释放,并抑制胰腺细胞的凋亡与坏死[43]。本文的Meta分析结果表明,黄芪及其成分可能通过下调部分促炎性细胞因子(TNF-α、IL-6、IL-1β)的水平和上调部分抗炎细胞因子(IL-10)的水平综合调控炎症因子网络,从而发挥潜在的治疗作用。然而,当前纳入分析的研究中涉及IL-1β和IL-10指标的文献数量较少,该分析结果存在一定的局限性,未来仍需开展更多的相关研究,以进一步阐明黄芪及其成分对于AP疾病进展中各类炎症因子的影响。
活性氧(reactive oxygen species,ROS)的产生与释放可影响AP最终组织损伤的严重程度,ROS主要来源于炎性缺氧的胰腺组织以及病变初始阶段浸润于胰腺组织的中性粒细胞。富含ROS且过度激活的白细胞可迁徙至肺部,产生大量过氧化物(如MDA),下调SOD和GSH-Px等内源性抗氧化关键酶的活性,进而导致多种并发症[44]。本文的Meta分析结果显示,黄芪注射液可显著增强SOD和GSH-Px的活性,并降低MDA水平,表明黄芪注射液可能通过干预AP疾病进展中的氧化/抗氧化平衡过程发挥治疗作用。
本文分析结果显示,黄芪及其成分(黄芪注射液、黄芪总皂苷、毛蕊异黄酮)对AP相关指标(AMY、TNF-α、IL-6、SOD)的影响呈剂量相关性,然而未证明剂量高低对MDA指标的影响。黄芪及其活性成分的药用安全性在既往临床及基础研究中均得到了一定的验证,但长期、大剂量使用仍可能引发肝功能和肾功能损伤及生殖发育毒性等不良反应[45]。但现有文献中仅有6项研究设置了药物的浓度梯度,且仅覆盖5项指标,因此该分析结果同样存在一定的局限性。未来仍需开展相应的动物实验研究,以明确黄芪及其成分的作用效果与剂量间的关系,并探索安全剂量阈值。
本研究结果表明,纳入文献间存在较高的异质性(I²>50%)。首先,纳入文献中实验动物种属与造模方法存在差异:纳入文献中使用的实验动物包括SD大鼠、C57BL/6小鼠、BALB/c小鼠和昆明小鼠4个品系,造模制剂包括磺胆酸钠、雨蛙素、牛黄胆酸、L-精氨酸等,不同的实验动物和不同的造模制剂可能会诱发不同程度的AP,从而影响黄芪的疗效。其次,各文献间黄芪实验组的给药方式和给药剂量存在差异,如存在静脉注射与灌胃给药等给药途径,黄芪注射液剂量由0.10 mL/100 g至3 mL/100 g不等。此外,治疗周期、采样时间、测量方法与设备之间也存在差异。以上原因均有可能成为文献间异质性的来源。同时本文经漏斗图分析发现,纳入文献存在一定的发表偏倚风险。但本研究采用SMD作为合并效应量,并使用随机效应模型进行分析,以尽可能降低高异质性所产生的影响,在一定程度上保证分析结果的准确可靠。在本研究对纳入文献进行质量评估时发现,纳入文献中普遍存在较多不确定的偏倚风险。这些不确定的偏倚风险主要出现在随机化与实验未明确采用盲法等问题上,因此在后续开展的相关动物实验中,可以着重考虑规范随机化过程,包括采用如随机数表法、区组随机化等方法科学分组,以进一步实现分配隐藏、随机化安置与饲养;同时,实验过程中尽量采用盲法操作,以实现高质量的动物实验。
综上所述,多项动物实验研究表明,黄芪注射液及其成分能有效改善AP相关特异性指标(如AMY和LPS)。其潜在作用机制可能包括:调节炎症因子网络(如下调TNF-α、IL-6和IL-1β的水平,上调IL-10的表达),以及干预氧化/抗氧化平衡过程(如升高SOD和GSH-Px的活性,降低MDA的水平)。同时,除MDA外,黄芪及其成分对于降低AMY、TNF-α和IL-6的水平,提高SOD的活性方面呈现一定的剂量相关性。然而,现有研究存在较高异质性、发表偏倚、动物模型与人体病理之间存在差异等问题,因此未来仍需进一步开展高质量的动物实验研究,如通过开展多中心的随机对照双盲动物实验等,以尽可能地降低各类偏倚风险,深入探索黄芪及其成分对于AP的疗效和相关的药理作用机制。
引用本文
曹星新, 李艾亦, 侯婧涵, 等. 黄芪或其成分治疗急性胰腺炎的动物实验 Meta 分析[J]. 实验动物与比较医学, 2025, 45(5): 561-573. DOI:10.12300/j.issn.1674-5817.2025.026.
CAO X X, LI A Y, HOU J H, et al. Meta-Analysis of animal experiments on astragali radix or its ingredients for acute pancreatitis[J]. Lab Anim Comp Med, 2025, 45(5): 561-573. DOI:10.12300/j.issn.1674-5817.2025.026.
作者贡献声明
曹星新负责方案策划、数据策划、方法设计、软件处理、初稿写作;
李艾亦负责有效验证、可视化,参与软件处理;
侯婧涵负责调查研究;
李明学参与方法设计、软件处理;
李艳艳参与方法设计、项目管理;
靳玮华参与形式分析、提供资源;
杨凤梅参与调查研究、提供资源;
段素琴参与方法设计、获取资助、项目管理;
和占龙负责获取资助、项目管理、监督指导、写作审编。
利益冲突声明
本文涉及的单位和作者均无利益冲突。
参考文献
Acute pancreatitis: a review
[J].
Impact of characteristics of organ failure and infected necrosis on mortality in necrotising pancreatitis
[J].
Burden of pancreatitis and associated risk factors in China, 1990 to 2019: a systematic analysis for the Global Burden of Disease Study 2019
[J].
Acute pancreatitis
[J].
通腑逐瘀方联合常规西药治疗腑实热结证急性胰腺炎临床研究
[J].
Clinical study on Tongfu Zhuyu decoction combined with conventional western medicine for acute pancreatitis with syndrome of bowel excess and heat bind
[J].
Acute pancreatitis
[J].
A review of the botany, phytochemistry, traditional uses, pharmacology, toxicology, and quality control of the Astragalus memeranaceus
[J].
黄芪注射液对急性胰腺炎患者氧化应激状态及肠黏膜屏障功能的影响
[J].
Effects of Huangqi Injection on the oxidative stress and intestinal mucosal barrier function in patients with acute pancreatitis
[J].
黄芪注射液对急性胰腺炎肠道屏障功能和微炎性反应状态的影响
[J].
Clinical study on Huangqi injection on intestinal barrier function and micro inflammatory state in patients with acute pancreatitis
[J].
Efficacy and safety of small extracellular vesicle interventions in wound healing and skin regeneration: a systematic review and meta-analysis of animal studies
[J].
Efficacy and safety of prophylaxis for venous thromboembolism in brain neoplasm patients undergoing neurosurgery: a systematic review and Bayesian network meta-analysis
[J].
黄芪总苷对实验性急性胰腺炎的保护作用
[J].
Effects of astragalosides on experimental acute pancreatitis
[J].
急性出血坏死性胰腺炎小鼠辅助性T细胞亚群1/2的变化规律及中药干预作用研究
[J].
Study on regularity of changes of helper T cell subgroup Th1/Th2 and interference effect of traditional Chinese medicine in mice with acute hemorrhage necrotizing pancreatitis
[J].
重症急性胰腺炎时MDA、SOD与肝脏微循环变化及黄芪干预的实验研究
[D].
Severe acute pancreatitis MDA, SOD and liver microcirculation changes and the experimental intervention study of Astragalus
[D].
黄芪注射液对SAP肺损伤大鼠的实验研究
[J].
The experimental study on Astragalus to rats with lung injury associated with severe acute pancreatitis
[J].
黄芪注射液对SAP肺损伤大鼠SOD、MDA及肺组织bcl-2、bax蛋白表达的影响
[J].
Effects of Astragalus injection on SOD, MDA and the expression of bcl-2 and bax protein in lung tissue of rats with SAP lung injury
[J].
黄芪甲苷对实验性大鼠重症急性胰腺炎的治疗作用
[J].
Therapeutic effects of astragaloside Ⅳ on severe acute pancreatitis in rats
[J].
黄芪注射液对重症急性胰腺炎大鼠外 周血清氧化相关物质的影响
[J].
Effect of Huangqi injection on oxidative relevant materials of peripheral serum in rats with severe acute pancreatitis
[J].
Astragaloside Ⅳ ameliorates acute pancreatitis in rats by inhibiting the activation of nuclear factor-κB
[J].
黄芪多糖对大鼠重症急性胰腺炎的作用及机制
[J].
Effects of Astragalus polysaccharides on rats with severe acute pancreatitis and underlying mechanisms
[J].
黄芪注射液对急性胰腺炎大鼠肠道屏障功能的影响
[J].
Effects of Astragalus injection on intestinal barrier functions in rats with acute pancreatitis
[J].
黄芪多糖对重症急性胰腺炎大鼠肠黏膜屏障损伤的保护作用
[D].
Protection of astragalus polysacharin on intestinal barrier dysfunction in rats with severe acute pancreatitis
[D].
Calycosin alleviates cerulein-induced acute pancreatitis by inhibiting the inflammatory response and oxidative stress via the p38 MAPK and NF-κB signal pathways in mice
[J].
黄芪甲苷对重症急性胰腺炎小鼠胰腺的影响
[J].
Effects of Astragalus glycoside in severe acute pancreatitis mice
[J].
Calycosin attenuates severe acute pancreatitis-associated acute lung injury by curtailing high mobility group box 1 - induced inflammation
[J].
黄芪总皂苷对重症急性胰腺炎大鼠肠道损伤的保护作用及对肠组织p38MAPK/NF-κB表达的影响
[J].
Total saponins of Astragalus has protective effect on intestinal injury in rats with severe acute pancreatitis and its effect on P38MAPK/NF-κB expressions in intestinal tissues
[J].
黄芪总皂苷通过激活Nrf2/HO-1信号通路缓解L-精氨酸诱导的小鼠急性胰腺炎氧化损伤的研究
[J].
Study on the effect of Astragalus saponins on oxidative damage of L-arginine induced acute pancreatitis in mice by activating Nrf2/HO-1 signaling pathway
[J].
黄芪注射液通过调控mTOR/p70S6K信号通路对急性出血坏死型胰腺炎肺损伤炎症反应的影响
[J].
Astragalus injection improves inflammatory response in lung injury in acute hemorrhagic necrotizing pancreatitis by regulating the mTOR/p70S6K signal pathway
[J].
黄芪多糖对大鼠急性胰腺炎的作用及其机制研究
[J].
Effect of Astragalus polysac-charides on acute pancreatitis in rats and its mechanism
[J].
Antioxidative effect of astragalosides on acute pancreatitis in mice
[J].
Burden and Cost of Gastrointestinal, Liver, and Pancreatic Diseases in the United States: Update 2018
柴胡龙骨牡蛎汤对肝胆湿热证急性胰腺炎患者的临床疗效
[J].
Clinical effect of Chaihu Longgu Muli decoction on acute pancreatitis with hepatobiliary damp-heat syndrome
[J].
中药辅助治疗经内镜逆行胰胆管造影术后急性胰腺炎研究进展
[J].
Research progress on traditional Chinese medicine assisted treatment of acute pancreatitis after endoscopic retrograde cholangiopan-creatography
[J].
黄芪注射液对病毒性心肌炎患者外周血NLRP3炎性小体表达的影响
[J].
Influence of Huangqi injection on the expressions of NLRP3 inflammasome in peripheral blood of patients with viral myocarditis
[J].
黄芪注射液联合布地奈德对支气管哮喘急性发作患者肺功能的影响
[J].
Effect of Astragalus injection combined with budesonide on lung function in patients with acute attack of bronchial asthma
[J].
中国急性胰腺炎诊治指南(2021)
[J].
Guidelines for diagnosis and treatment of acute pancreatitis in China(2021)
[J].
2019 WSES guidelines for the management of severe acute pancreatitis
[J].
黄芪多糖调节脂联素/TLR/NF-κB信号通路对溃疡性结肠炎小鼠的治疗作用
[J].
Regulatory effect of Astragalus polysaccharide on adiponectin/TLR/NF-κB signal pathway in mice with ulcerative colitis
[J].
Acute pancreatitis: a multifaceted set of organelle and cellular interactions
[J].
The mechanism of lung and intestinal injury in acute pancreatitis: a review
[J].
Qingyi granules ameliorate severe acute pancreatitis in rats by modulating the gut microbiota and serum metabolic aberrations
[J].
Amuc_1100 pretreatment alleviates acute pancreatitis in a mouse model through regulating gut microbiota and inhibiting inflammatory infiltration
[J].
Pirfenidone increases IL-10 and improves acute pancreatitis in multiple clinically relevant murine models
[J].
Autophagy-mediated ferroptosis is involved in development of severe acute pancreatitis
[J].
黄芪对中枢神经系统的药理作用及毒理研究现状
[J].
Review on neuroprotection effect of Astragali Radix on central nervous system and related toxicology
[J].