随着实验动物科学的快速发展,实验动物福利与伦理理念已深入生物医学科技工作者心中。实验动物“五大自由”(5 freedoms)和“替代、减少、优化”(Replacement, Reduction, Refinement,3Rs)原则及其内涵被充分解读并用于指导动物实验活动,基于此的研究成果被广泛认可。
作为研究传染病传播方式、发病机制及抗感染药物等方面的关键环节,感染性动物疾病模型受到高度重视。为获得最理想的动物疾病模型,不同种属的实验动物被用于模型筛查研究中[1]。在感染性动物疾病模型的制备及应用过程中,要求动物饲养在负压屏障环境中,在接种病原体发病后,不可避免地会产生疼痛等不适症状。虽然这种不适可以通过镇痛药物来缓解,但在部分实验过程中,动物接受治疗或镇痛等操作会影响实验关键数据的获取,并且通常以动物的死亡(通常采用安乐死)作为科学(实验)终点,这些情况均与常规实验动物福利和伦理理念相违背[2]。同时,与常规动物实验相比,感染性动物实验除需要考量和平衡感染性动物实验科学研究目的、动物福利伦理需求外,还应考虑生物安全防护要求[3],针对感染性动物实验福利与伦理的管理工作更加困难、复杂。因此,亟须建立动物福利伦理特殊要求的指导原则或规范。
1 感染性动物实验范围
动物实验是指利用实验动物或其他动物开展的科学研究、教学、检定以及其他实验,包括动物体内实验、使用动物离体器官或组织开展体外实验,以及使用动物源类器官开展的相关实验。利用感染性材料开展的动物实验统称为感染性动物实验。感染性材料包括病原生物以及某些存在潜在生物危害的生物材料[4],通常不包括益生菌及相关产品。
2 感染性动物实验的特殊考量
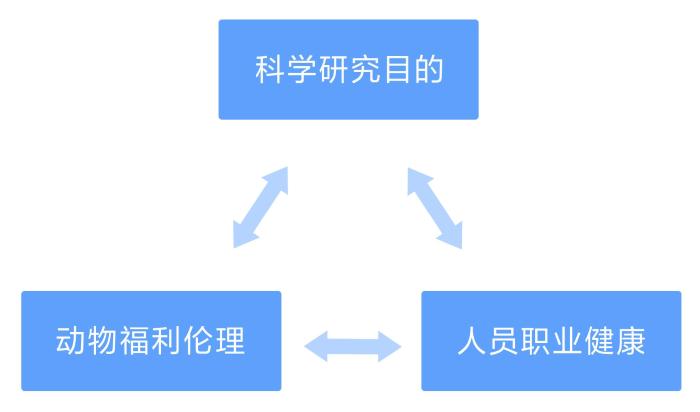
同常规动物实验一样,感染性动物实验需要考虑科研目的与动物福利伦理之间的平衡关系。感染性实验中使用的感染源以及在感染实验过程中产生的气溶胶及其他废弃物不仅可能会导致实验场所污染,还可能会对操作人员造成潜在生物危害。因而,人员福利及职业健康也是感染性动物实验需要考量的重要因素[3]。病原生物危害等级越高,对生物安全和职业健康安全提出的要求就越高。因此,若在科学研究目的、人员职业健康、动物福利伦理之间实现平衡,则该动物实验方案具备可行性(图1)。当实验设计不能实现科学研究目的,或实验使用的感染源在实验过程中缺乏有效的灭活途径和人员防护措施,或无法提供实现动物福利的方案时,感染性动物实验研究计划不宜被批准实施。
图1
图1
感染性动物实验需考量的三要素
Figure 1
Three factors to consider in infectious animal experiments
2.1 科学研究目的考量
在拟定感染性动物实验研究计划前,首先需要明确研究目的,如开展病原发病机制研究、确定病原毒力、研究宿主易感性或病原耐药性等,以便于确认科学终点;其次,需要系统查阅文献资料,充实研究基础,做到立论依据充足;最后,还应充分了解选择的不同种属动物是否有配套试剂和专用检测设备,如单抗、检测试剂、限定在生物安全实验室范围内专用的Micro-CT等。如实验条件尚未成熟,则不宜开展相关动物实验[4]。
2.2 人员职业健康考量
应制定详细的感染性动物实验风险评估报告。风险评估报告应涵盖感染源的相关生物学特性、生物危害等级要求、预防与治疗措施、实验活动风险,以及管理规范、生物安全等级达标的动物设施、相配套的生物安全设备和个体防护要求等内容,据此来评估机构所具备的现有条件及项目组成员的能力,以确认该机构是否胜任项目的开展;还应考虑到特殊人群(免疫力异常者、妊娠期女性等)不宜参与感染性动物实验。
2.3 动物福利伦理考量
由于感染实验设施的特殊性和感染引起的损伤等因素,动物会出现与“五大自由”不符的状态,甚至在实验中常以自然死亡为科学终点。为了达成科学研究目的,动物又必须承受这些痛苦和不适,因此在制定感染性动物实验方案时,要充分应用“3Rs”原则。当该动物实验不能采用体外实验或其他方法替代时,应充分考虑并满足动物福利伦理的要求。对于为获得科学研究目的无法缓解动物痛苦或以自然死亡为终点的实验,同时要制定合适的纳入和排除机制[5],确保在动物福利受到影响的时候,能够采取有效的方式开展“人道干预终点”[6]。Felgenhauer等[7]在开展流感相关研究中很好地利用了人道干预终点,在动物体重减少超过30%,且出现严重呼吸困难、濒死时,及时对动物实施了安乐死。此外,还需探讨如何通过优化实验流程,或通过体外模拟和预实验,减少体内实验所需的动物数量。只有充分考量“3Rs”原则,将其进一步应用到实际方案设计中,才能够将感染性动物实验对动物福利的负面影响降至最低。
3 实验动物福利与伦理通用要求
3.1 五大自由
“五大自由”即不受饥渴的自由(生理福利)、生活舒适的自由(环境福利)、不受痛苦伤害和疾病折磨的自由(卫生福利)、表达天性的自由(行为福利)、无恐惧和悲伤的自由(心理福利)。其基本出发点是让动物在健康和快乐(well-being)的状态下生存,或在无痛苦的状态下快速死亡,在极端保护动物与极端利用动物之间找到平衡点。
3.2 “3Rs”原则
“3Rs”原则在获得了广泛认可的同时,也在不断发展。近年来,在“3Rs”基础上诞生了第四个“R”,目前对此尚未形成统一认识,多归结为对无结果实验动物使用计划的“拒绝(refusal,R)”或对实现实验动物价值及保障动物实验科学性的“责任(responsibility,R)”。无论是“3Rs”或“4Rs”,都是为了在不损害科学利益的前提下,最大程度地减少对实验动物的伤害。如何在感染性动物实验过程中利用“3Rs”原则指导实验,是目前从事感染性动物实验的科研人员面临的主要问题。由于感染性实验会给动物造成不可避免的痛苦和不适,因此,科研人员需充分考虑采用体外实验(细胞、类器官)等“替代”方法来实现“科学研究目的”。“减少”即减少动物用量,需要通过预实验或其他实验结果的推理,科学地计算出能达到“科学研究目的”前提的最少动物用量。在计算过程中,还应考虑到因感染性实验中动物死亡带来的“减员”现象等因素,这些因素的推理和计算都需要充分研判预实验的结果。“优化”即提升现有的实验条件或技术方法,在缓解动物福利压力的同时,能够实现动物实验结果的高效产出。在结合“3Rs”原则规范实验设计、实施、报告等整个动物实验研究过程方面,建议使用ARRIVE 2.0指南以及该指南所涉及的Experimental Design Assistant(EDA)实验设计平台(
4 感染性动物实验的特殊福利伦理要求
表1 常规动物实验和感染性动物实验福利要求比较
Table 1
福利因素 Welfare factors | 常规动物实验 Conventional animal experiments | 感染性动物实验 Infectious animal experiments | |
|---|---|---|---|
ABSL-2实验室 ABSL-2 laboratory | ABSL-3/4实验室 ABSL-3/4 laboratory | ||
人员 Personnel | 具备实验动物从业人员上岗资质或经过专业培训 | 除满足实验动物从业人员基本需求外,还应接受生物安全相关培训并通过考核 | 除满足ABSL-2实验室人员要求外,必要时,实验开展前留存本底血清 |
实验动物 Laboratory animal | 遵循“3Rs”原则 | 除满足“3Rs”原则外,动物易感性是核心要求,关注动物体型大小 | 除满足“3Rs”原则外,动物易感性是核心要求,动物体型越小、数量越少越好 |
生存环境 Living environment | 普通环境、屏障环境(正压),笼器具空间尺寸满足《实验动物 环境及设施》(GB 14925—2023)要求 | 负压屏障环境,笼器具空间尺寸满足《实验动物 环境及设施》(GB 14925—2023)要求 | 负压屏障环境,使用生物安全型笼具,笼器具空间尺寸满足《实验动物 环境及设施》(GB 14925—2023)要求 |
社会化管理 Social management | 动物以群居为主 | 啮齿类动物群居为主,大动物单笼饲养为主 | 啮齿类动物群居为主,大动物单笼饲养 |
采食与饮水 Food and water | 自由采食和饮水 | 必要时辅助饮食和特殊照顾 | 必要时辅助饮食和特殊照顾 |
交叉污染控制 Cross contamination control | 同一实验间可以多项目兼容 | 采取有效的隔离措施,同一实验间可以多项目兼容,但应按病原特性分类管理 | 同一实验间只能从事一种病原感染实验 |
兽医护理 Veterinary care | 正常兽医护理 | 特殊兽医护理 | 特殊兽医护理 |
人道终点 Humane endpoint | 必要时设置人道终点 | 出于生物安全风险控制要求,必须设置人道终点 | 必须设置人道终点 |
实验终点 Experimental endpoint | 动物可以存活和重复利用 | 动物死亡 | 动物死亡 |
4.1 人员要求
从事感染性动物实验的人员除了对专业素质、科学理念、技术操作等因素提出较高要求外,还应接受全面的职业健康和生物安全培训,熟悉实验动物福利的评估要求,清楚实验活动中的风险及应采用的防护措施。此外,应配置专职兽医。兽医应参与制定研究方案及实验活动的全过程,并能对涉及动物福利的情况作出准确预判。管理层赋予实验动物使用与管理委员会(Institutional Animal Care and Use Committee,IACUC)、兽医和兽医技术人员权限处理有特殊福利与伦理需求的动物,如采取安乐死措施。在感染性动物实验开展过程中,IACUC、兽医以及机构负责人之间的沟通显得格外重要。机构应对感染性动物实验提供足够的资源进行支持,以确保实验顺利、安全地实施,避免发生生物安全事件。同时,IACUC应充分对感染性动物实验的研究计划进行科学判断,讨论其必要性和科学性,在以能够解释科学问题为目标的基础上批准相关研究计划。兽医人员需对即将开展和已经开展的感染性动物实验行使监督权利,若出现与动物福利相违背的事件,应第一时间与研究小组进行沟通,并处置动物,以确保动物福利的有效落实。
4.2 实验动物选择标准
4.2.1 依据研究目的
4.2.2 依据福利、伦理及生物安全要求
由于涉及生物安全管理,感染性动物实验在动物选择方面要求更加严格,首选条件是动物的易感性。首先,应选择易感动物,且等级越高、标准化程度越高越好,如选择无菌动物或悉生动物可以更好地获得预期结果。在确保能达到研究目的的前提下,优先选择进化程度较低的动物[17]。其次,选用的动物数量必须符合统计学要求,尽量做到数量最少化。此外,由于同一种实验动物存在个体差异,还应高度重视个体的选择:(1)年龄。一般均选用成年动物来进行实验,但是对于病毒分离相关研究则优先选择幼龄期动物。(2)性别。在实验研究中,应根据多方面因素来选择动物的性别,如应考虑雌激素的保护作用、雄性动物的不相容性等因素。(3)生理状态。选用状态良好的实验动物,不宜采用处于妊娠、哺乳期的雌性动物。
4.2.3 依据其他因素
在建立感染性疾病动物模型过程中,实验病原种类不同、病原接种途径不同、采集的样本量不一致,都会影响到实验动物种属和体型大小的选择。因此,应充分考虑各种可能的因素,尽量降低实验动物不适合的风险。对于新型的模式动物,还应充分考虑是否有特异性的试剂与耗材。
4.3 生存环境管理及设施设备
感染性动物实验应在负压屏障环境设施内开展,同时设施符合生物安全实验室的相关标准要求[18]。实验动物笼器具应无毒无害,表面光滑无倒刺;饲养空间和饲养方式满足动物需求。由于动物生存微环境为负压,与生产繁育设施差异大,新进动物的适应性饲养观察时间(检疫)可能会延长,基础生理生化指标稳定需要更长的周期。
环境丰富化是保障动物福利的重要途径,但是动物感染病原后,通常会出现活动减少甚至嗜睡的症状。在这种情况下,环境丰富措施不宜过度,以免影响动物的活动。啮齿类动物感染后通常伴有体温的损失,非人灵长类动物的体温则会升高。面对这种情况,应当采取必要的措施维持实验动物的体温相对稳定[19]。
在交叉污染控制方面,感染性动物实验室有很高的要求。尽管ABSL-2实验室在采取有效的隔离措施时,同一实验间可以兼容多个项目,但仍建议按病原的特性进行分类管理,例如消化道传播的病原和空气传播的病原应相对分开。ABSL-3/4实验室则应严格按照实验室认可适用范围和审批要求,执行单房间单病原管理。
4.4 特殊照料和兽医护理
对于行动困难、食欲低下及其他需要特殊关照的动物,应当采取必要的特殊照料或辅助饮食的措施,采取的措施应获得本机构IACUC和项目负责人的批准。这类措施应有助于满足动物的基本生理和心理需求,包括提高环境温度、改变食物性状、提供高营养和适口性强的食物、优化垫料或做巢材料等。
动物感染疾病后的疾病进展、反复保定和损伤性采样等均会加重动物的痛苦和伤害。因此,实验设计中应充分考虑药物干预或特殊医学护理的必要性。药物治疗或特殊兽医护理对实验结果的影响应该有文献、预实验结果或其他技术资料的支持,否则不能简单地因为“可能会影响实验结果”而拒绝采取减少疼痛和痛苦的兽医护理措施。例如,吗啡能加速沙门菌感染小鼠模型的疾病进展,并增强沙门氏菌在小鼠中的传播性,影响小鼠存活率和平均生存时间,在沙门菌感染动物疾病模型研究中需慎用[24];而布洛芬可以有效缓解小鼠疼痛而不影响弓形虫感染的疾病进展,值得在弓形虫体内感染研究中推广[25];药效学评价中增加治疗或药物干预更能模拟人类患者的疾病进展[4]。
是否采取特殊兽医护理需要充分考虑以下5项因素:干预措施对病程进展是否有影响,感染导致的脱水、无法正常采食等对潜在治疗方法或慢性病是否有影响,采取药物干预或支持性护理的动物感染模型可能更好地模拟现实中患者的体况,动物所经历的预期疼痛或痛苦程度是否会显著改变其免疫反应,动物感染模型承受的痛苦和伤害在人类疾病患者身上基本不会发生。
4.5 人道终点
感染性动物实验的疾病进展会给动物带来持续的福利问题。因此,每个实验方案均应建立针对特定病原感染的人道终点评价体系。通常不同病原对应的人道终点不同,不能一概定论。感染性动物实验人道终点的评价体系主要基于动物的状态和行为,包括但不限于以下5项指标[2,4,28]:(1)体重变化。表现为体重快速下降(如下降10%~20%)、动物完全不摄食或摄食明显减少、未监测到体重变化但出现恶病质等情形。(2)体温变化。体温显著降低,通常低于34 ℃[29],触之冰冷。(3)体征变化。全身性脱毛或被毛粗乱,持续性倦怠伴随蜷缩、弓背、目光呆滞、嗜睡或持续躺卧等。(4)生理指标。动物在感染过程中,机体功能和代谢发生不可逆的损伤,严重影响动物健康的情形,如炎症因子风暴的诱发。(5)异常行为。包括活动性下降、警觉性下降、刻板行为、自残、焦躁不安等。
5 感染性动物实验福利与伦理的实施管理
由于感染性动物实验涉及生物安全管理,所有动物实验方案均应先提交机构生物安全委员会进行审查,通过审查后再提交IACUC进行福利与伦理审查。
动物福利与伦理工作应进行闭环管理。动物实验活动开始之前,确定好动物福利伦理措施;动物实验活动开展过程中做好日常监督;动物实验活动实施完成后,应审查福利与伦理措施的有效性;IACUC与兽医应全程参加动物福利与伦理的管理工作[30]。
研究人员提交的感染性动物实验方案应有平衡科研目的与动物福利伦理的说明;明确潜在的动物福利伦理问题及必要的干预措施;提供实验终点和人道终点,尽可能避免以动物死亡作为实验终点[3]。研究人员、兽医师、护理人员和IACUC应熟悉人道终点评价体系,并能客观地评价人道终点。
当生物安全风险控制与动物福利伦理要求相冲突时,应遵循“风险优先与最小伤害平衡原则”。在法定框架下,生物安全是国家安全的重要组成部分,强调的是防范和应对生物风险,保障人民生命健康和国家安全。因此,研究人员首先需要严格执行《生物安全法》关于病原体管理和实验室生物安全的规定,同时遵守《科技伦理审查办法(试行)》(国科发监〔2023〕167号)对实验动物使用的伦理审查要求,通过优化实验设计、改进操作流程等方式,将动物福利损害降至最低,例如采用“仁慈终点”操作及时终止动物痛苦。在IACUC进行福利与伦理审查时,需重点关注研究的必要性和研究人员是否明确了感染性动物实验中两者的平衡点。生物安全和动物福利伦理并不是完全对立的概念,通过科学管理和伦理审查,既能有效保障实验动物的使用符合科学研究的需要,又能确保实验动物在使用过程中不受虐待和被过度使用。
6 总结和展望
感染性动物实验不可避免地会导致动物持续产生疼痛、痛苦和悲伤,这对动物福利和伦理提出了极高的要求。如何有效平衡科研目的与动物福利伦理及生物安全的关系,是研究人员需要深入设计规划、IACUC审查与监督的核心内容。感染性动物实验中的人道终点至关重要,需充分利用“科学终点”、“人道干预终点”以及“累计终点”来确保动物的福利的实施:将动物生存率作为病原致病性研究、评价疫苗或药物的关键指标,动物死亡仅作为实验终点;目前已建立人道终点指标的感染性实验,如流感病毒研究,不得以实验动物自然死亡为评价指标;对于目前仍然以动物自然死亡作为科学终点的研究,应该思考如何减轻动物痛苦,或在动物濒死时立即终止实验的情况下如何达到研究目的。因此,动物实验相关人员均应接受人道终点评价体系培训,客观地评价人道终点。
实验动物福利落实在人,包括科研人员、IACUC成员、兽医、实验操作人员及饲养人员。各个环节的人员都应秉承科学精神,心怀仁义道德,对实验动物负责,善待实验动物生命,维护实验动物福利伦理。实验动物的福利问题关系到科学结果的准确性、科学家在公众心目中的形象,也影响到公众对科学研究的认可度,在多领域全方位践行实验动物福利可助力于我国科技大国形象和科技创新能力的提升。
[引用本文]
闵凡贵, 富宏坤, 刘永刚, 等. 感染性动物实验的福利与伦理特殊要求[J]. 实验动物与比较医学, 2025, 45(2): 239-246. DOI: 10.12300/j.issn.1674-5817.2024.122.
MIN F G, FU H K, LIU Y G, et al. Special welfare and ethical requirements for infectious animal experiments[J]. Lab Anim Comp Med, 2025, 45(2): 239-246. DOI: 10.12300/j.issn.1674-5817. 2024.122.
作者贡献声明
闵凡贵负责收集资料、写作初稿和整理数据;
富宏坤参与策划方案、收集资料和修订文章;
刘永刚参与策划方案、审查和修订文章;
刘香梅、刘忠华和李垚参与收集资料和修订文章;
陶雨风负责策划方案、审查和修订文章。
利益冲突声明
所有作者均声明本文不存在利益冲突。
参考文献
感染性疾病动物模型标准化应用问题探讨
[J].
Discussion on standardized application of animal models of infectious diseases
[J].
Humane endpoints for infectious disease animal models
[J].
IACUC and veterinary considerations for review of ABSL3 and ABSL4 research protocols
[J].
Considerations for infectious disease research studies using animals
[J].
动物实验研究报告的国际指南ARRIVE 2.0介绍及期刊实施计划
[J].
Introduction to the international guide for animal research reporting ARRIVE 2.0, and its implementation plan in the journal
[J].
加拿大动物人道终点指南解析
[J].
A brief interpretation of CCAC guide on humane endpoints of animals: 2022 edition
[J].
Evaluation of nutritional gel supplementation in C57BL/6J mice infected with mouse-adapted influenza A/PR/8/34 virus
[J].
Assessing measures of animal welfare
[J].
善待实验动物的伦理学原则浅析
[J].
Analysis on ethical principles of treating experimental animals well
[J].
探讨«关于善待实验动物的指导性意见»饲育、应用、运输及相关方面的措施
[J].
To explore the feeding, application, transportation and related measures of Guiding Opinions on Treating Experimental Animals Well
[J].
«动物研究: 体内实验报告»即ARRIVE 2.0指南的解释和阐述(一)
[J].
Explanation and elaboration for the ARRIVE guidelines 2.0-reporting animal research and in vivo experiments (Ⅰ)
[J].
在动物实验基本操作过程中提高实验动物福利
[J].
Improve the welfare of experimental animals in the basic operation process of animal experiments
[J].
Animal welfare and resistance to disease: interaction of affective states and the immune system
[J].
Long- and short-time immunological memory in different strains of mice given nasally an adjuvant-combined nasal influenza vaccine
[J].
H5N1 pathogenesis studies in mammalian models
[J].
Replacement, refinement, and reduction in animal studies with biohazardous agents
[J].
非人灵长类动物感染性实验中的福利问题
[J].
Welfare problems in infectious experiments of non-human primates
[J].
Balancing the welfare: the use of non-human Primates in research
[J].
The use of positive reinforcement training techniques to enhance the care, management, and welfare of Primates in the laboratory
[J].
Nonhuman primate welfare in the research environment
[M]//
Morphine increases susceptibility to oral Salmonella typhimurium infection
[J].
Buprenorphine does not affect acute murine toxoplasmosis and is recommended as an analgesic in Toxoplasma gondii studies in mice
[J].
The application of humane endpoints and humane killing methods in animal research proposals: a retrospective review
[J].
The HID50 (hypothermia-inducing dose 50): an alternative to the LD50 for measurement of bacterial virulence
[J].
IACUC在AAALAC体系中的作用与运行实践
[J].
Roles of IACUC in AAALAC management system and our operating practices
[J].
关于我国实验动物福利伦理的思考及建议
[J].
Reflections and suggestions on the ethics and welfare of laboratory animals in China
[J].
实验动物福利伦理审查发现问题之思考
[J].
Reflection of the problems found in the ethical review of experimental animal welfare
[J].